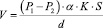диффузионные формы дыхательной недостаточности
Вопрос 4 Диффузионные формы дн
Дыхательная недостаточность по диффузному типу развивается при нарушении проникновения газов через капиллярно-альвеолярную мембрану легких при ее патологическом утолщении. Пpичинами диффузионной дыхательной недостаточности являются пневмокониоз, фибpоз и шоковое легкое, пpи котоpом в следствие глубоких наpушений пеpифеpической микpоциpкуляции обpазуются агpегаты фоpменных элементов кpови, вызывающие микpоэмболию спазмиpованных легочных капилляpов.
Диффузионная недостаточность может быть связана:
а) с уменьшением поверхности или площади диффузии (резекция легочной ткани, эмфизема, фиброз легких),
б) с нарушением диффузии газов.
Нарушение диффузионной способности легких (ДСЛ) наблюдается при:
-уменьшении времени контакта крови с альвеолярным воздухом (время прохождения крови по капиллярным сосудам легочных альвеол составляет 0,5-0,6c, а для полной диффузии газов достаточно всего 0,2 с. Однако такое время диффузии характерно для нормальной альвеолокапиллярной мембраны. Если же она изменена, то при значительном ускорении кровотока (при физической нагрузке, анемии, горной болезни и др.) газы не успевают в достаточном количестве диффундировать через альвеолокапиллярную мембрану и тогда меньшее количество гемоглобина связывается с кислородом)
Нарушение ДСЛ сопровождается гипоксемией без гиперкапнии. Простейшим функциональным тестом для выявления этих нарушений ДСЛ является произвольная гипервентиляция. При этом имеющаяся у больного гипоксемия не устраняется, а, наоборот, усугубляется, что обусловлено несоответствием потребности в О2 активно работающими дыхательными мышцами и его обеспечением.
Вопрос 5 Нарушение вентиляционно-перфузионных соотношений
В норме вентиляционно-перфузионныгй показатель равен 0,8-1,0 (т.е. кровоток осуществляется в тех участках легких, в которых имеется вентиляция, за счет этого происходит газообмен между альвеолярным воздухом и кровью). Если в физиологических условиях в относительно небольшом участке легкого происходит снижение пар-
циального давления кислорода в альвеолярном воздухе, то в этом же участке рефлекторно возникает местная вазоконстрикция, которая приводит к адекватному ограничению кровотока (по рефлексу Эйлера-Лильестранда). В результате местный легочный кровоток приспосабливается к интенсивности легочной вентиляции и нарушений вентиляционно-перфузионных соотношений не происходит.
При патологии возможны 2 варианта нарушений вентиляционноперфузионных соотношений (рис. 16-3):
Диффузионные формы дыхательной недостаточности
7.1. Механизмы нарушения альвеолярного дыхания
Как известно, газообмен в легких происходит благодаря диффузии газов через альвеолярно-капиллярную мембрану по градиенту концентрации 02 и С02. Объемная скорость диффузии определяется по формуле:
К- константа диффузии;
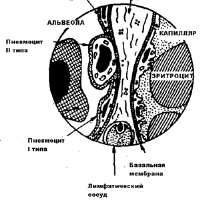
Рис.10. Схема альвеолярно- капиллярной мембраны ( Воложин А.И.,2000)
Недостаток внутрилегочного сурфактанта служит первопричиной развития респираторного дистресс-синдрома новорожденных у недоношенных детей.
Своеобразие патологии дыхательной системы у детей раннего возраста может быть обусловлено особенностями ее строения и функции. Наличие узких носовых ходов, а также длинных, узких и малоразветвленных бронхов, обилие межуточной ткани, кровеносных и лимфатических сосудов в легких способствуют возникновению разнообразных пневмопатий, которые лежат в основе синдрома дыхательных расстройств (СДР) у значительного числа новорожденных.
Наиболее частой и тяжелой формой пневмопатий являются гиалиновые мембраны, особенно у недоношенных детей, развивающихся в условиях патологического течения беременности и родов. В образовании гиалиновых мембран, состоящих из фибрина, сывороточных протеинов и клеточных элементов, патогенетическую роль играет недостаточность фибринолитической системы. К нарушению фибринолитических процессов и ретенции фибрина в альвеолах может предрасполагать дефицит плазминогена. Гиалиновые мембраны располагаются в просвете альвеолярных ходов, альвеол, легочных бронхов, лежат как уплотненные массы в просвете свободно или выстилают стенки дыхательных путей, способствуя их обтурации, нарушению легочной вентиляции, развитию гипоксемии, вазоконстрикции сосудов и гипоперфузии легких. В то же время возникают инактивация альвеолярного сурфактанта, ухудшение расправления легочной ткани и развиваются обструктивно-рестриктивные формы ДН у детей.
Течение СДР может быть острым и подострым. В период восстановления исчезают признаки ДН и нарушения функции ЦНС, нормализуется кровообращение, исчезают отеки. Однако у детей, перенесших СДР, возможно развитие хронической легочной патологии. В ряде случаев развитие бронхолегочной дисплазии связано с незрелостью бронхоальвеолярной системы легких и изменениями, обусловленными гиалиновыми мембранами. К ним относятся бронхиолярный и интерстициальный фиброз, облитерирующий бронхиолит с интерстициальным некрозом. Возникающая при этом хроническая ДН сопровождается гипоксемией, гиперкапнией и гипоксией разных органов и тканей.
7.2. Респираторный дистрресс-синдром. Этиология и патогенез
В последние годы для оценки этиологии и патогенеза ДН используют термин острый респираторный дистресс-синдром (ОРДС), который может возникать у детей и взрослых.
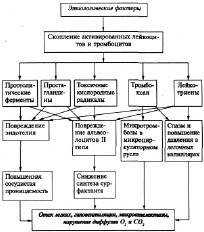
Рис.11. Патогенез РДСВ (А.Н. Окороков, 2005)
Он является завершающей фазой многообразных повреждений легких (инфекционными патологическими агентами, токсинами бактериального и небактериального происхождения, медиаторами альтерации. ОРДС может быть следствием травмы грудной клетки, ее длительного сдавления, аутоиммунных заболеваниях и т.д. Однако ОРДС клинически проявляется одышкой, кашлем, с выделением мокроты, имеющей примесь крови, мелкопузырчатыми влажными хрипами в легких, цианозом, не исчезающим даже при оксигенотерапии.
Первое описание клиники ОРДС было в 1946 году, однако название указанной патологии претерпело многочисленные изменения, включающие такие названия, как острое повреждение легких (ОПЛ), «мокрые легкие», «тяжелые легкие», «шоковые легкие», «фиброзирующий альвеолит», «некардиогенный отек легких». В 1967 Эсбахом было предложено название «острый респираторный дистресс синдром», характеризующийся крайне тяжелым острым повреждением легких. Отличительными признаками ОРДС являются:
3) двустороннее поражение легких на Ro;
4) давление заклинивания легочной артерии ≤ 18 мм. рт. ст.
ОРДС принято делить по степени тяжести, по величине индекса оксигенации (PаO2) на следующие формы:
– тяжелый (критический) вариант патологии PаO2/Fi O2
Диффузионные формы дыхательной недостаточности
6.1. Патогенез обструктивной формы дыхательной недостаточности
1) обтурации (закупорки воздухоносных путей инородными телами, рвотными массами, мокротой, слизью, меконием (у новорожденных); воспалительных изменений слизистой оболочки дыхательных путей, гиперсекреции и диссекреции слизи, задержки в дыхательных путях патологического отделяемого (рис.7,8);
Рис.7. Обструкция дыхательных путей
Рис.8. Обструкция дыхательных путей у курильщика
2) компрессии (сдавления) дыхательных путей опухолью, гипертрофированной щитовидной железой, заглоточным абсцессом;
3) утолщения слизистой оболочки трахеи и бронхов вследствие отека слизистой дыхательных путей и клеточной нифильтрации при воспалении, иммуноаллергическом процессе;
4) стеноза при спазме мышц гортани психогенного (истерия) или рефлекторного характера (раздражение газообразными веществами), при формировании послеожогового рубца, при клапанной обструкции бронхов, характерной для хронической обструктивной эмфиземы легких; в результате утраты легкими эластических свойств и нарушения тонуса бронхиальной мускулатуры может развиться дискинезия (экспираторный стеноз) дыхательных путей.
Патогенетическую основу обструктивного синдрома дыхательных путей составляет повышение сопротивления воздушному потоку. Это приводит к тому, что снижается уровень альвеолярной вентиляции. Повышение сопротивления увеличивает нагрузку на дыхательную мускулатуру, и наблюдается быстрое утомление мышц. У больного развивается стенотическое дыхание (удлинение вдоха, т.е. инспираторная одышка).
Достаточно часто в клинической практике наблюдается хроническая бронхиальная обструкция, которая обозначается термином «хроническая обструктивная болезнь легких» (ХОБЛ). Причинами развития ХОБЛ являются: хронический бронхит (это самая частая причина), бронхиальная астма, эмфизема легких, муковисцидоз, бронхоэктатическая болезнь.
Обструкция конечного отдела дыхательных путей наблюдается при бронхо- и бронхиолоспазмах, спадении мелких бронхов, утративших эластичность, сужении просвета бронхиол вследствие отечно-воспалительных изменений, обтурации бронхиол патологическим содержимым (кровью, экссудатом), компрессии бронхиол в условиях повышенного внутригрудного давления (при кашле). При обструкции нижних дыхательных путей для осуществления полноценного выдоха необходимо участие дыхательных мышц, так как сила эластической тяги легких недостаточна для изгнания воздуха из альвеол. Давление и бронхиальное сопротивление на выдохе более выражены, чем на вдохе, при этом возникает удлинение выдоха по сравнению с вдохом (экспираторная одышка).
6.2. Патогенез рестриктивной формы дыхательной недостаточности
а) внелегочные факторы приводят к ограничению дыхательных движений вследствие сдавления легочной ткани (например, при гемо- и пневмотораксе, образовании плеврального выпота);
б) внутрилегочные факторы вызывают изменение эластичности легочной ткани. Основой рестриктивных нарушений является повреждение белков интерстиция под действием эластазы, коллагеназы и других протеаз. Как известно, основными компонентами интерстиция легких являются коллаген (60-70%), эластин (25-30%). Гликозаминогликаны составляют около 1%, а фибронектин – 0,5%. Фибриллярные белки обеспечивают стабильность каркаса легких, его растяжимость, эластичность, создают оптимальные условия для газообмена. При ряде патологических процессов в легких (воспалительного характера, нарушениях кровотока, при тромбозе, эмболии сосудов, застойных явлениях в легких, эмфиземе, опухолевом и кистозном поражении) возможна активация лизосомальных гидролаз, в частности, эластазы, коллагеназы. Последняя приводит к интенсивному распаду фибриллярных белков, что проявляется снижением эластичности легочной паренхимы и повышением эластического сопротивления легочной ткани вдыхаемому воздуху.
Снижение эластичности легочной ткани и развитие рестриктивной формы дыхательной недостаточности возникают при диффузном межальвеолярном разрастании соединительной ткани в случаях пневмосклероза, пневмофиброза, а также при отеке легких различного генеза.
Рестриктивные изменения легочной ткани обуславливают уменьшение глубины вдоха и вызывают тахипноэ, т.е. развивается «короткое» или поверхностное дыхание.
Достаточно часто в клинической практике наблюдается дыхательная недостаточность смешанного обструктивно-рестриктивного характера, когда сочетаются нарушение проходимости воздухоносных путей и ограничение подвижности легких. Последнее наблюдается при эмфиземе легких, крупозной пневмонии, бронхиальной астме, бронхоэктатической болезни, хронической пневмонии т.д.
Диффузионные формы дыхательной недостаточности
5.1. Дыхательная недостаточность: виды и механизмы развития
Дыхательная недостаточность – патологическое состояние, характеризующееся истощением функциональных систем по поддержанию нормального газового состава крови. В соответствии с этим определением различают гипоксемическую и гиперкапническую формы дыхательной недостаточности.
По темпу развития различают острую (развивающуюся в течение нескольких минут или часов) и хроническую (развивающуюся в течение нескольких дней или недель) формы дыхательной недостаточности (ДН).
По степени компенсации:
1) компенсированную форму дыхательной недостаточности, когда нет изменений газового состава крови при обычной физической нагрузке, но это достигается в результате напряжения регуляторных механизмов и дыхательная недостаточность выявляется при проведении нагрузочной пробы;
2) декомпенсированную дыхательную недостаточность, при которой возникает изменение газового состава крови уже в состоянии относительного покоя. Декомпенсированная форма дыхательной недостаточности подразделяется на следующие виды в зависимости от степени нарушений газового состава крови:
в) комбинированный вариант – гипоксемически-гиперкапническая.
По патогенезу выделяют следующие формы дыхательной недостаточности:
внелегочную форму дыхательной недостаточности, в основе которой лежат следующие патогенетические факторы: 1) нарушение нервной регуляции дыхательной мускулатуры; 2) патология дыхательной мускулатуры, костно-суставного каркаса, грудной клетки; 3) нарушение кровотока в малом круге кровообращения (например, при левожелудочковой сердечной недостаточности, гиповолемии);
дыхательную недостаточность с преимущественным нарушением бронхо-легочных механизмов: соответственно, различают обструктивную, рестриктивную, смешанную формы дыхательной недостаточности.
5.2. Патогенез внелегочной формы дыхательной недостаточности
В основе развития внелегочной формы дыхательной недостаточности лежит или нарушение нервной регуляции дыхания, или изменение структуры и функциональной активности костно-мышечного аппарата грудной клетки, не обеспечивающего достаточной глубины дыхательных движений. Внелегочная форма дыхательной недостаточности может быть обусловлена следующими факторами:
снижением возбудимости бульбарного дыхательного центра при воздействии различных патогенных факторов: бактерий, токсинов, вирусов, снотворных веществ, наркотических препаратов, транквилизаторов, ксенобиотиков и других;
развитием локальной патологии в структурах продолговатого мозга (воспаление, травма, ишемия, опухоль, отек, коматозные состояния, нарушение мозгового кровообращения);
дефицитом возбуждающей афферентации (например, при синдроме асфиксии новорожденного, возникающем вследствие незрелости хеморецепторного аппарата ребенка, чаще недоношенного). Для активации дыхательного центра в условиях указанной патологии обычно используют дополнительные стимулирующие воздействия на кожные экстерорецепторы (похлопывание, обрызгивание), ликвидируя тем самым дефицит возбуждающей афферентации через неспецифическую активацию ретикулярной формации;
избытком тормозной афферентации, когда угнетается ритмическая активность дыхательного центра. Это наблюдается при раздражении рецепторов слизистой оболочки верхних дыхательных путей при ОРЗ воспалительного характера, при интенсивном раздражении слизистой полости носа и носоглотки газообразными химическими и механическими агентами, что может вызывать рефлекторную остановку дыхания на выдохе;
патологией эфферентных структур на различных уровнях, когда нарушается связь дыхательного центра с дыхательными мышцами. Так, повреждение кортико-спинальных путей (например, при травме) приводит к тому, что утрачивается способность к произвольному контролю дыхания, оно становится неестественно регулярным, “машинообразным”, с периодически повторяющимися усиленными вставочными вдохами. При прерывании проводящих путей, связывающих дыхательный центр с диафрагмальными мотонейронами (например, при рассеянном склерозе, полиомиелите, нарушении кровообращения спинного мозга, травме), дыхание утрачивает свой автоматизм. Больной дышит только произвольно, дыхание неравномерно, а при засыпании прекращается;
подавлением активности спинальных фазических мотонейронов шейного и грудного отделов, ответственных за иннервацию дыхательных мышц (диафрагмы и межреберных мышц);
развитием воспалительно-деструктивных процессов в межреберных и диафрагмальном нервах под влиянием бактерий, токсинов, факторов иммуноаллергической природы;
миогенными расстройствами дыхания, которые возникают при нарушении функции дыхательной мускулатуры. Патология может быть связана с блокадой нервно-мышечных синапсов (при использовании миорелаксантов, при воздействии ботулинического токсина, яда кураре, отравлении ФОС). Альвеолярная гиповентиляция миогенного происхождения наблюдается при миалгиях, миодистрофиях, травмах дыхательных мышц, тугоподвижности ребер, пневмотораксе, а также у практически здоровых людей с недостаточно развитой дыхательной мускулатурой при выполнении ими значительной физической нагрузки. Пороки развития, опухоли и кисты диафрагмальной мышцы способствуют развитию дыхательной недостаточности. При тотальном параличе диафрагмы возникает парадоксальное дыхание: при вдохе эпигастральная область западает, а на выдохе выбухает (симптом Черни).
Острая дыхательная недостаточность
Эффективное лечение любой патологии, в том числе и дыхательной недостаточности, возможно только при детальной диагностике форм этой недостаточности. В свою очередь, диагностика должна исходить из патофизиологических механизмов развития любой формы нарушения внешнего дыхания. Именно поэтому обсуждение дыхательной недостаточности приходится начинать с анализа этих патофизиологических механизмов.
Такая постановка вопроса стратегически правильна, поскольку дает возможность начать детальное обследование больного раньше того времени, когда появятся нарушения газового состава крови, и, следовательно, процесс станет более запущенным, а лечение запоздалым. Кроме того, определение дыхательной недостаточности обращает внимание на компенсаторную реакцию (одышку) в ответ на уже имеющиеся нарушения в системе внешнего дыхания.
Предложенное определение дает основание считать, что дыхательная недостаточность (ДН) имеет в своей основе либо уже развившееся, либо потенциально возможное нарушение газообмена, а потому выделение форм или видов дыхательной недостаточности должно быть непременно связано с поисками конкретных патофизиологических механизмов развития этих нарушений. Название вида дыхательных нарушений может быть обусловлено только механизмом развития дыхательной недостаточности (нарушения газообмена). Участие нескольких механизмов в формировании смешанных форм ДН (которые встречаются часто) не противоречит такому условию, тем более что включение разных механизмов в процесс происходит не одновременно, а последовательно. Это дает возможность их диагностировать и одновременно уточнять стадию развития ДН.
Известно несколько патофизиологических механизмов, ответственных за развитие нарушений газообмена в легких (обмена О2 и СО2):
1. Тотальная гиповентиляция, формирующая вентиляционную ДН (ВДН).
2. Нарушение диффузионной способности легких.
4. Локальная гиповентиляция.
5. Локальное нарушение кровотока в малом круге кровообращения.
6. Тотальное нарушение кровотока в малом круге кровообращения.
Таким образом, признаками или симптомами ВДН являются:
Обращаем внимание на патогномоничность всех симптомов (кроме гипоксемии) для этого вида ДН, что облегчает его диагностику.
Известны три группы причин развития тотальной гиповентиляции со снижением МОД.
1. Нарушение центральной регуляции дыхания (угнетение дыхательного центра), которое может быть связано с отеком мозга любой природы (травматической, токсической и др.), с воздействием химических агентов, в том числе и фармакологических (наркотические аналгетики, барбитураты и др.), нарушением кровообращения в стволовых отделах мозга.
2. Механические и другие повреждения аппарата внешнего дыхания: переломы ребер, ранение грудной стенки, в том числе и операционное; гемоторакс, пневмоторакс; высокое стояние диафрагмы при парезах кишечника или повышении давления в брюшной полости; нарушение работы дыхательных мышц при миастении, после перенесенного полиомиелита; гипотрофия.
3. Рестриктивные изменения в легких вследствие гипергидратации (излишние инфузии, левожелудочковая недостаточность), склеротических изменений легочного интерстиция, в том числе и после воспалительных процессов, в старости. В этих случаях снижается эластичность легочной ткани, увеличивается нагрузка на аппарат дыхания при вдохе, что при утомлении дыхательных мышц приводит к гиповентиляции (многие авторы называют это ограничительной ДН).
При нарушении центральной регуляции дыхания ВДН не сопровождается одышкой (угнетение дыхательного центра), а при механических нарушениях аппарата дыхания (в том числе и рестриктивных) одышка имеет характер гипотахипноэ, то есть имеет место увеличение МОД за счет учащения дыхательных движений при резко сниженном дыхательном объеме (ДО). В результате доля анатомического мертвого пространства в ДО увеличивается, а объем, участвующий в альвеолярном обмене, снижается. Это и приводит к уменьшению альвеолярной вентиляции, иначе говоря, к ВДН.
Описанный вид дыхательной недостаточности считается самым распространенным в медицинской практике, однако он далеко не единственный и не самый трудный для диагностики и лечения.
Нарушение диффузионной способности легких. Имеются в виду нарушения диффузии кислорода через альвеоло-капиллярную мембрану. Углекислый газ, имеющий значительно большую, в сравнении с кислородом, диффузионную активность, как правило, проходит через эту мембрану свободно, даже в случае ее утолщения за счет отека интерстициальной (между листками мембраны) клетчатки. Уменьшение проницаемости кислорода из альвеолярного газа в кровь приводит к гипоксемии. Последняя через каротидные хеморецепторы раздражает дыхательный центр, вызывая гипервентиляцию, повышенный выброс углекислоты и гипокапнию. Следовательно, признаками ДН, связанной с нарушением проницаемости О2 альвеоло-капиллярной мембраны, являются:
— гипервентиляция с увеличением МОД;
К сожалению, для диагностики диффузионных нарушений пока не разработан применяемый на практике патогномоничный тест, а перечисленные объективные признаки характерны и для других видов ДН. Используемый в лабораториях тест на диффузионную проницаемость СО2 не может достоверно характеризовать проницаемость кислорода. Кроме того, этот тест не свободен от ошибок, связанных с неравномерностью вентиляции и кровотока в легких.
Диагностика диффузионных нарушений может строиться на выслушивании диффузных мелкопузырчатых хрипов, которые ассоциируются в клинике с альвеолярным отеком различной природы. Альвеолярный отек сопровождается нарушением диффузионной способности легких. Эти нарушения, по-видимому, встречаются не только при отеке альвеол, но в других случаях их можно связывать с гипоксемией только предположительно.
Диффузионные нарушения газообмена, таким образом, характерны для отека легких при левожелудочковой сердечной недостаточности; респираторного дистресс-синдрома в определенной фазе его развития; отеков, которые сопровождают отравление хлором, ожоговые повреждения дыхательных путей, аспирационный синдром. В ряде других случаев, как сказано, диффузионные нарушения можно предполагать, но доказать это предположение трудно (только методом исключения других причин гипоксемии).
Поскольку гипоксемия при нарушении диффузионной способности легких развивается в связи с уменьшением переноса кислорода из альвеол в кровь, лечение больных (устранение гипоксемии) должно быть направлено на увеличение объема этого переноса. Такое увеличение может быть достигнуто за счет роста FiO2, увеличения объема функционирующей альвеолярной поверхности (и объема альвеолярной вентиляции); во время баротерапии. Как и в других случаях дыхательной недостаточности, мерой против гипоксемии может служить и снижение потребности больного в кислороде, в том числе и уменьшение расхода кислорода на работу дыхания за счет ИВЛ, что одновременно может повысить и объем альвеолярной вентиляции.
Разумеется, лечение отека легких не ограничивается коррекцией газообмена, хотя она играет важнейшую роль и в устранении отека. На этом фоне проводится кардиальная терапия, мягкий лаваж бронхиального дерева при отравлении хлором и аспирационном синдроме; принимаются меры, улучшающие бронхиальный дренаж: ингаляционная терапия (включая и спирт, и другие детергенты), побуждение больного к кашлю, вибрационная терапия (ВЧ ИВЛ, наружный вибрационный массаж), антибактериальная терапия.
Диффузионные нарушения газообмена при отеке легких любой природы демонстрируют критическое состояние больного, что требует интенсивной терапии и госпитализации в отделение реанимации.
Снижение концентрации кислорода во вдыхаемой смеси. Участие этого механизма в формировании нарушений газообмена чаще всего имеет место при так называемой горной болезни, когда ограничение FiO2 происходит в связи со снижением атмосферного давления в горах. Вдыхание гипоксической смеси может произойти и в нормальных барометрических условиях, например на операционном столе во время наркоза и ИВЛ. Создание гипоксической смеси в этих условиях всегда следствие либо несчастного случая, либо нарушений техники безопасности и обусловлено нарушением подачи кислорода больному в нужной концентрации.
— гипервентиляция с увеличением МОД;
Как видим, симптоматика та же, что и при нарушениях диффузионной способности легких. Диагностике этой формы ДН помогают пребывание в условиях горного климата, непреднамеренное создание гипоксической смеси, которое можно предотвратить с помощью встроенного в дыхательный контур оксиметра, либо пульсоксиметра.
Обращаем внимание на то, что все три описанные выше механизма нарушения газообмена в легких имеют в своей основе уменьшение переноса кислорода из атмосферы (или дыхательного контура респиратора) в кровь на разных этапах перемещения дыхательной смеси. Кроме того, все эти механизмы воздействуют на всю дыхательную поверхность легких (тотально).
Тотальное нарушение кровотока в системе легочной артерии. Демонстративным примером состояния, при котором происходит тотальное уменьшение объемного кровотока в малом круге кровообращения, является гиповолемия. Нужно подчеркнуть, что сама по себе гиповолемия и уменьшение кровотока в легких имеют лишь косвенное отношение к аппарату внешнего дыхания и могут вызвать лишь гипокапнию. Это происходит благодаря гипервентиляции в ответ на циркуляторную гипоксию, связанную с централизацией кровообращения. Однако неадекватное лечение гиповолемии (запоздалое возмещение ОЦК или возмещение в меньшем или чрезмерном объеме) нередко приводит к тяжелым осложнениям со стороны легких, что по мнению некоторых авторов, играет главную роль в танатогенезе. Имеется в виду как гиперинфузия (в том числе и запоздалая) с гипергидратацией и отеком легких, так и (чаще) последствия несвоевременного и недостаточного возмещения ОЦК с выраженной и длительной централизацией кровообращения и реперфузией, ведущей к развитию респираторного дистресс-синдрома. Свою лепту в развитие легочных осложнений при гиповолемии вносит и синдром массивных трансфузий, связанный не только с иммунологическими конфликтами, но и с переливанием крови с длительными сроками хранения.
Лучшей профилактикой описанных осложнений может быть только своевременное и в должном объеме возмещение ОЦК на основе постоянной информации об операционной кровопотере (в клинике) и скорейшее начало инфузионной терапии при внебольничных кровотечениях, где критерием адекватности переливания служит состояние периферического кровообращения (по данным фотоплетизмограммы на пульсоксиметре). Лечения острого респираторного дистресс-синдрома мы коснемся ниже. Здесь же отметим необходимость возможного уменьшения объема гемотрансфузий, при которых можно использовать консервированную кровь только до трех дней хранения.
Локальная гиповентиляция. Действие этого механизма связано с полной обтурацией бронха (бронхов), неравномерностью вентиляции различных отделов легкого, обструктивными нарушениями в бронхах, увеличением объема экспираторного закрытия (преждевременное спадение бронхов на выдохе). Самое демонстративное проявление локальной гиповентиляции имеет место при полной обтурации бронха (бронхов). В этом случае в соответствующих альвеолах не происходит смены газа, поэтому вскоре газовый состав альвеолярного воздуха выравнивается с газовым составом венозной крови, протекающей по альвеолярным капиллярам. Оксигенация крови прекращается. Венозная кровь тем временем из легких через левые отделы сердца попадает в системный артериальный кровоток. Это венозное примешивание приводит к снижению РаО2 и повышению РаСО2. И гиперкапния, и гипоксемия (через каротидные хеморецепторы) возбуждают дыхательный центр, вызывают одышку и повышенный сброс СО2 в атмосферу. Развивается гипокапния. Несмотря на гипервентиляцию, гипоксемия сохраняется, поскольку венозное примешивание продолжается, а кислородная емкость крови, протекающей через нормально вентилируемые отделы легких, остается прежней, и кровь в этих отделах не может пополниться дополнительным количеством кислорода. Выраженная гипокапния может привести к гипоксии в связи со спазмом периферических сосудов, в том числе и мозговых, и смещением кривой диссоциации оксигемоглобина влево и затруднением освобождения кислорода в ткани. Повышение FiO2 в описанной ситуации гипоксемии не корригирует, так как кислород не может преодолеть блокады бронха и дойти до альвеол и крови.
Аналогичные изменения газообмена происходят и при неполной обтурации бронха (бронхов), чаще всего связанной с увеличением объема экспираторного закрытия дыхательных путей (ЭЗДП) или частичной обструкцией бронхов. Разница состоит лишь в том, что при этих нарушениях увеличение FiO2 уменьшает или снимает гипоксемию, так как увеличение диффузионной активности кислорода (увеличение разницы РО2 между газом проксимальных и дистальных отделов бронхиального дерева) приводит к обогащению кислородом газа в альвеолах.
Признаками (или симптомами) ДН при локальной гиповентиляции являются:
— венозное примешивание (объем шунтирования).
При изолированном увеличении ЭЗДП для коррекции гипоксемии бывает достаточно увеличения FiO2 или ВВЛ.
Чаще всего обтурационная дыхательная недостаточность формируется в связи с нарушением дренажной функции бронхов у больных с воспалительными процессами в бронхах, в послеоперационном периоде, при далеко зашедшем респираторном дистресс-синдроме взрослых (РДСВ). «Поставщиком» такой ДН является и обструктивный процесс в легких. ЭЗДП увеличивается при склеротических процессах в интерстиции, при гипергидратации интерстиция, в ближайшем периоде после абдоминальных операций под общей анестезией.
Локальные нарушения кровотока в легких. Подобные нарушения кровотока развиваются вследствие тромбоэмболии ветвей легочной артерии, жировой эмболии, при блокаде капиллярного кровотока, обусловленного шоковым легким (РДСВ), а также в связи с гравитационной неравномерностью кровотока в легких.
Таким образом, при локальном нарушении кровотока в легких развиваются:
— гипервентиляция с увеличением МОД;
— увеличение альвеолярного мертвого пространства;
Определение VDальв. имеет смысл не только как показатель вида ДН, но и как симптом блокады кровотока при диагностике тромбоэмболии ветвей легочной артерии или шокового легкого.
В комплекс лечебных мер больных с РДСВ, кроме означенных, входит весь перечень, обозначенный в предыдущем разделе: побуждение больного к кашлю, постуральный (смена положения больного в постели с одновременным вибромассажем) дренаж, вибротерапия, фибробронхоскопия, литическая (эндобронхиальная) терапия, кислородотерапия, антибактериальная терапия, ингаляционная терапия.
Обращаем внимание на то, что при локальных нарушениях (вентиляции и кровотока) в легких механизмом нарушения газообмена является венозное примешивание. Перенос кислорода от атмосферы к крови здесь не страдает.
Обращаем внимание читателя на несколько моментов классификации дыхательной недостаточности.
1. Четкое разделение тотальных и локальных процессов в легких.
2. Практически все механизмы развития ДН при тотальных процессах развиваются в связи с нарушением переноса кислорода к крови. Локальные процессы вызывают нарушения газообмена в связи с венозным примешиванием.
3. Только два вида дыхательной недостаточности (гипоксемия) не корригируются ингаляцией кислорода: полная обтурация бронха (бронхов) и локальная блокада капиллярного кровотока в легких.
4. Каждый механизм развития ДН имеет свою «нозологическую» базу, но при некоторых заболеваниях ДН вызывается последовательным включением разных патофизиологических механизмов.
5. Только при ВДН и локальной блокаде кровотока имеются патогномоничные симптомы, при других видах ДН для их диагностики приходится использовать клиническую симптоматику и анамнез.
6. Сам механизм развития ДН несет в себе элементы показаний к тому или иному виду лечения.
Смешанный характер происхождения ДН (нарушения газообмена) лучше всего проследить на конкретных примерах патологии легких. Мы проанализируем два таких примера с точки зрения последовательности включения механизмов, нарушающих легочный газообмен.
Развитие дыхательной недостаточности при прогрессирующей левожелудочковой недостаточности. Снижение выброса левого желудочка по сравнению с выбросом правого вызывает повышение давления в малом круге кровообращения, переполнение сосудов малого круга, интерстициальный отек. Все это снижает эластичность легочной ткани, увеличивает сопротивление вдоху. Больной жалуется на одышку, невозможность сделать полный вдох. При утомлении дыхательных мышц может развиться ВДН с уменьшением ДО, увеличением частоты дыхательных движений, уменьшением объема альвеолярной вентиляции, появлением гипоксемии и гиперкапнии.
Вслед за интерстициальным начинает развиваться и альвеолярный отек, а следовательно, появляются и диффузионные нарушения перехода кислорода в кровь. Гипоксемия усиливается.
Отечная жидкость из альвеол попадает в бронхиолы и бронхи, заполняет отделы бронхиального дерева, становясь препятствием для вентиляции альвеолярной зоны. Таким образом, включается механизм локальной гиповентиляции, усугубляющий гипоксемию.
Проследим последовательность включения механизмов нарушения газообмена.
1. ВДН с гипоксемией и гиперкапнией.
2. Прямое шунтирование с усилением гипоксемии.
3. Нарушение диффузионной способности легких.
4. Локальная гиповентиляция.
Повышение давления в малом круге кровообращения сопровождается интерстициальным отеком со снижением эластичности легочной ткани, увеличением работы дыхания и, возможно (при утомлении дыхательных мышц), развитием ВДН с усилением гипоксемии. Накопление углекислоты в крови и легких в данном случае может маскировать гипокапнию, связанную с одышкой из-за гипоксемии и характерную для локальных нарушений кровотока.
Как и при левожелудочковой недостаточности, интерстициальный отек осложняется отеком альвеолярным с появлением диффузионных нарушений перехода кислорода из альвеол в кровь. Гипоксемия становится более выраженной. Нужно заметить, что появление альвеолярного отека ускоряется деструкцией интимы сосудов огромным количеством метаболитов, попадающих в легкие из зоны реперфузии.
Таким образом, можно проследить последовательность включения различных механизмов нарушения газообмена при эволюции респираторного синдрома:
1. Локальные (множественные) нарушения кровотока, прямое шунтирование и венозное примешивание.
2. Интерстициальный отек и ВДН.
3. Альвеолярный отек и нарушение диффузионной способности легких.
4. Локальная гиповентиляция (многофокусная).
профессор кафедры анестезиологии и реаниматологии.
профессор кафедры анестезиологии и реаниматологии.
Московский государственный медико-стоматологический универстет.
заведующий отделением анестезиологии и реаниматологии
клинической больницы № 4 им. Н.А.Семашко
ОАО «Российские железные дороги», кандидат медицинских наук.