доминантный правый поперечный венозный синус
Поперечный синус
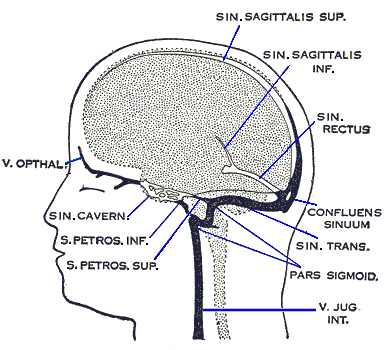
Синусы твёрдой мозговой оболочки (венозные синусы, синусы головного мозга) — венозные коллекторы, расположенные между листками твёрдой мозговой оболочки. Получают кровь из внутренних и наружных вен головного мозга, участвуют в реабсорбции ликвора из субарахноидального пространства.
Содержание
Анатомия
Стенки синусов образованы твёрдой мозговой оболочкой, выстланной эндотелием. Просвет синусов зияет, клапаны и мышечная оболочка, в отличие от других вен, отсутствуют. В полости синусов располагаются покрытые эндотелием волокнистые перегородки.
Из синусов кровь поступает во внутренние ярёмные вены, помимо этого существует связь синусов с венами наружной поверхности черепа посредством резервных венозных выпускников.
Венозные синусы
Клиническое значение
В результате травмы твёрдой мозговой оболочки, которая может быть обусловлена переломом костей черепа, возможно развитие тромбоза синуса. Также тромбоз синуса может развиться в результате неопластического или инфекционного процесса в черепе. В свою очередь, тромбоз синуса может стать причиной геморрагического инфаркта мозга.
Синусы твёрдой мозговой оболочки участвуют в формировании дуральных артериовенозных мальформаций (ДАВМ), чаще наблюдаемых в области поперечного и сигмовидного синусов, реже — верхнего сагиттального, каменистого синусов или дна передней черепной ямки (этмоидальные ДАВМ). ДАВМ формируются на фоне дегенеративных изменений сосудистой стенки, вследствие травмы или тромбоза синусов. Из прямых ДАВМ (или посттравматических дуральных артерио-венозных фистул) наиболее распространено, в связи с особенностями анатомии, каротидно-кавернозное соустье.
Изображения
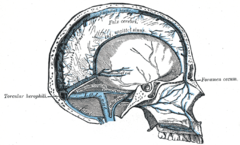
Твёрдая мозговая оболочка и её отростки
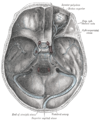
Синусы основания черепа
См. также
Ссылки
Полезное
Смотреть что такое «Поперечный синус» в других словарях:
поперечный синус — (sinus transversus, PNA, BNA, JNA) парный синус твердой мозговой оболочки, расположенный в одноименной борозде на внутренней поверхности затылочной кости; соединяет синусный сток с сигмовидным синусом … Большой медицинский словарь
синус поперечный — (sinus transversus) парный неспадающийся канал, образующийся за счет расщепления твердой мозговой оболочки головного мозга; лежит в одноименной борозде затылочной кости, продолжается латераль но и вниз, переходя в сигмовидный синус. Последний… … Словарь терминов и понятий по анатомии человека
Верхний сагиттальный синус — Вены головного мозга Срез черепа, демонстрирующий синусы твёрдой мозговой оболочки Синусы твёрдой мозговой оболочки (венозные синусы, синусы головного мозга) венозные коллекторы, расположенные между листками твёрдой мозговой оболочки. Получают… … Википедия
Кавернозный синус — Вены головного мозга Срез черепа, демонстрирующий синусы твёрдой мозговой оболочки Синусы твёрдой мозговой оболочки (венозные синусы, синусы головного мозга) венозные коллекторы, расположенные между листками твёрдой мозговой оболочки. Получают… … Википедия
Нижний сагиттальный синус — Вены головного мозга Срез черепа, демонстрирующий синусы твёрдой мозговой оболочки Синусы твёрдой мозговой оболочки (венозные синусы, синусы головного мозга) венозные коллекторы, расположенные между листками твёрдой мозговой оболочки. Получают… … Википедия
Прямой синус — Вены головного мозга Срез черепа, демонстрирующий синусы твёрдой мозговой оболочки Синусы твёрдой мозговой оболочки (венозные синусы, синусы головного мозга) венозные коллекторы, расположенные между листками твёрдой мозговой оболочки. Получают… … Википедия
Пещеристый синус — Расположение пещеристого синуса (вид сбоку, синус располагается в середине, подписан как sin. cavern … Википедия
Мозговы́е оболо́чки — (meninges) соединительнотканные структуры, покрывающие головной и спинной мозг. Различают твердую оболочку (dura mater, pachymeninx), паутинную (arachnoidea) и сосудистую, или мягкую (vasculosa, pia mater). Паутинную и мягкую оболочки объединяют… … Медицинская энциклопедия
Оболочки головного мозга — … Атлас анатомии человека
Синусы твёрдой мозговой оболочки — У этого термина существуют и другие значения, см. Синус (значения). Вены головного мозга … Википедия
Нарушение венозного оттока головного мозга
Общие сведения о нарушении венозного оттока головного мозга
Мозговое кровообращение происходит при активном участии сосудов головного и спинного мозга. При нарушениях в венозном оттоке крови можно утверждать, что поражены глубокие вены мозга. Это патологический процесс и динамика его развитиея будет зависить от индивидуальных особенностей.
Основными факторами при нарушении венозного оттока головного мозга являестя легочная недостаточность, опухоли головного мозга, сердечная недостаточность, тромбозы вен и синусов мозга, сдавление вен при краниостенозе и водянке мозга, асфиксия новорожденных, черепно-мозговые травмы.
Симптоматика нарушения венозного оттока головного мозга
При заболевании изменения нормального оттока крови из мозга провоцируют венозный застой. При этом, симптомы у пациента обычно следующие:
Также возможно повышение температуры, отек лица и гипертермия тела. Больные могут находиться в коматозном состоянии при тяжелых поражениях мозга. Начальные проявления заболевания характеризуются шумом в голове, головокружением и слабостью. Снижается работоспособность, переодически возникают сильные головные боли.
Тромбоз поверхностных вен мозга
Тромбоз глубоких вен мозга и большой мозговой вены
Клиническая картина отличается особой тяжестью. Пациенты находятся в коматозном состоянии, признаки дисфункции стволовых и подкорковых структур. Врачу следует наблюдать за развитием мозговых симптомов на фоне тромбофлебита конечностей или воспалительных очагов в организме (послеродовый период, инфекционные заболевания).
Тромбоз венозных синусов
Заболевание характеризуется резкими головными болями, отеками подкожной клетчатки лица, а также волосистой части головы. Также у больного наблюдается повышение температуры, изменения сознания (вплоть до впадания в кому). Цереброспинальная жидкость прозрачная.
Тромбоз сигмовидного поперечного синуса
Эта разновидность заболевания встречается чаще всего. Может являтся осложнением гнойного отита. Симптомы: отеки мягких тканей, боль при жевании и поворотах головы.
Тромбоз кавернозного синуса
Тромбоз верхнего продольного синуса
Болезнь развивается в зависимости от сопутствующих факторов. При тромбозе верхнего продольного синуса наблюдается переполнение и извитость вен век, висков, лба, темени с отеком этой области. Также характерны следующие симптомы:
Инфекционные тромбозы мозговых вен и синусов могут осложняться гнойным менингитом, энцефалитом (воспаление головного мозга) и абсцессом мозга (очаговое скопление гноя в веществе головного мозга).
Лечение нарушения венозного оттока головного мозга
Эффективным лечением нарушений венозного оттока головного мозга занимаются врачи-неврологи, а также инфекционисты. Для лечения нарушений венозного оттока используют препарат «Детралекс». Он специально предназначен для улучшения оттока крови. Также в некоторых случаях полезен масаж шеи. Однако проходить курс массажа нужно только по рекомендации лечащего врача.
Сегодня существуют специальные препараты, которые помагают устранить нарушения венозного оттока. Эти препараты называются венотоники. Также венотоники можно употреблять в качестве профилактики заболевания. Среди самых популярных растительных препаратов:
Лечебная физкультура для усиления кровотока
Иногда достаточно проработать шею, чтобы облегчить симптомы заболевания.
Упражнение «длинная шея» для усиления венозного оттока головного мозга
Для выполнения этого упражнения необходимо расслабиться. Опустите голову на грудную клетку и на вдохе поднимите голову вверх. При это смотрите вверх. Представьте, что вас тянет вверх невидимой нитью. Опустите голову, сделав выдох. Повторяйте упражнение 6-7 раз.
Упражнение для расслабления головы
Сядьте на стул и обопритесь руками на спинку. Голову откиньте назад, полностью расслабив тело. Дышите глубоко и медленно. Выполняйте упражнение в два-три захода.
Упражнение «рисуем восьмерку» для усиления венозного оттока головного мозга
Расслабтесь и при помощи макушки головы рисуйте в воздухе воображаемую восьмерку. Дышите свободно. Повторяйте упражнение 5-6 раз.
Также улучшить состояние пациента могут занятия йогой и бег. Важно знать, что вредные привычки (курение, алкоголь, жирная еда) способны провоцировать и усугублять развитие болезни. Пересмотрие Ваш образ жизни и попытайтесь искоренить вредные
Доминантный правый поперечный венозный синус
Наблюдение 1
Наблюдение 2
Больной Д. поступил в отделение нейрохирургии детского возраста ФГУ РНХИ в 2012 г. с жалобами на наличие патологического образования в области большого родничка, возвышающегося над кожными покровами, синюшного цвета. Анамнез болезни: с рождения в области большого родничка выявлено патологическое образование с синюшным оттенком, венозной сетью. Сразу после рождения отмечалось кровотечение из образования, которое на фоне проводимых мероприятий было остановлено. Увеличение образования, со слов матери, с 2-месячного возраста. В горизонтальном положении ребенка, а также при плаче объемное образование увеличивалось в размере. Местно: в проекции большого родничка объемное образование, синюшного цвета, размером 5×7×4 см (рис. 2, г).
Обсуждение
По мнению C. Marras и соавт. [28], первое упоминание о SP зафиксировано в 1760 г. и связано с именем Percivall Pott, который впервые дал описание сформировавшегося мягкотканого образования над местом перелома костей черепа. В 1845 г. А. Hecker [9] представил данную патологию под названием «varix spurius circumscriptus venae diploicae frontalis». В 1850 г. G. Stromeyer [45] впервые использовал термин Sinus pericranii для обозначения «резервуара, наполненного кровью, расположенного на костях черепа, который через диплоэтические вены связан с синусами твердой мозговой оболочки». Встречаются различные термины для обозначения этого патологического состояния: простое варикозное расширение (varix simplex), гроздевидное варикозное расширение (varix racemosus), варикозный герниоз (varix herniosis), варикозная аневризма (cirsoid aneurysm), венозная ангиома (venous angioma), варикозно-расширенная вена (varix cirsoideus), остеососудистый свищ (fistule osteovasculaire), венозная опухоль костей черепа, варикоз вен черепа [39].
T. Newton, D. Potts [34] определили SP как венозную мальформацию и описали данную патологию как сообщение между интра- и экстракраниальной венозными системами при помощи тонкостенного извитого сосудистого канала.
SP, однако, является не просто дополнительным чрескостным венозным каналом, соединяющим экстра- и интракраниальные венозные системы. Такая «эмиссарная вена» соединяет интракраниальный синус и сеть варикозно-расширенных венозных тонкостенных сосудов, расположенных на наружной поверхности черепа, в которой происходит депонирование крови с разнонаправленным кровотоком. С учетом этого, C. Gandolfo и соавт. [16] разделили SP по ангиоархитектонике на две основные группы: 1) доминантный тип, при котором основное дренирование паренхимы мозга осуществляется через вены, дренирующие в SP; 2) дополнительный тип, при котором только часть венозного оттока происходит в экстрадиплоэтические сосуды.
Этиология SP до конца не изучена. Чаще SP может быть врожденной патологией, но травма также может быть вероятным причинным фактором развития SP [12, 21, 47 и др.].
SP разделяют на врожденный, приобретенный и посттравматический [35].
SP врожденного генеза чаще локализуется на «средней линии» в лобной области, однако описаны случаи локализации врожденного SP в теменной области, височно-затылочной области [26].

Перикраниальный синус представляет собой экстрадуральную DVA [31]. Это объясняет частое сочетание SP и DVA, не только при врожденном, но и при травматическом и спонтанном вариантах [4, 9, 13, 22 и др.]. Также описаны случаи сочетания SP c артериовенозными мальформациями [4] и каверномами [6, 30].
Согласно K. Sakai и соавт. [40], формирование SP происходит в позднем эмбриональном периоде вследствие явлений венозной гипертензии, на фоне окклюзии венозного оттока. В связи с частым сочетанием SP c краниостенозом C. Gandolfo и соавт. [16] считают, что формирование врожденного SP на фоне краниостеноза происходит вследствие образования дополнительных путей оттока (на фоне внутричерепной гипертензии и нарушения венозного оттока), что также соответствует данным N. Mitsukawa и соавт. [29].
Общепринятым критерием для установления первопричины данной патологии является тип ткани, выстилающей мешок. Эндотелиальная выстилка характерна для врожденного SP, тогда как приобретенное образование имеет выстилку из соединительной ткани [39]. C. Wen и соавт. [50] считают, основываясь на работе E. Hahn [19], что гистологически спонтанный и травматический типы не различаются. Данные гистологического заключения в случае больного Д. (наблюдение 2, см. выше) (рис. 4) указывают на наличие кавернозной ангиомы (каверномы).
SP может встречаться в любом возрасте [7, 22, 38]. Однако, по данным M. Sheu и соавт. [43], манифестация заболевания (прогредиентное увеличение образования, неврологический дефицит) при врожденных случаях наблюдается в основном у детей младшего возраста; почти половина описанных случаев относится к пациентам до 20 лет, а в общем числе описанных случаев пациенты до 40 лет и младше составляют 88%.
Некоторые авторы считают, что у мальчиков SP встречается чаще, но T. Ohta и соавт. [35] полагают, что большая частота встречаемости SP у мальчиков обусловлена высокой частотой посттравматических случаев.
SP не имеет характерной клинической картины, чаще всего поводом для обращения к врачу является наличие косметического дефекта. Однако клиническая картина заболевания может быть представлена головной болью, головокружением, тошнотой, болью и ощущением давления в зоне локализации SP. Крайне редко больные предъявляют жалобы на брадикардию, атаксию, снижение слуха, рвоту [43]. Отмечается постепенное увеличение размеров образования [9], хотя в литературе [37] имеются сообщения о спонтанном тромбировании. У больного М. (наблюдение 1, см. выше) единственной жалобой явилось наличие косметического дефекта. У больного Д. (наблюдение 2, см. выше), кроме косметического дефекта, отмечалось ранее не описанное в литературе осложнение в виде кровотечения из SP, сразу после родов, вероятно, обусловленное травматизацией SP вследствие прохождения плода через родовые пути.
Необходимо дифференцировать SP и другие подкожные образования черепа, включая подапоневротическую гематому, атретическое менингоцеле, растущий перелом, дермоидную кисту, опухоль костей черепа. Характерной особенностью данного образования является зависимость размеров от положения тела. В горизонтальном положении больного образование имеет наибольшие размеры, а в вертикальном положении уменьшается. Однако в вертикальном положении и при компрессии яремных вен с двух сторон или проведении теста Вальсальвы размеры образования увеличиваются [7, 21].
Но не для всех вариантов SP данная особенность является обязательной, что в своей классификации отразил J. Volkmann (1950). У пациента М. (наблюдение 1) размеры образования не зависели от положения тела. У пациента Д. (наблюдение 2) отмечалось значительное увеличение размеров образования в горизонтальном положении.
При нейросонографическом исследовании SP представляет собой анэхогенную структуру [24]. Допплерографическое исследование позволяет провести дифференциальный диагноз между сосудистой и несосудистой патологией, верифицировать венозный характер кровотока, направление тока крови в эмиссарных венах, двунаправленный турбулентный кровоток в самом патологическом образовании [52], что было выявлено в 2 наших наблюдениях.
При КТ без контрастного усиления SP имеет большую плотность по отношению к окружающим структурам мозга. Также КТ позволяет выявить наличие дефекта костей свода черепа. При КТ с внутривенным контрастированием SP имеет такую же плотность, как другие венозные структуры, исключением являются случаи тромбированного SP [26].
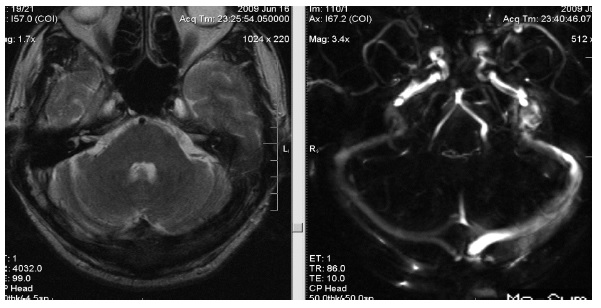
МРТ дает информацию о содержимом синуса на основании характеристик сигнала и взаимосвязи патологического образования и подлежащего синуса [39]. Данные МРТ больного Д. указывали на наличие патологического образования, характеризующегося сигналом со смешанной интенсивностью. Это было обусловлено турбулентным кровотоком. Для определения взаимосвязи образования и синусов твердой мозговой оболочки используют магниторезонансную или компьютерную венографию [7].
В случае пациента Д. проведения МРТ и спиральной компьютерной ангиографии головного мозга явилось достаточным для установления диагноза. В случае пациента М. данные спиральной КТ неубедительно указывали на отсутствие артериовенозного шунтирования.
Хирургическое лечение
В 1771 г. Percivall Pott [13] успешно произвел трефинацию и тампонаду SP. До 1902 г. сообщений в литературе о проведении успешных операций не было. Несмотря на наличие сообщений, указывающих на возможность спонтанного тромбирования [20, 37], активная хирургическая тактика при данной патологии является обоснованной [2, 12, 44, 47, 50 и др.].
Наличие доминантного типа, по классификации C. Gandolfo и соавт. [16], является противопоказанием к любому виду хирургии, так как это может привести к осложнениям, таким как выраженный венозный застой и/или инфаркт мозга. При дополнительном паттерне тактика хирургического лечения зависит от особенностей дренирования паренхимы мозга. По данным зарубежной литературы [12], до 30% описанных случаев относились к доминантному типу и не были оперированы.
Микрохирургические методы можно разделить на два вида: 1) радикальная операция, которая заключается в широкой краниотомии, окклюзии венозных коллекторов, соединяющих синус и экстракраниальное сосудистое образование, краниопластике [28,49]; 2) удаление экстракраниального компонента, окклюзия венозных коллекторов, соединяющих синус и экстракраниальное сосудистое образование, без проведения краниотомии [29].
К возможным осложнениям данного вида хирургического вмешательства относятся воздушная эмболия и кровотечение [2, 5, 14, 15, 25].
Описанные нами наблюдения (больной М. и больной Д.) по классификации C. Gandolfo и соавт. (2007) относились к дополнительному типу.
Особенностью у больного М. являлась гипоплазия левой половины поперечного синуса. По данным церебральной ангиографии, не отмечалось стенозов правой и левой половины поперечного синуса, не был выявлен стеноз яремных вен. В случае больного Д. данные МРТ и спиральной КТ-ангиографии, транскраниальной допплерографии не выявляли значимого дренирования паренхимы мозга с участием SP. В обоих случаях была выбрана хирургическая тактика. С учетом малого возраста, высокого риска развития тяжелой постгеморрагической анемии вследствие кровопотери хирургическое лечение у больного Д. было разделено на два этапа.
Имеются малочисленные сообщения [10, 23, 36] о применении при лечении SP эндовазальных методов c различными исходами.
Заключение
В тех случаях, когда основное дренирование мозга осуществляется через вены, дренирующие в SP, хирургическое лечение не показано. В случаях, когда только часть венозного оттока происходит в экстрадиплоэтические сосуды, показано хирургическое лечение. Методом выбора хирургического лечения является удаление экстракраниального компонента, окклюзия венозных коллекторов, соединяющих синус и экстракраниальное сосудистое образование, без проведения краниотомии. Однако, если рассматривать перикраниальный синус как экстракраниальную DVA, то выбор тактики в пользу хирургии должен основываться на балансе между предполагаемым эффектом и вероятностью послеоперационных осложнений, таких как венозный застой и/или инфаркт мозга.
Комментарий
В любом случае работа освещает сравнительно редкую и малоизвестную проблему и вызывает интерес.
С. Яковлев, Л. Шишкина, А. Меликян (Москва)
Нарушение мозгового венозного кровотока у больных с гипертонической дисциркуляторной энцефалопатией
Изучить клинико-нейровизуализационные особенности венозной дисциркуляции у больных с гипертонической дисциркуляторной энцефалопатией (ГДЭ).
Материалы и методы
Были обследованы 132 пациента с ГДЭ, которых распределили на группы в зависимости от стадии ГДЭ, а также с учетом наличия конституциональной венозной недостаточности (КВН). Всем пациентам проведено полное клинико-неврологическое исследование, МРТ головного мозга и МР-венография.
У пациентов с КВН гипоплазия поперечных и сигмовидных синусов (57,5%), расширение поверхностных вен мозга (68,5 %) и вены Галена (65,6%), хронические тромбозы венозных синусов (24,7%) визуализировались чаще, чем у больных без КВН на всех стадиях ГДЭ. Установлена взаимосвязь выявленных изменений с клиническими проявлениями церебральной венозной дисциркуляции.
Применение методов нейровизуализации в сочетании с клинико-неврологическим исследованием позволяет оптимизировать этиопатогенетическую терапию, а также программу профилактических и реабилитационных мероприятий, которые должны проводиться с учетом выраженности венозных расстройств.
Хронические цереброваскулярные заболевания представляют собой важную медико-социальную проблему 2. Одной из наиболее распространенных форм хронических цереброваскулярных заболеваний является ГДЭ [3,4], развитие которой во многом зависит от нарушения венозного компонента церебральной гемодинамики, что может быть обусловлено наличием как врожденных причин в виде конституциональной венозной недостаточности (КВН), так и, в соответствии с концепцией «энцефалопатии пульсовой волны», формироваться вторично при гипертоническом поражении сосудов 6. В настоящее время выделен патогенетический подтип ГДЭ, сопровождающейся КВН, описан его клинико-неврологический симптомокомплекс, с помощью ультразвуковых методов изучено состояние гемодинамики на всех структурно-функциональных уровнях сосудистой системы мозга [7,8,10]. Тем не менее, в полной мере оценить структурное состояние венозного компонента сосудистой системы мозга ультразвуковыми методами диагностики не представляется возможным [11]. Внедрение в клиническую практику магнитно-резонансной томографии (МРТ) открыло новые перспективы в изучении венозной системы головного мозга [12].
Целью исследования было изучить клинико-нейровизуализационные особенности венозной дисциркуляции у больных ГДЭ.
Материал и методы
В исследование включали пациентов с артериальной гипертонией, сопровождавшейся ГДЭ, которые были обследованы в неврологическом отделении для больных с нарушением мозгового кровообращения ГУЗ «Центральная клиническая медико-санитарная часть им. заслуженного врача России В.А. Егорова» г. Ульяновска. Клиническими критериями КВН были «венозные» жалобы, обусловленные венозной церебральной дисциркуляцией, такие как пастозность лица и век в утренние часы, симптом «тугого воротника», симптомы «песка в глазах» и «высокой подушки», семейный «венозный» анамнез, наличие типичных проявлений венозной патологии (варикозное расширение и тромбоз вен нижних конечностей, геморрой, варикоцеле, варикозное расширение вен пищевода) и неврологических симптомов, в развитии которых особую роль играет венозная дисциркуляция. Критерием исключения служили соматические заболевания, которые могут быть причиной вторичных нарушений венозного кровообращения [10].
МРТ проводили на аппарате Siemens Magnetom Symphony с силой поля 1,5 Тесла. Исследование параметров церебрального венозного оттока осуществляли с использованием времяпролетной МР-венографии (Time of flight – TOF) в двухмерном (2D) изображении.
Статистический анализ полученных результатов проводился с использованием пакета прикладных программ Statistica 8.0 и Excel. Для проверки гипотезы о различии выборок групп больных использовали U-тест Манна– Уитни, а для определения связи между количественными показателями – непараметрический корреляционный анализ Спирмена. Результаты представлены в виде медианы, 25% и 75% квартилей – Мe [25%; 75%]. Различия считали достоверными при р
Результаты
Обследовали 132 пациентов с ГДЭ, в том числе 47 мужчин и 85 женщин в возрасте от 41 до 76 лет (в среднем 60±10,7 лет). Все пациенты страдали гипертонической болезнью в течение более 5 лет (в среднем 11,2±7,2 лет). В соответствии с классификацией Научного центра неврологии (1985 г.) у 37 (28,1%) пациентов диагностирована ГДЭ I стадии, у 51 (38,6 %) – II стадии, у 44 (33,3 %) – III стадии. Контрольную группу составили 30 человек с нормальным АД, в том числе 17 женщин и 13 мужчин в возрасте в среднем 59,4±10,3 лет.
| КВН (n=73) | КВН (n=59) | |
|---|---|---|
| Примечание: *p | ||
| Женщины, n (%) | 48 (65,8) | 37 (62,7) |
| Средний возраст, лет | 56,4±10,2 | 60,5±11,8 |
| Стадия ГДЭ, n (%) | ||
| I | 21 (28,8) | 16 (27,1) |
| II | 29 (39,7) | 22 (37,3) |
| III | 23 (31,5) | 21 (35,6) |
| Симптомы, n (%) | ||
| Симптом «тугого воротника» | 49 (67,2)* | 24 (40,7) |
| Симптом «высокой подушки» | 50 (68,5)* | 23 (38,9) |
| Симптом «песка в глазах» | 55 (75,3)* | 22 (37,3) |
| Пастозность лица и век в утренние часы | 60 (82,2)* | 22 (37,3) |
Признаки КВН выявили у 73 (55,3%) пациентов. Группы пациентов с КВН и без КВН не отличались по возрасту, полу и стадиям ГДЭ (табл. 1). «Венозные» жалобы у больных с КВН встречались достоверно чаще, чем в группе сравнения. Снижение корнеальных рефлексов, болезненность точек выхода и гипестезия в зоне иннервации первой ветви тройничного нерва и диссоциация коленных и ахилловых рефлексов, в развитии которых играет роль венозная дисциркуляция, у пациентов с КВН определялись уже на I стадии ГДЭ и наблюдались чаще, чем у пациентов без КВН, на всех стадиях ГДЭ (р ТАБЛИЦА 2. Неврологические симптомы церебральной венозной дисциркуляции у больных с КВН и без КВН, n(%)
иннервации первой ветви тройничного нерва
Результаты визуализации анатомического строения интракраниальной венозной системы по данным МРвенографии представлены в (табл. 3). Симметричное строение поперечных и сигмовидных синусов у пациентов с КВН на всех стадиях ГДЭ определялось значительно реже, чем у пациентов без КВН (р ТАБЛИЦА 3. Анатомические варианты строения поперечных и сигмовидных синусов у больных с КВН и без КВН, n (%)
У больных с КВН диаметры поверхностных вен и вены Галена превышали таковые у пациентов без КВН и пациентов контрольной группы и нарастали по мере прогрессирования ГДЭ. У больных ГДЭ III стадии они были значительно больше, чем у пациентов с ГДЭ I стадии (p ТАБЛИЦА 4. Размеры венозных структур (мм) по данным МР-венографии в группах больных с КВН и без КВН.
В соответствии с триадой R. Virchow (1856) стаз и иммобилизация крови в венозном русле играют важную роль в развитии венозного тромбоза [14]. В нашем исследовании при МР-венографии определялись тромбозы поперечных и сигмовидных синусов, сигнальная характеристика которых соответствовала диагностическим нейровизуализационным критериям тромбоза в хронической стадии [15,16]. У больных с тромбозом отсутствовали указания в анамнезе на клинические состояния, соответствующие классическому описанию церебрального венозного тромбоза, который часто развивается подостро (в 50-80% случаев в течение от нескольких дней до одного месяца) [17,18] и характеризуется полиморфизмом и неспецифичностью клинической картины [19], особенно у пациентов с КВН. На фоне уже имеющихся венозных жалоб и относительной адаптации к клиническим проявлениям КВН не всегда заметно нарастание симптомов центрального венозного тромбоза, что обусловливает позднее обращение больных за медицинской помощью. Тромбозы поперечных и сигмовидных синусов у пациентов с КВН встречались чаще (24,7%), чем у больных без КВН (8,5%, p 0,05). В контрольной группе случаев тромбоза поперечных и сигмовидных синусов не выявлено.
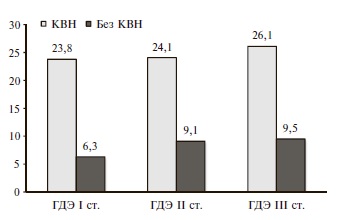
В целом при МР-венографии у 65,8% пациентов с КВН визуализировали расширение поверхностных вен головного мозга, у 57,5% – гипоплазию венозных синусов, у 64,4% – расширение вены Галена, у 24,7% – тромбозы венозных синусов (рис. 2).
| Расширение поверхностных вен | Расширение вены Галена | Гипоплазия венозных синусов | Тромбозы венозных синусов | |||||
|---|---|---|---|---|---|---|---|---|
| r | p | r | p | r | p | r | p | |
| Симптом «тугого воротника» | 0,46 | 0,03 | 0,52 | 0,02 | 0,54 | 0,02 | 0,47 | 0,03 |
| Симптом «песка в глазах» | 0,56 | 0,01 | 0,46 | 0,03 | 0,47 | 0,03 | 0,46 | 0,04 |
| Пастозность лица и век в утренние часы | -0,52 | 0,02 | -0,58 | 0,01 | -0,46 | 0,03 | -0,54 | 0,01 |
| Симптом «высокой подушки» | -0,47 | 0,02 | -0,44 | 0,04 | -0,42 | 0,04 | -0,48 | 0,03 |
| Снижение корнеальных рефлексов | 0,47 | 0,01 | 0,58 | 0,01 | 0,84 | 0,001 | 0,50 | 0,02 |
| Болезненность точек выхода и гипестезия в зоне иннервации первой ветви тройничного нерва | 0,42 | 0,04 | 0,48 | 0,02 | 0,80 | 0,01 | 0,46 | 0,04 |
| Диссоциация коленных и ахилловых рефлексов | 0,56 | 0,02 | 0,44 | 0,03 | 0,83 | 0,003 | 0,42 | 0,04 |
У больных с КВН наблюдалась корреляционная связь средней силы между расширением поверхностных вен и вены Галена, тромбозами венозных синусов и «венозными» жалобами и неврологическими симптомами церебральной венозной дисциркуляции, а также между гипоплазией венозных синусов и «венозными» жалобами (табл. 5). Обращало на себя внимание наличие высокой корреляции между гипоплазией венозных синусов и неврологическими симптомами церебральной венозной дисциркуляции.
Обсуждение
У больных ГДЭ с КВН в клинической картине заболевания существенное место занимают симптомы, свидетельствующие о венозной церебральной дисциркуляции и проявляющиеся уже на ранних стадиях ГДЭ. У пациентов без КВН нарастание клинических проявлений венозной дисциркуляции зависит от прогрессирования ГДЭ. МР-венография является важнейшим неинвазивным методом диагностики КВН у пациентов с ГДЭ. Нейровизуализационными коррелятами КВН у являются расширение поверхностных вен и вены Галена, гипоплазия и тромбозы венозных синусов в хронической стадии. При наблюдении больных ГДЭ, особенно при наличии КВН, необходим высокий уровень настороженности в отношении центрального венозного тромбоза вследствие неспецифичности, стертости и медленного нарастания симптоматики. Применение методов нейровизуализации в сочетании с клиниконеврологическим исследованием позволяет оптимизировать этиопатогенетическую терапию, а также программу профилактических и реабилитационных мероприятий, которые должны проводиться с учетом выраженности венозных расстройств у больного. Медикаментозная терапия должна быть направлена на облегчение венозного оттока из полости черепа.
Винпоцетин (Кавинтон®, «Гедеон Рихтер», Венгрия), производное алкалоида винкамина, содержащегося в растении барвинок малый, является препаратом выбора в лечении больных с церебральными венозными расстройствами, что обусловлено его воздействием на целый ряд патофизиологических процессов, вызывающих поражение эндотелия сосудов и нарушение церебральной, в том числе, венозной гемодинамики. Винпоцетин модулирует активность митохондриальной поры и предотвращает нарушение метаболизма в этих органеллах и гиперпродукцию активных форм кислорода (АФК) [20]. В эксперименте показано, что увеличение содержания АФК в сосудах приводит к стимуляции вазоконстрикции и ремоделирования с повышением системного сосудистого сопротивления, а увеличение концентрации АФК в головном мозге вызывает стимуляцию нейронов с увеличением симпатической активации и продукции провоспалительных цитокинов, воздействующих на эндотелий сосудов [21]. Кроме того, винпоцетин ингибирует фосфодиэстеразу и увеличивает уровень цГМФ в сосудистом эндотелии, что способствует вазодилатации [20], а также уменьшает выделение воспалительных цитокинов и хемокинов из эндотелиальных клеток, гладкомышечных клеток сосудов, макрофагов и микроглии путем ингибирования сигнального пути NF-κB [21]. Таким образом, препарат оказывает положительное действие на мышечную стенку и эндотелий сосудов и улучшает состояние церебральной гемодинамики в целом.
Благоприятное влияние винпоцетина на артериальные сосуды, вероятно, реализуется посредством воздействия как на мышечную стенку, так и на эндотелий. Предотвращая нарастание гипертонического или атеросклеротического ремоделирования, уменьшая периферическое сосудистое сопротивление, нормализуя пульсацию и улучшая вазоактивные свойства артерий, винпоцетин способствует улучшению и венозной гемодинамики, так как отток в венах осуществляется пассивно, в том числе за счет проталкивания крови. В венозных сосудах, с их невыраженной мышечной стенкой, вазоактивный эффект винпоцетина, вероятнее всего, преимущественно определяется воздействием на эндотелий, который, в отличие от артериального, обладает большей восприимчивостью к провоспалительным цитокинам, фактору некроза опухоли, липополисахаридам и запрограммирован на более высокий уровень адгезионного ответа [22,23]. В связи с этим противовоспалительный и антиоксидантный механизмы действия винпоцетина имеют крайне важное значение в отношении именно венозного эндотелия.
Важнейшим эффектом винпоцетина, способствующим увеличению микроциркуляции и перфузии ткани мозга, является улучшение реологических свойств крови путем снижения ее вязкости. В свою очередь, вязкость крови во многом зависит от агрегации и деформируемости эритроцитов, составляющих 99% всех ее клеток. Исследования показали, что винпоцетин, увеличивая уровень цГМФ в мембранах эритроцитов, оказывает положительное влияние на их деформируемость у больных с хроническими цереброваскулярными заболеваниями [20] и инсультом [24]. Помимо защиты нейронов в условиях ишемии и гипоксии за счет улучшения перфузии данный механизм уменьшает вероятность развития церебральных венозных тромбозов вследствие улучшения текучести крови и уменьшения выраженности застойных явлений, прежде всего, в венозных структурах мозга, что имеет важное значение для больных ГДЭ [25]. Уменьшение вероятности развития венозных тромбозов при лечении винпоцетином происходит также за счет противовоспалительного действия препарата на венозный эндотелий. Наряду с этим, винпоцетин предотвращает развитие и артериальных тромбозов путем снижения агрегации тромбоцитов, увеличения простациклин-тромбоксанового соотношения, что приводит к увеличению защитного атромбогенного потенциала сосудистой стенки, в частности, его антиагрегационного звена [26].
Таким образом, терапия винпоцетином у больных с хроническими цереброваскулярными заболевания оказывает системное действие и улучшает состояние всей сосудистой системы мозга, в том числе, ее венозного компонента. Препарат оказывает выраженное проти вовоспалительное действие на венозный эндотелий, улучшает его барьерную функцию, способствует сохранению структурной целостности венозных сосудов, улучшает их функциональное состояние. Следствием этого является улучшение реактивности вен и оттока венозной крови от мозга и, как следствие, уменьшение застойных явлений в сосудах мозга и выраженности хронической гипоксии у данной группы больных. Наряду с этим, важнейшими механизмами действия препарата при восстановлении неврологического дефицита, уже сформировавшегося в условиях хронического нарушения мозгового кровообращения, являются активация периферических бензодиазепиновых рецепторов [20] и влияние на нейропластические процессы путем стимуляции экспрессии BDNF [27].
Клиническая эффективность Кавинтона® установлена в двойных слепых, плацебо-контролируемых, рандомизированных исследованиях у больных с различными формами цереброваскулярной патологии: уменьшение частоты жалоб на головную боль, головокружение, шум в ушах, выраженности когнитивных, эмоциональных и астенических расстройств, статических нарушений, снижение риска падений, регресс речевых, двигательных, мнестических расстройств, улучшения качества жизни [24,27-33]. Кроме того, последние исследования [34] позволили выявить уникальный механизм действия винпоцетина, аналогичный феномену ишемического прекондиционирования (феномен прерывистой ишемии или метаболической адаптации) и позволяющий рассматривать препарат как средство профилактики развития церебральных катастроф у больных с хроническими нарушениями как артериальной, так и венозной гемодинамики различной степени выраженности.
Следует отметить хорошую переносимость и безопасность терапии винпоцетином у больных различных возрастных групп, а также у пациентов с сопутствующими заболеваниями. Препарат хорошо сочетается с другими лекарственными средствами, в том числе его можно комбинировать с другими венотоническими препаратами и антиоксидантами.
Появление на фармацевтическом рынке инновационной лекарственной формы винпоцетина (Кавин тон® Комфорте) в виде диспергируемых (растворимых в воде или слюне) таблеток способствовало повышению приверженности к терапии и ее эффективности у ряда пациентов. Одним из наиболее важных преимуществ данной формы является высокая биодоступность, обусловленная тем, что микросферы, на которые распадается таблетка во время растворения в полости рта, защищают находящееся в них действующее вещество при прохождении по желудочно-кишечному тракту до всасывания в тонком кишечнике. Также растворение Кавинтон® Комфорте в полости рта исключает травматизацию слизистой оболочки желудка и обеспечивает оптимальную скорость всасывания препарата.
Кавинтон® Комфорте является предпочтительной формой для больных с нарушениями глотания, возникшими в результате хронического нарушения мозгового кровообращения, а также больных с острым инсультом или инсультом в анамнезе, у которых прием обычных таблеток и желатиновых капсул сопряжен с определенными трудностями. Тошнота, когнитивные и психоэмоциональные расстройства, часто возникающие при данных состояниях, также являются причиной выбора новой формы. С учетом отсутствия у Кавинтона® Комфорте отрицательного воздействия на слизистую оболочку желудка он является препаратом выбора для больных с сопутствующими заболеваниями желудочнокишечного тракта. Кроме того, Кавинтон® Комфорте не требуется запивать водой, что делает его применение удобным и комфортным для работающих, занятых пациентов, а также для путешественников.
Немедикаментозные методы лечения больных с хроническими цереброваскулярными заболеваниями должны включать соблюдение растительной диеты, дозированную дыхательную гимнастику, отводящий массаж головы и шеи, физиотерапевтические процедуры (гальванический воротник, СМТ на шейно-воротниковую зону, теплые ножные ванны). Для пациентов с хроническими цереброваскулярными заболеваниями, обязательным компонентом которых являются венозные расстройства различной степени выраженности, необходима разработка индивидуальной программы реабилитации. В соответствии с консенсусом International Union of Phlebology, основные составляющие реабилитационной программы больных с хроническими венозными заболеваниями включают лечебную физкультуру, адаптированную физическую нагрузку, психологическую и социальную поддержку. Особое внимание уделено необходимости системного подхода к пациентам с венозными расстройствами, индивидуальной разработке алгоритма реабилитационных мероприятий для каждой группы пациентов с учетом выраженности венозной недостаточности, возраста, двигательной активности, сопутствующих заболеваний, состояния психического здоровья. Отмечена необходимость проведения рандомизированных контролированных исследований для оценки эффективности многочисленных реабилитационных протоколов.