иммунокомпетентность что это такое
Иммунокомпетентность что это такое
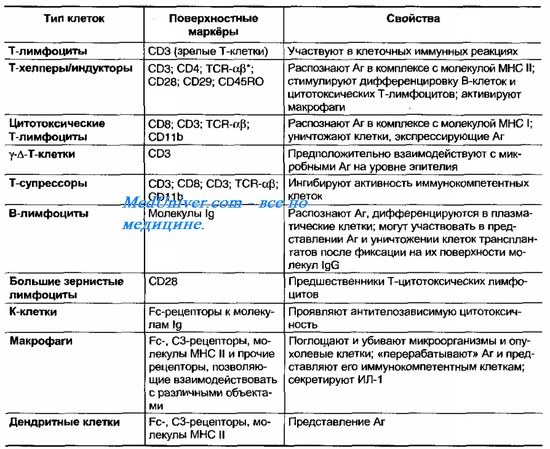
Иммунокомпетентные клетки (лимфоциты, макрофаги и дендритные клетки) по функциям подразделяют на эффекторные и регуляторные (табл. 10-6). Взаимодействие иммунокомпетентных клеток с другими регулируют цитокины (табл. 10-7), известные также как медиаторы иммунного ответа.
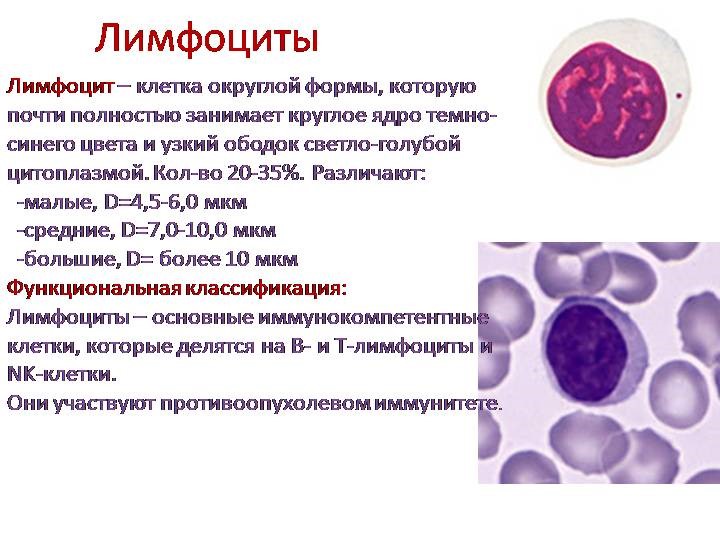
Лимфоциты выполняют основную функцию иммунной системы — высокоспецифичное распознавание чужеродных и измененных собственных Аг. В организме лимфоциты постоянно рециркулируют между зонами скопления лимфоидной ткани.
Таблица 10-6. Популяции иммунокомпетентных клеток
Распределение лимфоцитов в лимфоидных органах и их миграция по кровеносному и лимфатическому руслам упорядочены и отражают функции конкретных клеток. При изучении в световом микроскопе лимфоциты имеют одинаковую морфологию, но их функции, поверхностно-клеточные маркёры, индивидуальное (клональное) развитие и судьба различны.
Все лимфоциты происходят из единой стволовой клетки костного мозга, но популяции лимфоцитов и других клеток крови развиваются под влиянием различных дифференцирующих факторов. По наличию специфических поверхностных маркёров лимфоциты разделяют на функционально различные популяции и субпопуляции.
У млекопитающих основные популяции: Т-лимфоциты, созревающие в вилочковой железе [лат. thymus]; В-лимфоциты, созревающие в аналоге сумки [лат. bursa] Фабрициуса у птиц (у человека — костный мозг или лимфоидная ткань кишечника).
Иммунная система Часть 8 Анализы
Иммунная система Часть 8 Анализы
Помимо поражения вирусом иммунодефицита человека, вторичный иммунодефицит развивается после объемных оперативных вмешательств, обширных, тяжелых инфекций, на фоне терапии иммуноподавляющими или сильными противовоспалительными препаратами.
Исследования иммунитета помогают в оценке активности и стадии воспалительного, инфекционного и аллергического иммунного ответов, эффективности проводимой терапии. С этой целью они проводятся неоднократно.
Клинический анализ крови с лейкоцитарной формулой
Клинический анализ крови с лейкоцитарной формулой позволяет выявить множество заболеваний. Он отражает состояние гемопоэза – созревания и роста клеток крови в костном мозге. О состоянии иммунной системы говорят уровни белых клеток крови – лейкоцитов и лейкоцитарная формула. Наблюдение за лейкоцитарной формулой в динамике заболевания позволит выявить осложнения, распространение инфекции по организму, реакцию на лечение.
При бактериальных инфекциях можно увидеть повышение лейкоцитов и нейтрофилов с появлением их молодых форм в крови.
При вирусных инфекциях, наоборот, лейкоциты снижаются, а в лейкоцитарной формуле преобладают лимфоциты.
Преобладание тех или иных популяций в лейкоцитарной формуле помогает в диагностике причины воспаления. Например, при определенных инфекциях (например, инфекционный мононуклеоз) нарастают измененные моноциты, а при аллергических и паразитарных заболеваниях – эозинофилы.
Наличие совсем юных клеток (бластов) в крови признак чрезмерной активации костного мозга, а низкий уровень лейкоцитов и нейтрофилов без воспаления – его угнетения.
Лимфоциты, иммунофенотипирование
Выделяют разные популяции лимфоцитов, которые играют ключевую роль в направлении иммунного ответа – клеточный или гуморальный. Определение иммунного фенотипа лимфоцита возможно в специальном исследовании методом проточной цитофлюориметрии. Фенотип лимфоцитов зависит от особых рецепторов на их поверхности – кластеров дифференцировки CD. Наличие того или иного рецептора свидетельствует о принадлежности клетки к определенной популяции лимфоцитов.
Т-лимфоциты (CD3+) общие и их подтипы:
Т- клетки-киллеры (CD3+CD16+CD56+)
Естественные клетки-киллеры (CD3-CD16+CD56+)
Лимфоциты с маркером HLA-DR+
Иммунорегуляторный индекс (Т-хелперы/Т-цитотоксические)
Дополнительно исследуют другие CD маркеры лимфоцитов для определения их активности.
Циркулирующие иммунные комплексы и система комплемента
Антигены связываются специфическими антителами с образованием иммунных комплексов. Последние активируют комплемент, способствуют удалению чужеродных антигенов. Если их слишком много циркулирует в крови, они откладываются в тканях, например почек, кожи, легких. Высокое содержание циркулирующих иммунных комплексов (ЦИК) наблюдается при аутоиммунных, хронических воспалительных и инфекционных заболеваниях. С другой стороны, определение ЦИК в крови неспецифично, не отражает ни причину их нарастания, ни непосредственное влияние на органы.
Снижение уровней ЦИК на фоне лечения говорит о затихании воспалительного процесса и эффективности терапии.
Наиболее распространенными анализами на систему комплемента являются определение ключевых С3 и С4 компонентов. Показаниями для исследования – повторяющие инфекции, ревматические и аутоиммунные заболевания для выявления врожденных дефицитов комплемента, утяжеляющих течение этих болезней.
Исследуют уровни ЦИК, С3-компонент и С4-компонент комплемента.
Иммуноглобулины A, M, G, E
Общие иммуноглобулины – показатели гуморального иммунного ответа. Уровни IgM возрастают в острый период заболевания и при обострении хронической инфекции, IgG – в процессе выздоровления, IgA – в острый период заболевания, сохраняясь дольше IgM, отражают затяжное течение и поражение слизистых оболочек. Повышенные уровни IgE свидетельствуют об аллергическом воспалении.
Общие иммуноглобулины не объясняют причину инфекции, поэтому целесообразно смотреть специфические антитела к конкретным возбудителям. Основные показания для определения общих антител – это подозрение на врожденный иммунодефицит, связанный с гуморальным иммунитетом.
Интерфероновый статус и Интерлейкины
Исследования Интерфероновый статус, Интерлейкин-1бета, Интерлейкин-6, Интерлейкин-8, Интерлейкин-10, Фактор некроза опухоли-альфа и другие определяют уровни цитокинов – специфических маркеров иммунного ответа. Помогают в определении стадии заболевания, врожденных дефектов, онкологических заболеваний, активности воспалительного процесса и осложнений. Как правило, требуют динамического контроля для помощи в оценке клинической ситуации и эффективности лечения.
Фагоцитарная активность
Фагоцитарной активностью обладают нейтрофилы, моноциты-макрофаги и другие клетки. Фагоцитоз – это способность поглощать и переваривать антигены, вплоть до целых клеток. Он определяет возможности врожденного иммунитета и необходим для формирования приобретенного иммунитета. Оценка фагоцитарной активности клеток крови трудоемка и сложна. Используют такие тесты как оценка фагоцитоза бактерий с флюоресцентной меткой, тест по восстановлению нитросинего тетразолия.
Фагоцитарная активность повышается при бактериальных, аутоиммунных, аллергических заболеваниях.
Ее снижение наблюдается при врожденных дефектах фагоцитарной системы, хронических инфекциях.
Иммунограмма – это общее название всех исследований иммунного статуса. И в разных лабораториях включают разное сочетание анализов в зависимости от цели обследования. Для оценки клеточного иммунитета применяют исследование иммунофенотипов лимфоцитов. Для оценки гуморального иммунитета – общие иммуноглобулины, при необходимости дополняя их ЦИК, комплементом и белками острой фазы. Для оценки врожденного иммунитета больше подходят определения цитокинов в крови, фагоцитарная активность.
Иммунитет
Иммунитет – защитная система организма, поддерживающая в нем генетическое постоянство. Она оберегает его от проникновения вирусов, бактерий, грибков, простейших, ядов и аллергенов из окружающей среды. Также иммунитет человека защищает организм от вредоносного воздействия изнутри — уничтожает мутировавшие вследствие заболеваний и других патологических процессов клетки, устраняет продукты распада. Другими словами, он поддерживает здоровье человека.Чтобы иммунная система качественно работала, необходимо регулярно поддерживать ее состояние, устранять неполадки. Укрепление иммунитета – вопрос, актуальный и для здорового человека. В нашей статье вы узнаете, как эффективно провести профилактику, какие действия следует осуществить в первую очередь, а от чего стоит воздержаться.
Что такое иммунитет
Иммунная система отвечает за генетический состав организма. Она выполняет как защитную, так и «ремонтную» функцию – устраняет неполадки, образовавшиеся внутри.
В нашем организме происходит множество процессов, и для них нужны определенные условия, которые поддерживаются за счет температуры, давления, уровня кислорода и т.д. Изменения этих параметров отражаются на самочувствии человека: например, при перепадах температуры тела или давления он испытывает дискомфорт.
Справка! Способность организма поддерживать постоянство необходимых значений называется гомеостазом. За динамическое равновесие показателей отвечают любые органы и системы: сердце, почки, печень, сосуды, легкие и т.д.
Еще одна задача иммунитета – не допустить изменений в генетическом составе организма.
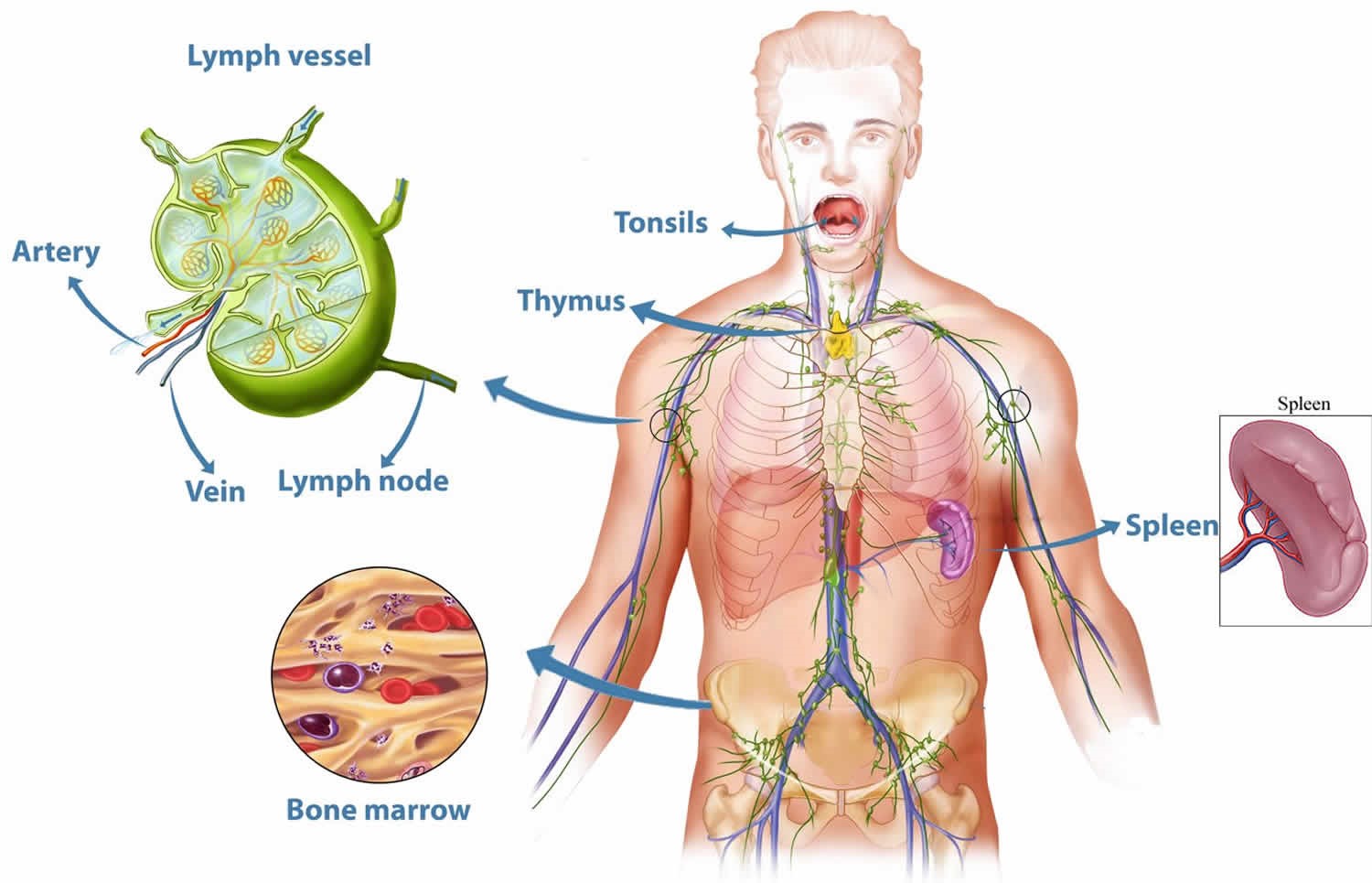
Органы иммунной системы
Многие люди обеспокоены состоянием своего иммунитета и стараются его поддерживать. Однако, задаваясь вопросом, что попить для иммунитета, не каждый представляет себе, где этот самый иммунитет находится и из чего он состоит. Давайте в этом разберемся.
К органам иммунной системы относятся:
Органы иммунной системы выполняют 3 важные функции:
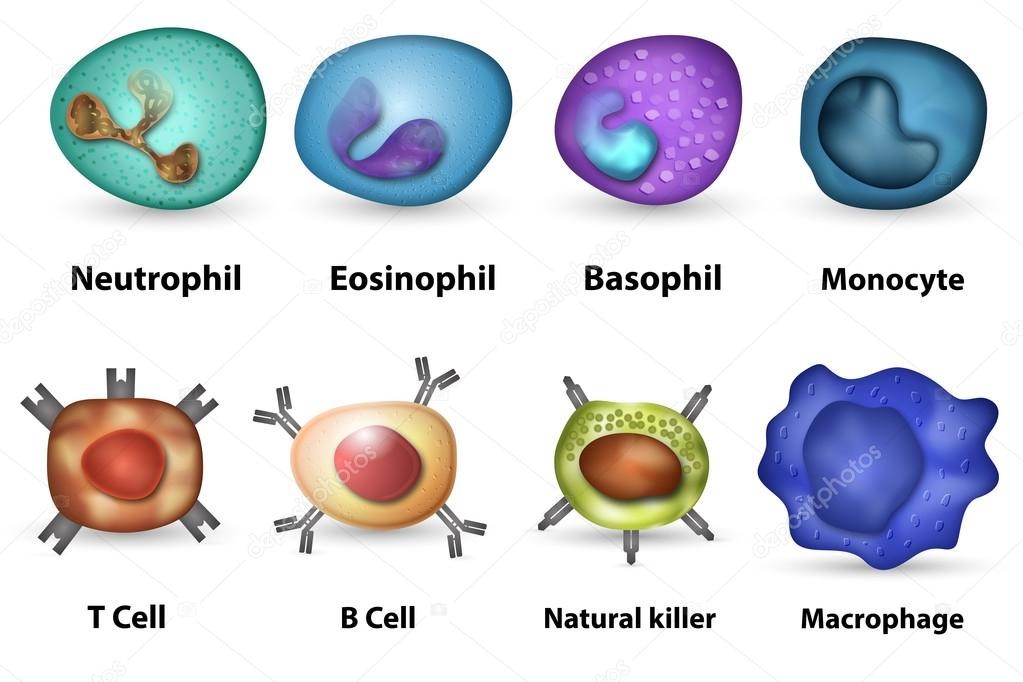
По всему организму расположено огромное количество разных иммунных клеток. К главным их видам относятся:
Справка! Чужеродные агенты обычно называют антигенами. Специфические белки, вырабатываемые лимфоцитами для связывания антигенов – антителами или иммуноглобулинами.
Разновидности иммунитета
Иммунитет можно классифицировать по происхождению и типу реакции. По происхождению он бывает:
Врожденный иммунитет человека начинает формироваться еще в материнской утробе (защищает его в это время иммунитет мамы – через плаценту) и продолжает после появления ребенка на свет. Формироваться иммунной системе новорожденного помогает молозиво. Оно богато кровяными тельцами и антителами, в молоке их гораздо меньше. Молозиво можно расценивать как естественную прививку: именно оно на первых порах помогает организму ребенка бороться с чужеродными агентами. Однако врожденный иммунитет не «запоминает» чужеродные агенты. Он одинаково реагирует на всех возбудителей инфекций. Если бактерия проникнет в организм повторно, неспецифический иммунитет распознает ее как новую угрозу. Проще всего это понять на примере занозы. Каждый раз организм отвечает на ее появление воспалительной реакцией, и всегда она развивается так же, как и впервые.
Борьба с тяжелыми инфекциями неспецифическому иммунитету не под силу, однако не стоит его недооценивать. Именно врожденный иммунитет первым «замечает» угрозу и реагирует на нее. Затем уже подключается специфический иммунитет.
Специфический иммунитет бывает активным и пассивным. Активный формируется при столкновении с новыми для организма бактериями, вирусами и прочими возбудителями инфекций. Пассивный – с помощью молозива и прививок. Каждый раз, сталкиваясь с новым для себя чужеродным агентом (вирусами, простейшими, растительными или животными ядами, аллергенами, бактериями, грибками, модифицированными клетками организма), иммунная система формирует «персональный» ответ для конкретного возбудителя. Также она «запоминает» его. В следующий раз иммунитет уже будет располагать информацией об этом «враге» и антителами к нему, поэтому с легкостью его уничтожит. Именно таким образом формируется специфический иммунитет.
Если врожденный иммунитет у всех одинаков, то приобретенный у каждого человека индивидуален. Многое зависит от особенностей организма, количества прививок, от того, с какими чужеродными агентами сталкивалась иммунная система человека.
Справка! Прививка – один из способов формирования специфического иммунитета. Пациенту вводят ослабленных или мертвых возбудителей инфекции – в таком состоянии они не способны спровоцировать заболевание. Иммунная система получает о них информацию, «запоминает», и если впоследствии столкнется с ними, сразу начинает с ними бороться. В результате болезнь либо не развивается вовсе, либо протекает намного легче.
По типу реакций иммунитет делится на клеточный и гуморальный
Клеточный иммунитет работает благодаря MHC-I (главному комплексу гистосовместимости первого типа). Это группа специфических белков, у каждого человека она уникальна и находится на всех клетках. MHC-I – своеобразная идентификационная карта. Она сообщает иммунитету о том, что данная клетка является частью организма, другими словами – она «своя». Если она изменяется под воздействием вируса или трансформируется в раковую, то метаморфозы происходят и с MHC-I (либо он вовсе «стирается»). Так клетка становится «чужой». Т-киллеры и натуральные киллеры «контролируют» наличие MHC-I, и когда они сталкиваются с его отсутствием или измененным вариантом, то уничтожают клетку.
Гуморальный иммунитет работает иначе. Его главное «оружие» – вырабатываемые B-лимфоцитами антитела. Для каждого чужеродного антигена вырабатываются индивидуальные иммуноглобулины. Их молекулы состоят из 2 участков:
Антитела нейтрализуют чужеродные агенты за счет Fab-участка. Поэтому он «разрабатывается» в соответствии с составом антигена.
Пример реакции иммунной системы
Борьба с чужеродным агентом – сложный процесс, в ходе которого разные иммунные клетки ведут совместную слаженную работу. Это проще представить себе на конкретном примере попадания в организм инфекции. Предположим, на вашей коже возникла царапина. Рана – это «распахнутые врата в организм» для различных бактерий. Однако клетки иммунной системы уже на страже! При нарушении целостности тканей пострадавшие клетки выделяют цитокины, сообщающие другим иммунным клеткам о начале воспалительного процесса. Цитокины – это «весточка» для макрофагов и нейтрофилов. Они устремляются к пострадавшему участку, проходя сквозь стенки капилляров. Начинается процесс уничтожения проникших в рану микроорганизмов. Макрофаги и нейтрофилы их «поедают» и «переваривают». Так работает врожденный, неспецифический иммунитет.
В процессе «пожирания» возбудителей инфекции макрофаги осуществляют презентацию антигена: «демонстрируют» Т-хелперам и B-лимфоцитам фрагменты уничтожаемых бактерий. Те знакомятся с предоставленной информацией и на ее основании «разрабатывают» специфические антитела, которые лучше всего справятся с уничтожением именно этих микроорганизмов. Это занимает достаточно много времени, до 2-х недель, если иммунитет сталкивается с возбудителем инфекции впервые. Затем B-лимфоциты трансформируются в плазматические клетки и вырабатывают антитела, которые распространяются по организму через кровоток. Антитела обволакивают бактерии, буквально «прилипают» к ним, из-за чего микроорганизмы гибнут. На помощь спешат и макрофаги – им легче «пожирать» возбудителей инфекции, когда они находятся в «связанном» состоянии. Так работает специфический гуморальный иммунитет.
Пониженный иммунитет: причины и симптомы
С возрастом иммунитет способен снижаться. Это происходит под влиянием неблагоприятных факторов окружающей среды, вредных привычек, нездорового образа жизни. Ослабленный иммунитет уже не успевает отслеживать всех возбудителей заболеваний, проникших в организм, и своевременно убивать их. Так развиваются острые и хронические заболевания, ускоряются процессы старения.
К причинам, влияющим на снижение иммунитета, относят:
Симптомами ослабленного иммунитета являются:
Важно! При наличии симптомов снижения иммунитета необходимо обязательно обратиться к врачу. В противном случае могут развиться иммунодефицитные состояния (снижение активности гуморального и клеточного иммунитета).
Укрепление иммунитета
Восстановление иммунитета и профилактика его ухудшения проводятся с соблюдением одних и тех же правил:
Справка! Укрепление иммунитета у взрослых подразумевает также отказ от вредных привычек: курения, частого употребления спиртного.
Чаще всего вредоносные бактерии и вирусы попадают в организм через нос, полость рта, желудок и кожу. Поэтому необходимо тщательно соблюдать личную гигиену – это также позволит укрепить иммунитет. Регулярно посещайте стоматолога, не допускайте развития патологий зубов и десен!
Стимулировать работу иммунной системы помогают специальные препараты – иммуномодуляторы. Однако принимать решение о целесообразности их приема (как и выбирать средства) должен врач.
Если у вас наблюдаются признаки ослабления иммунитета, запишитесь на прием к врачу-иммунологу Поликлиники Отрадное! Опытные врачи проведут необходимые исследования, выявят нарушения и назначат необходимое лечение. Также вы можете прийти на консультацию, даже если у вас нет тревожных симптомов, и провести вакцинацию качественными препаратами.
Иммунная система человека
к.м.н. Гольдинберг Б. М., Васюк Я.В.
Городской центр трансфузиологии учреждения здравоохранения «6-я городская клиническая больница», г. Минск,
учреждение здравоохранения «7-я городская детская поликлиника», г. Минск
ИММУНННАЯ СИСТЕМА ЧЕЛОВЕКА
Введение
Группа органов, имеющих общее происхождение, единый план строения и выполняющая общую функцию называется системой органов. Пять из всех десяти систем органов являются регулирующими (управляющими): нервная, кровеносная, эндокринная, лимфатическая и иммунная. Уточним, что лимфатические органы и лимфатических узлы, которых насчитывается около 600, функционально является частью иммунной системы, а к собственно лимфатической системе относится обширная сеть сосудов, которая проходит почти через все наши ткани, обеспечивая движение жидкости, называемой лимфой.
Слово «иммунитет» происходит от латинского «immunis» (на английском – immunity), что означает «чистый от чего-либо», невосприимчивый к чему-либо. Иммунная система появилась вместе с многоклеточными организмами и развивалась, как помощница их выживанию. Она объединяет органы и ткани, которые гарантируют защиту организма от генетически чужеродных клеток и веществ, поступающих из окружающей среды.
Иммунная система представлена тремя уровнями: органным, клеточным и молекулярным.
Органы иммунной системы человека
Иммунная система включает центральные и периферические органы.
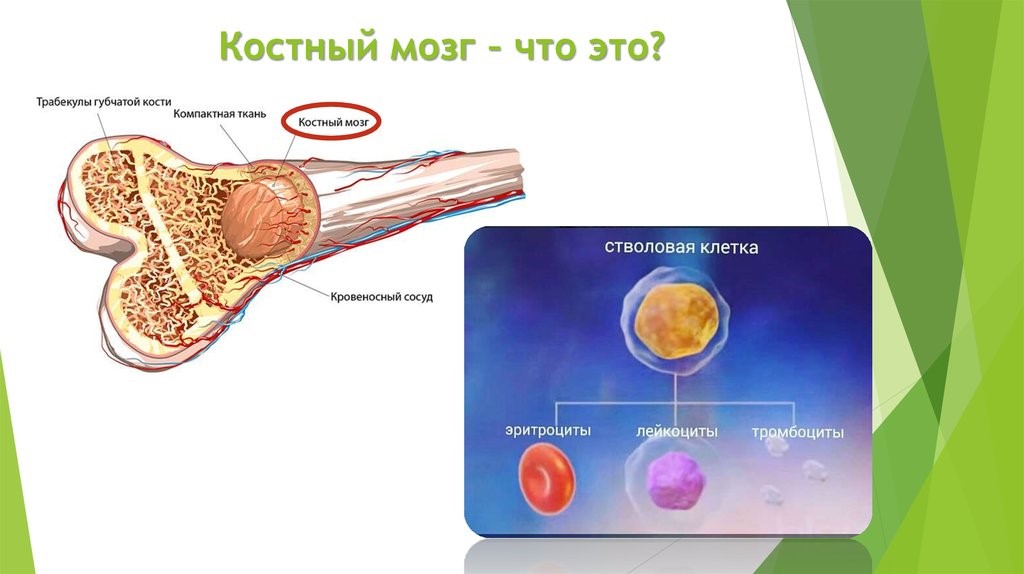
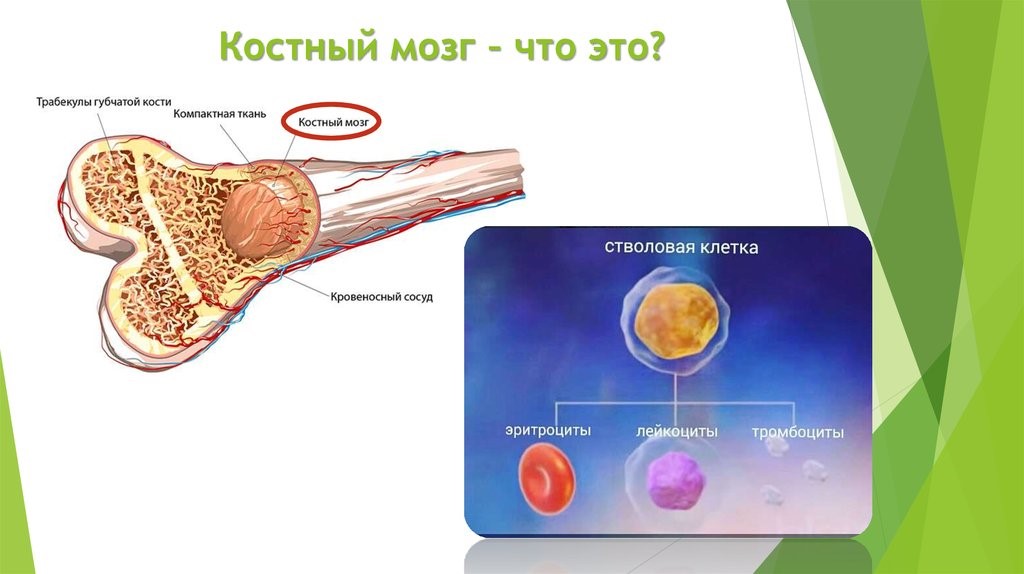
Центральные органы иммунной системы представляют собой красный костный мозг и тимус.
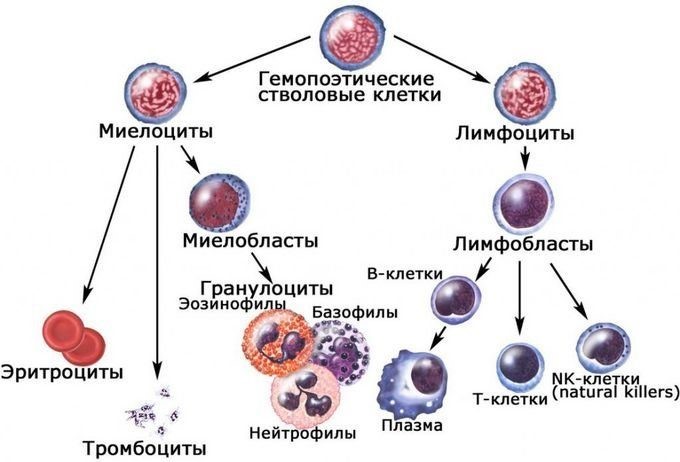
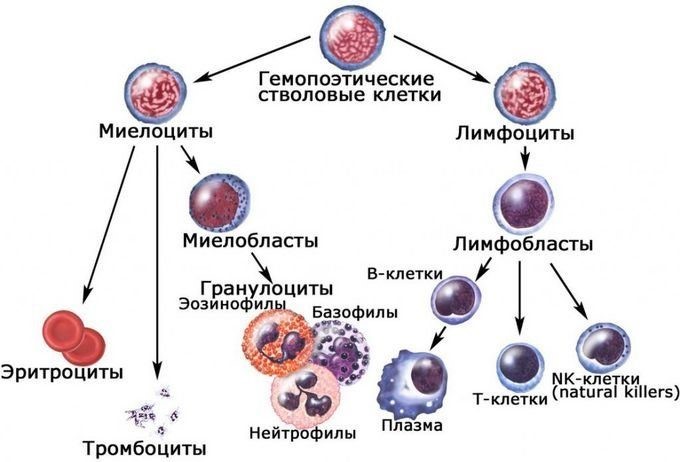
Костный мозг является хранилищем стволовых клеток, из которых образуются клетки крови (рис.1). В зависимости от ситуации, стволовые клетки трансформируются в иммунные В-лимфоциты. При необходимости, определенная часть B-лимфоцитов превращается в плазматические клетки, которые способны вырабатывать антитела.
Рис.1. Костный мозг содержит стволовые клетки
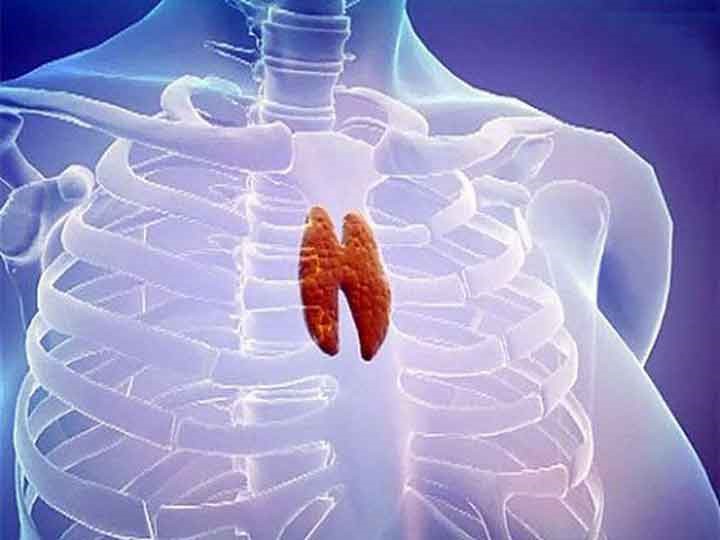
Тимус (или вилочковая железа) – один из главных органов иммунной системы, расположенный у человека за грудиной ниже ключиц, который отвечает за образование Т-клеток иммунной системы в лимфоидных тканях организма (рис.2).
К периферическим органам относятся селезенка, миндалины и лимфоузлы, в которых находятся зоны созревания иммунных клеток.
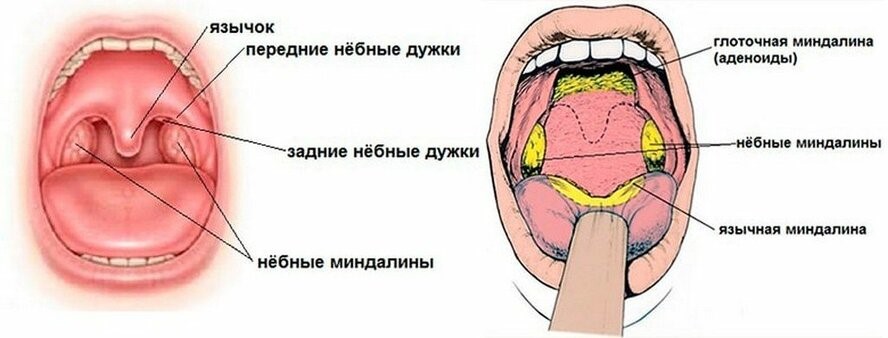
Миндалины, получившие свое название из-за внешней схожести с миндалем, представляют собой скопление лимфоидной ткани в верхней части носоглотки. У человека шесть миндалин: две небные, две грудные и по одной носоглоточной и язычной.
Самыми крупными из них являются небные миндалины, или гланды, которых легко осмотреть самостоятельно в зеркале, если достаточно широко раскрыть рот (рис.3).
Рис. 3. Небные миндалины
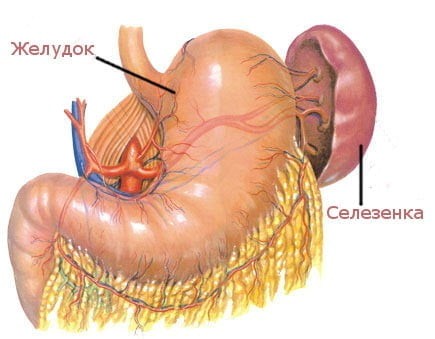
Селезенка является самым крупным лимфоидным органом (рис. 4). Кроме того, она может накапливать некоторое количество крови. В экстренных ситуациях селезенка способна послать свои запасы в общий кровоток. Это позволяет улучшить качество и скорость иммунных реакций организма. Селезенка очищает кровь от бактерий и перерабатывает всевозможные вредные вещества. В ней полностью разрушаются эндотоксины, а также остатки умерших клеток при ожогах, травмах или других повреждениях тканей. У людей, оставшихся по какой-либо причине без селезенки, ухудшается иммунитет.
Лимфатические узлы представляют собой небольшие образования округлой формы (рис. 5), расположенные в грудной полости (бронхолегочные, бронхотрахеальные) и брюшной полости (пейеровы бляшки, аппендикс и другие), окологрудные на поверхности грудной клетки, на шее и на конечностях. Лимфоузел – это один из барьеров на пути инфекций и раковых клеток, играющий роль своеобразной таможни (рис. 5). В нем образуются лимфоциты – специальные клетки, которые принимают активное участие в уничтожении вредных веществ.
Центральные органы иммунной системы отвечают за образование и созревание клеток, а периферические органы обеспечивают защиту, то есть иммунный ответ. Периферические и центральные органы иммунной системы выполняют свои работу только вместе и если выходит из строя какой-либо один из этих органов, то организм лишится защитного барьера.
Компоненты иммунной системы
Современная иммунология различает два взаимодействующих компонента иммунной системы – врожденный и приобретенный виды иммунитета, обеспечивающие развитие иммунного ответа на генетически чужеродные субстанции (сущности).
Врожденный (видовой) иммунитет – наследственно закрепленная система защиты организма человека от патогенных и непатогенных микроорганизмов, а также продуктов тканевого распада. Клетки врожденного иммунитета распознают патоген по специфичным для него молекулярным маркёрам – так называемым «образам патогенности». Эти маркёры не позволяют точно определить принадлежность патогена к тому или иному виду, а лишь сигнализируют о том, что иммунитет столкнулся с возмутителями спокойствия: чужаком или своим, но ставшим для организма предателем (рис.6).
Рис.6. Врожденный иммунитет: главное – спокойствие!
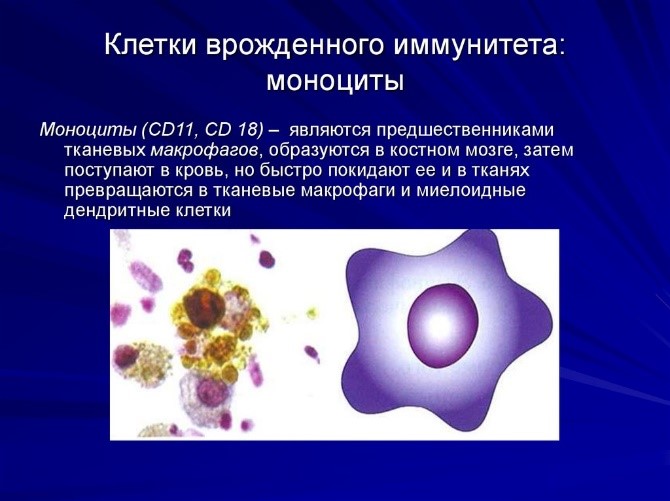
Врожденный иммунитет на клеточном уровне представляют:
Рис.8. Дендритная клетка и
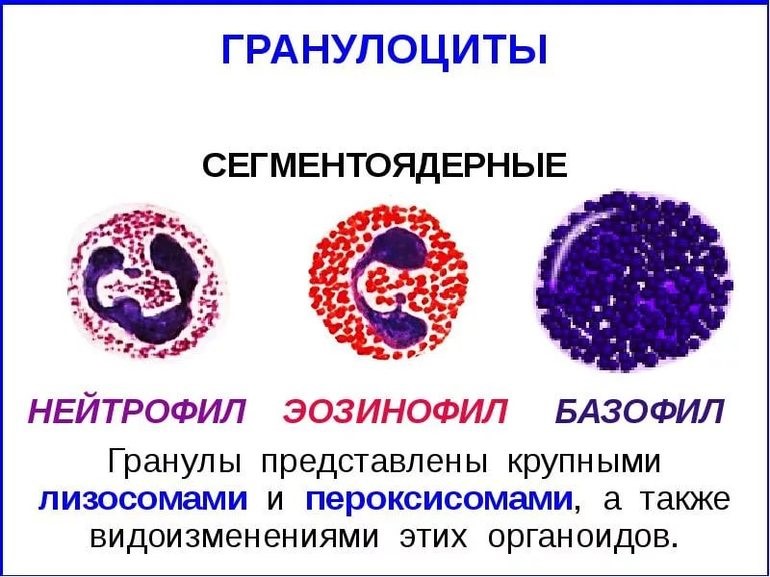
Нейтрофилы – самые многочисленные иммунные клетки в крови человека. Они циркулируют в крови всего 8-10 часов и бόльшую часть своей жизни путешествуют по тканям организма. При встрече с патогеном они его захватывают и переваривают, после чего обычно сами погибают. Из разрушенных нейтрофилов высвобождаются гранулы, содержащие антибиотические вещества.
Гранулы эозинофилов и базофилов осуществляют химическую защиту организма от крупных патогенов, например, паразитических червей, грибов, внеклеточных бактерий. Однако при чрезмерной активности могут участвовать и в развитии аллергической реакции;
Рис.10. Натуральный киллер
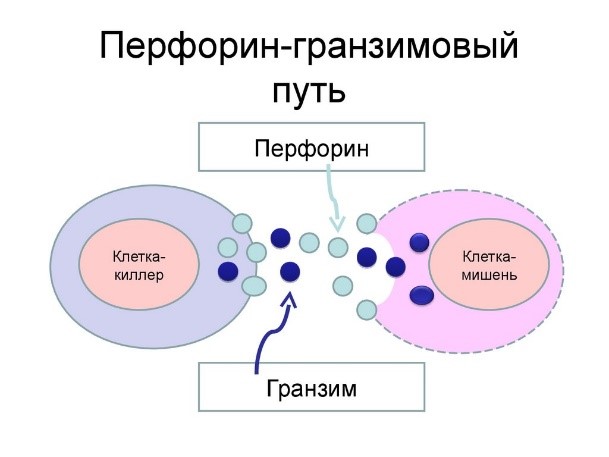
Действуют натуральные киллеры с помощью агрессивных веществ перфорина и гранзима, которые наподобие буравчиков «кусают» и разрушают пораженную клетку, ставшую для них мишенью (рис.11)
Рис.11. Проникновение перфорина и гранзима в раковую клетку и ее уничтожение
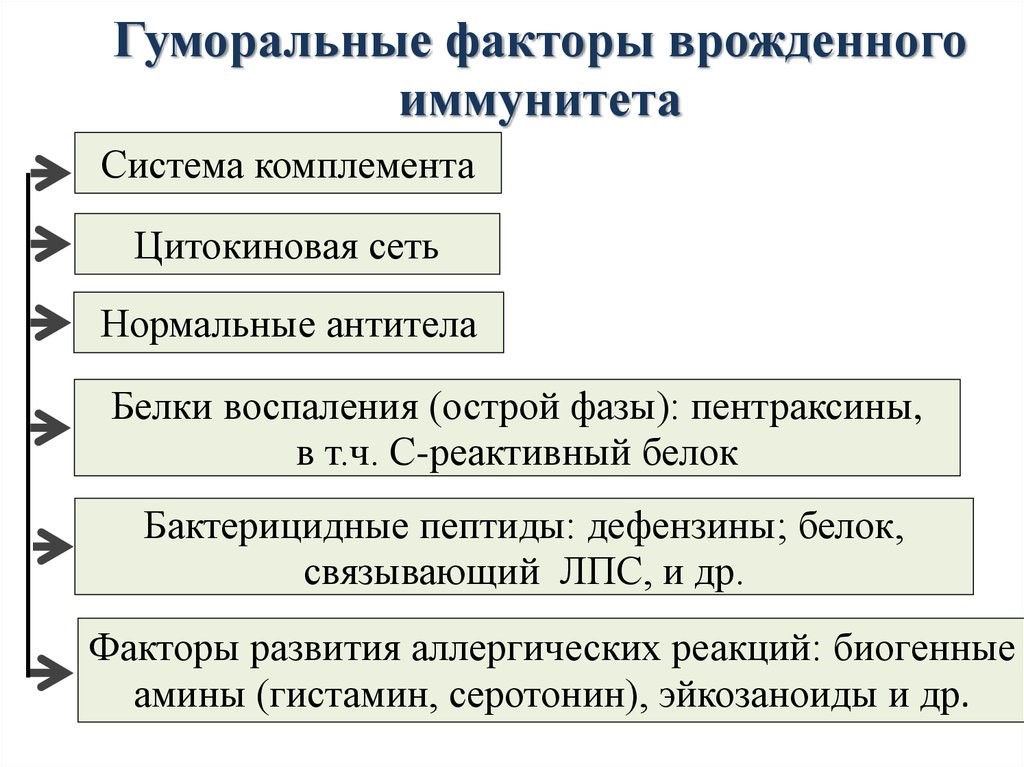
Молекулярными(гуморальные) факторами врожденного иммунитета являются (рис.12):
Рис.12.Гуморальные факторы врожденного иммунитета
Система комплемента – это многокомпонентная самособирающаяся система более 20 сывороточных белков, которые в норме находятся в неактивном состоянии.
После активации проявляются биологические эффекты комплемента: образование мембраноатакающего комплекса для лизиса патогенов, выброса медиаторов воспаления для привлечения фагоцитов и усиления их поглотительной способности.
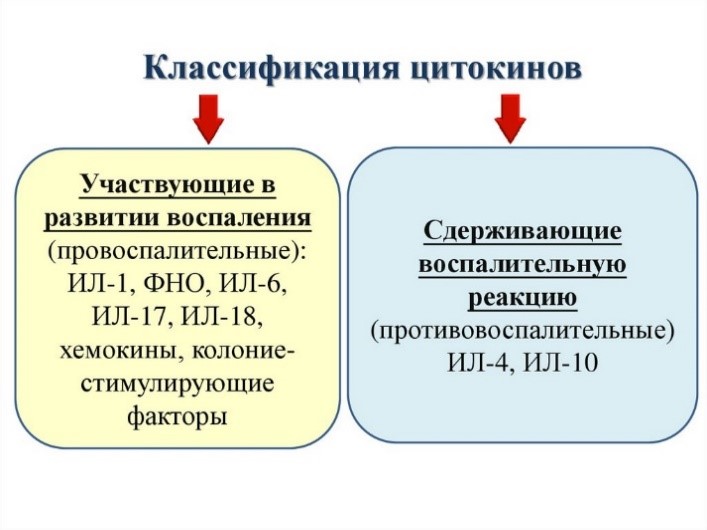
Цитокины – это система низкомолекулярных белков организма, синтезируемых преимущественно активными клетками иммунной и кроветворной систем, регулирующих межклеточные взаимодействия «универсальный» язык для всех клеток), представленные на рис.13 и 14.
Рис. 13. Цитокины: ИЛ – интерлейкины, которых в настоящее время насчитывается 34 разновидности;
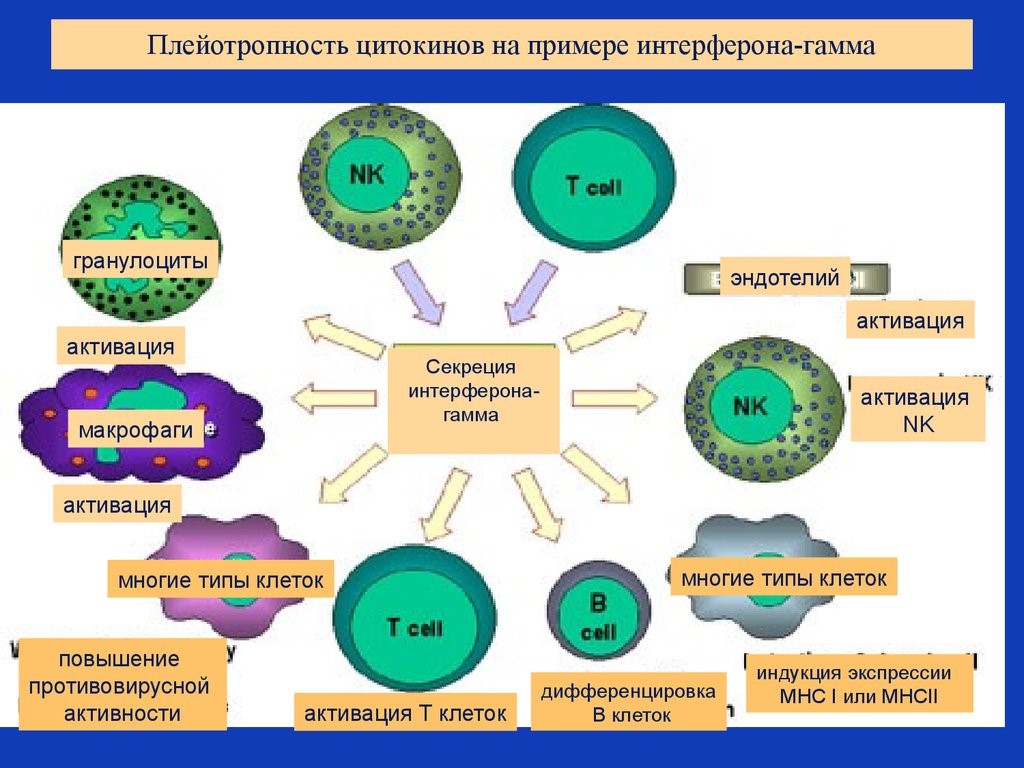
Рис. 14. Разнонаправленность действия цитокинов на примере гамма-интерферона
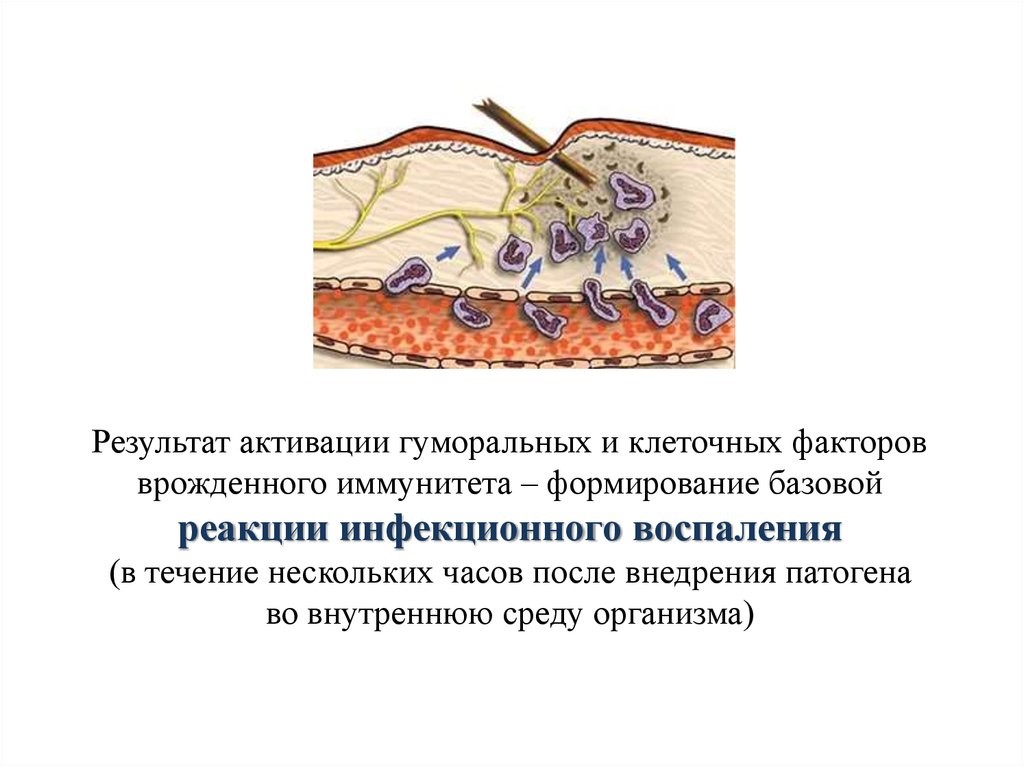
В результате активации гуморальных и клеточных факторов врожденного иммунитета в течение нескольких часов после внедрения патогена во внутреннюю среду организма формируется базовая реакция инфекционного воспаления (рис. 15)
Рис. 15. Инфекционное воспаление ткани на месте внедрения инородного тела с целью его удаления
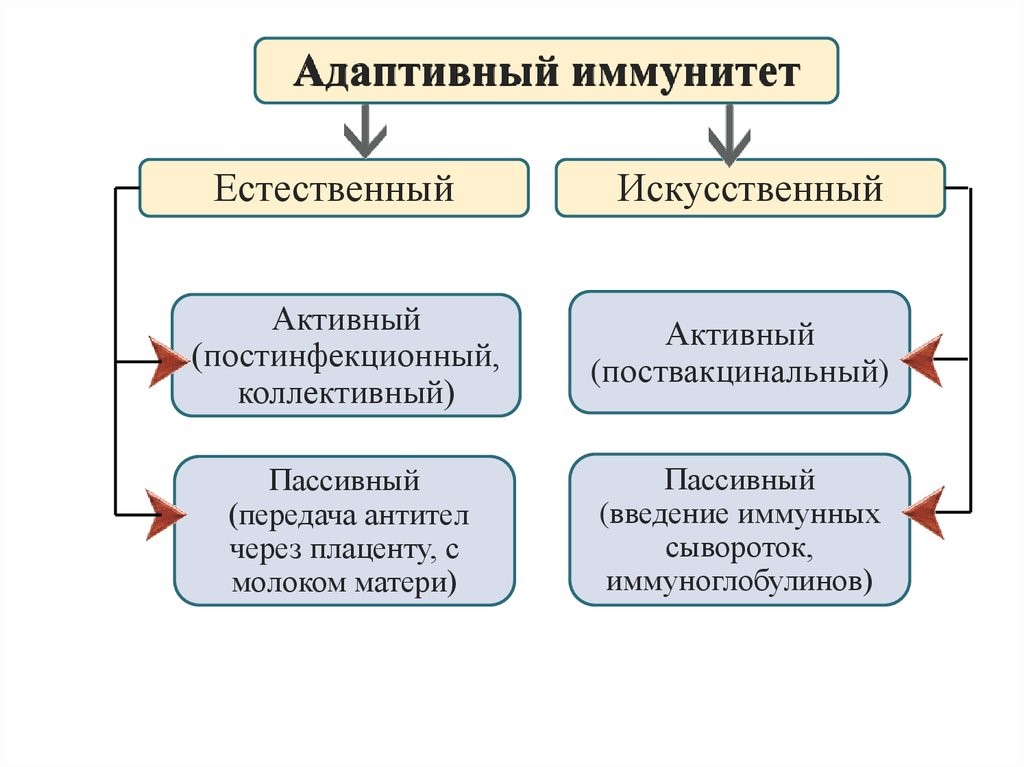
Приобретенный иммунитет (или адаптивный – от франц. adapter «приспосабливать») формируется индивидуально в течение жизни под влиянием антигенной стимуляции и, в свою очередь, подразделяется на естественный и искусственный (рис.16).
Естественный иммунитет формируется при встрече с патогеном, в результате чего в организме вырабатываются защитные иммунные факторы (активный естественный иммунитет), либо они попадают в готовом виде из материнского оргазма в период внутриутробного развития или при грудном вскармливании (пассивный естественный иммунитет).
Искусственный иммунитет создается путем введения вакцин или анатоксинов, которые стимулируют выработку антител против конкретных патогенов или их ядов. При этом с профилактической целью воспроизводится процесс реакции иммунной системы пациента на патоген, но в бессимптомной или легкой клинической форме с сохранением их защитной иммунной силы в течение нескольких месяцев, лет или даже пожизненно (искусственный активный иммунитет). Когда необходимо быстро и на короткое время защитить пациента от реального риска встречи с патогеном во время эпидемии или нейтрализовать уже проникший в его организм патоген применяются иммуноглобулины (антитела) как в очищенном виде, так и в дозированных объемах плазмы или сыворотки, полученных из крови донора (человека или животного). Применение готовых антител формирует пассивный искусственный иммунитет, сохраняющийся 2-3 недели.
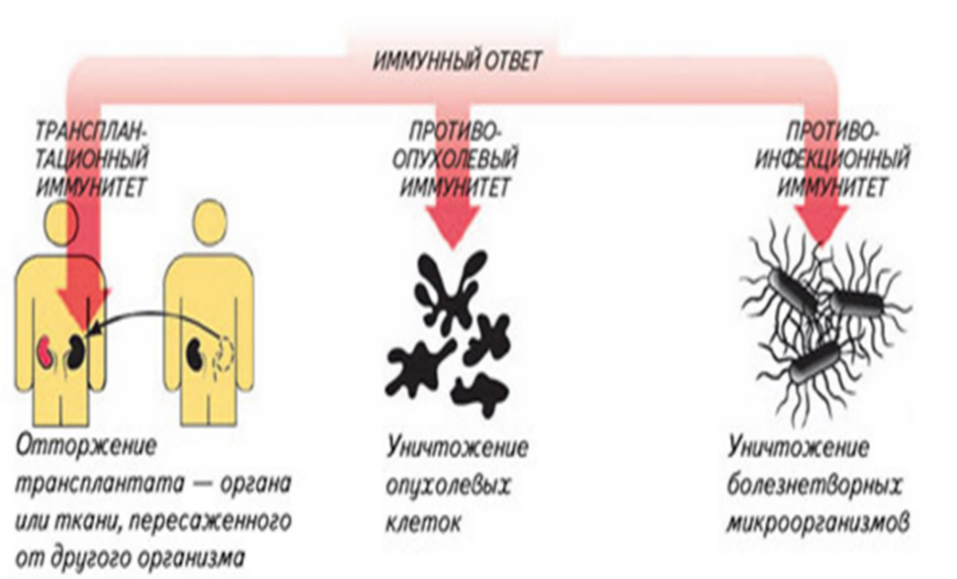
Адаптивный иммунитет основывается на трех главных процессах:
Рис.17.Варианты реагирования иммунной системы на пересадку органов или тканей, возникновение злокачественных новообразований и инфекций
Иммунокомпетентными клетками адаптивного иммунитета являются лимфоциты, которые живут в организме человека от нескольких месяцев до несколько лет. По функциям клетки подразделяются на Т-лимфоциты – 80% и В-лимфоциты – 20%.
То, что Т-лимфоцит распознает только чужеродные антигены, а не молекулы собственного организма, является следствием процесса, называемого селекцией, которая происходит в тимусе, где завершают свое развитие Т-клетки. Суть селекции такова: клетки, окружающие юный, или наивный, лимфоцит, показывают (презентируют) ему пептиды собственных белков. Тот лимфоцит, который слишком хорошо или слишком плохо узнает эти белковые фрагменты, уничтожается. Выжившие же клетки (а это менее 1% всех предшественников Т-лимфоцитов, пришедших в тимус) обладают промежуточным сродством к антигену, следовательно, они, как правило, не считают собственные клетки мишенями для атаки, но имеют возможность среагировать на подходящий чужеродный пептид.
Для активации Т-лимфоцита нужно, чтобы он получил специальные сигналы от рецепторов лейкоцитарной антигенной системы и коктейля из множества провоспалительных цитокинов.
С помощью специальных реагентов определяются маркеры поверхностных белков лейкоцитов определенного типа, которые называются кластерами дифференциации (Сluster of differentiation) – CD. В настоящее время известно 350 CD-антигенов и их подтипов (табл. 1).
Таблица 1. Главные идентификациионные СD-маркёры клеток
Лимфоидная стволовая клетка
CD19, CD72, CD79 и др.
Т-лимфоциты распознают клетки, несущие чужеродные антигены, и уничтожают их после непосредственного контакта (атаки), а также выполняют функцию регуляции иммунного ответа.
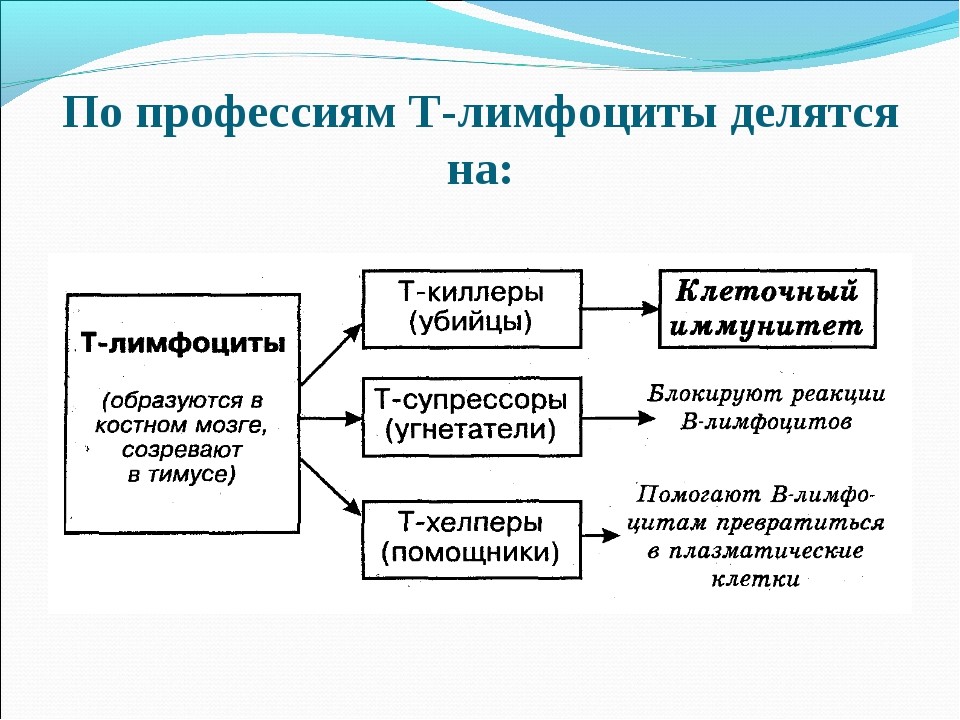
Т-лимфоциты имеют подтипы (рис. 18):
Рис. 18. Подтипы Т-лимфоцитов и их функции
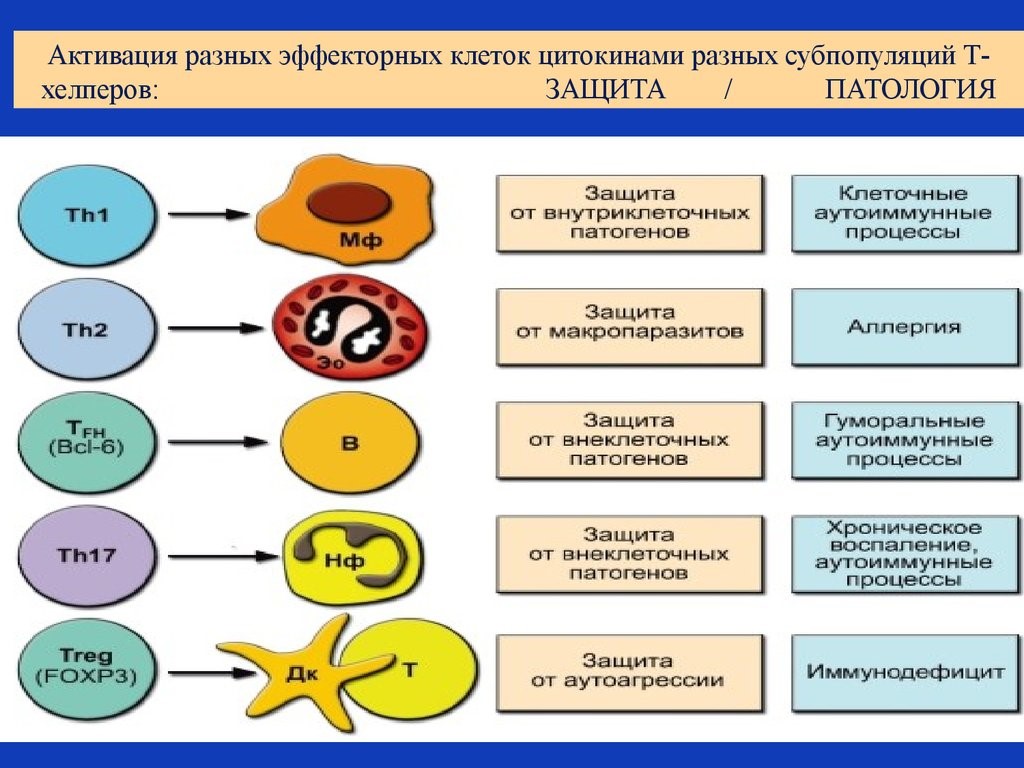
Рис. 19. Активация цитокинами разных субпопуляций Т-хелперов
Соотношение количества клеток CD4/CD8 называют иммунорегуляторным индексом (ИРИ). Если у пациента ИРИ повышен (более 2,2), то это говорит о чрезмерной активности T-хелперов и ослаблении регулирующей функции T-киллеров. При таком показателе иммунные клетки могут разрушать собственные ткани организма. Повышенный ИРИ чаще всего отмечается у пациентов с аутоиммунными болезнями (системной красной волчанкой, склеродермией, ревматоидным артритом и др.). Причиной чрезмерной активности T-хелперов может также стать опухоль вилочковой железы. При этой патологии продуцируется избыточное количество лимфоцитов. Высокие показатели ИРИ отмечаются при остром лимфобластном лейкозе. Это тяжелое онкологическое заболевание сопровождается неконтролируемым увеличением количества незрелых лимфоцитов.
Если иммунорегуляторный индекс понижен (менее1,6), то это говорит о серьезном ухудшении работы иммунитета. Низкие показатели ИРИ свидетельствуют о том, что в организме ослаблена функция защитных клеток, а регуляция со стороны T-киллеров чрезмерна. Обычно это отмечается при следующих патологиях, сопровождающихся иммунодефицитом: инфекционных болезнях (в том числе ВИЧ-инфекции); врожденном иммунодефиците; любых затяжных и хронических болезнях; опухолях костного мозга.
В-лимфоциты ответственны за гуморальное звено иммунитета – продукцию антител. После антигенного стимула В-лимфоцит превращается в лимфобласт – клетку, способную к делению. Часть лимфобластов дифференцируется в В-лимфоциты памяти, другая часть превращается в плазматические клетки, которые осуществляют продукцию антител.
В-лимфоциты несут на своей поверхности В-клеточный рецептор. При контакте с антигеном эти клетки активируются и превращаются в особый клеточный подтип – плазматические клетки, живущие до трех недель и обладающие уникальной способностью секретировать в этот срок тысячи антител.
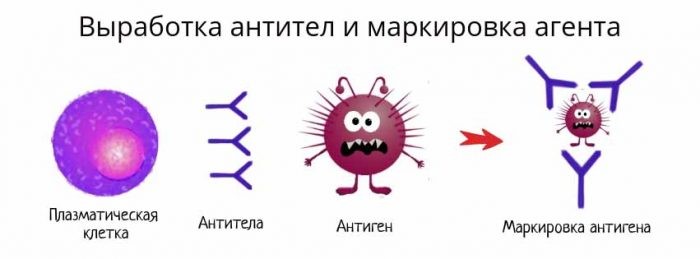
Антитело имеет сродство к распознаваемому им антигену, как бы «прилипает» к нему. Это дает возможность антителам обволакивать (опсонизировать) клетки и вирусные частицы, покрытые молекулами антигена, привлекая макрофаги и другие иммунные клетки для уничтожения патогена. Антитела также умеют активировать специальный каскад иммунологических реакций, называемый системой комплемента, который приводит к перфорации клеточной мембраны патогена и его гибели.
Рис. 20. Выработка антител и маркировка патогена
Различают несколько классов антител (иммуноглобулинов). Первыми после антигенного раздражения, вызывающих агглютинацию бактерий и нейтрализацию вирусов, появляются иммуноглобулины М (IgM). В длительном иммунитете участвуют иммуноглобулины G(IgG).
В табл.2 представлена интерпретация лабораторных исследований на наличие патогена на молекулярном уровне и с помощью тестов на иммуноглобулины М и G.
Таблица 2. Интерпретация лабораторных исследований на наличие патогена на молекулярном уровне
Результат молекулярного исследования
Инфицированный или повторно инфицированный пациент
Ранние стадии инфекции. Требуется дополнительное исследование
Инфекция. Требуется дополнительное исследование
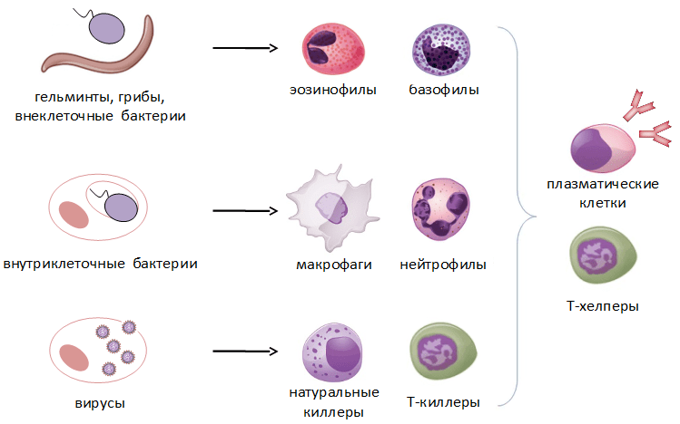
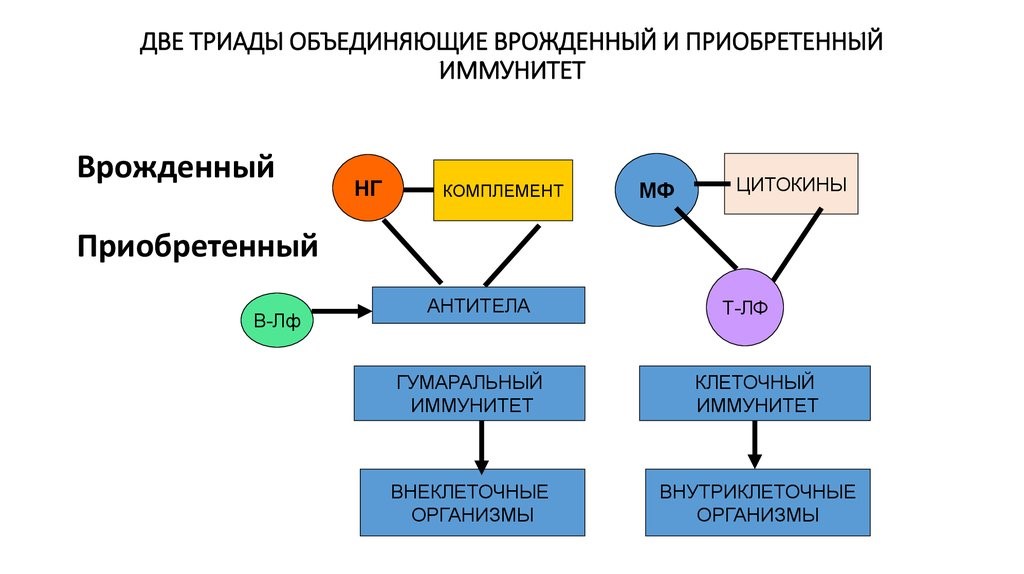
Врожденный и приобретенный виды иммунитета имеют точки соприкосновения, которые представляют две триады (рис.21)
Рис. 21. Две триады, объединяющие врожденный и приобретенный виды иммунитета
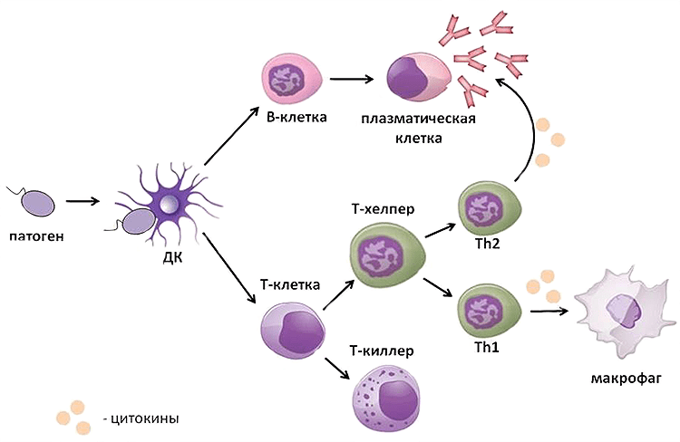
Развитие адаптивного иммунного ответа требует достаточно много времени (от нескольких дней до двух недель), и для того чтобы организм мог защищаться от уже знакомой инфекции быстрее, из Т- и В-клеток, участвовавших в прошлых битвах, формируются так называемые клетки памяти. Они, подобно ветеранам, в небольшом количестве присутствуют в организме, и, если появляется знакомый им патоген, вновь активируются, быстро делятся и целой армией выходят на защиту границ (рис.22).
Рис.22. Т-клетки памяти быстро формирует вторичный иммунный ответ
Иммунологическая толерантность
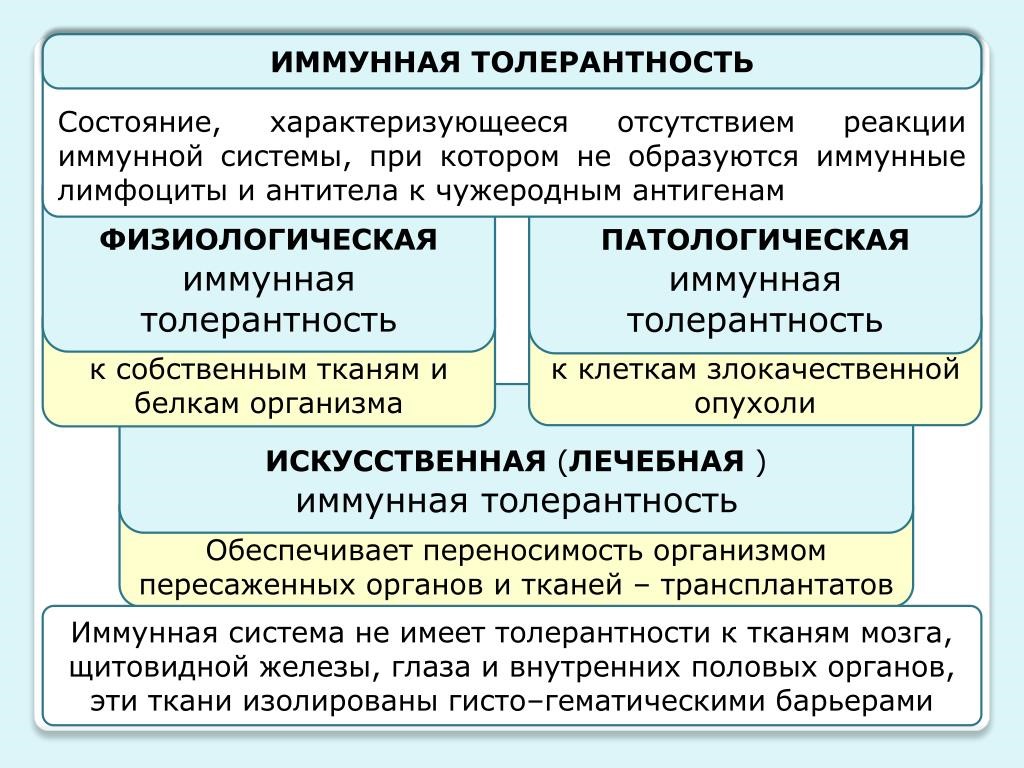
Под иммунологической толерантностью (терпимостью, ареактивностью) понимают отсутствие иммунного ответа на специфический антиген. Перечень антигенов, к которым может развиваться толерантность, практически неотличим от набора антигенов, против которых развивается специфический иммунный ответ (рис.23).
Рис. 23. Иммунная толерантность
Механизмы толерантности необходимы, поскольку иммунная система продуцирует огромное число разнообразных антиген специфичных рецепторов, и некоторые из них оказываются специфичными к собственным антигенам организма; толерантность предотвращает нежелательные реакции против собственных органов и тканей, также для нормального протекания беременности.
Нарушения иммунной системы у человека
Нарушения в работе иммунной системы можно подразделить на три категории: иммунодефициты, аутоиммунные заболевания и реакции гиперчувствительности.
Иммунодефициты
Иммунодефицит – снижение количественных показателей и/или функциональной активности основных компонентов иммунной системы, приводящее к нарушению защиты организма от патогенных микроорганизмов и проявляющееся повышенной инфекционной заболеваемостью.
Первичные иммунодефициты (ПИД) – наследственные заболевания, обусловленные дефектами генов, контролирующих иммунный ответ. В основном ПИД заявляют о себе уже в раннем детском возрасте, но иногда лишь к 30-40 годам жизни.
По механизмам развития выделяют 4 основные группы ПИД (табл.3):
Таблица 3. Некоторые первичные иммунодефициты
Частые бактериальные инфекции
Дефицит или полное отсутствие В-лимфоцитов
Антибиотики, пожизненное введение IgG
Частые респираторные инфекции, отиты
Дефекты Т- и В- лимфоцитов
Антибиотики, пожизненное введение IgG
Атаксия-телеангиоэкстазия (синдром Луи-Бар)
Аномалия двигательной функции, слабость мышц, нарушение речи
Дефицит Т- и В- лимфоцитов
ПИД, обусловленные дефектами фагоцитоза
Хроническая гранулёматозная болезнь
Частые пневмонии, гнойные инфекции
Пожизненная антибактериальная и противогрибковая терапия, интерферон гамма
ПИД, обусловленные дефектами в системе комплемента
Наследственный ангионевротический отек
Отеки губ и век при отсутствии зуда. Отеки гортани, носа, языка опасны для жизни
Низкая концентрация ингибитора эстеразы С1
Введение концентрата ингибитора эстеразы С1
Как следует из табл.3, основным и часто единственным методом лечения большинства пациентов с первичными В-клеточными иммунодефицитами являются иммуноглобулины. Это лекарственные средства, получаемые из плазмы крови человека. Они призваны заменить защитные антитела, отсутствующие в иммунной системе, с целью предотвращения или остановки развития тяжелых инфекционных заболеваний. Сегодня в арсенале врача имеются иммуноглобулины, различающиеся по концентрации активного вещества (5 и 10%), а также по способу введения (внутривенный и подкожный).
ПИД может проявиться в любом возрасте. В зависимости от этого у пациента возникают своеобразные проблемы, требующие определенных видов поддержки на протяжении всей жизни (табл. 4).
Таблица 4. Необходимость в видах поддержки пациента с ПИД в различных возрастных группах
В возрасте от 0 до 14 лет требуется уход со стороны родителей, направленный на профилактику инфекций и на период лечения. Могут потребоваться: обучение на дому; оказание психологической помощи; социальная поддержка в приобретении лекарственных средств.
В подростковом возрасте (14-18 лет) дополнительно могут возникнуть потребности в продолжении непрерывного обучения, профессиональной ориентации, налаживании взаимоотношений со сверстниками, организации досуга.
В возрасте от 18 до 65 лет у пациентов чаще возникают инфекционные осложнения, а с ними и расходы на приобретение лекарственных средств, не подлежащих восполнению, а также проблемы с трудоустройством.
В пожилом возрасте (старше 65 лет) возникают потребности в материальной, социальной и психологической поддержке пациента с ПИД.
Аутоиммунная патология
Повреждение собственных органов и тканей организма иммунной системой называется аутоиммунным процессом. Заболеваниями такого типа страдает около 5% человечества. В организме пациента развиваются боевые действия, напоминающие гражданскую войну: в атаку идут «свои против своих». В этой борьбе победителей нет – одни страдания.
Селекция Т-лимфоцитов в тимусе, а также удаление аутореактивных клеток на периферии (центральная и периферическая иммунологическая толерантность), о которых мы говорили ранее, не могут полностью избавить организм от аутореактивных Т-лимфоцитов. Что же касается В-лимфоцитов, вопрос о том, насколько строго осуществляется их селекция, до сих пор остается открытым. Поэтому в организме каждого человека обязательно присутствует множество аутореактивных лимфоцитов, которые в случае развития аутоиммунной реакции могут повреждать собственные органы и ткани.
В качестве аналога можно привести созданную турками в ХIV веке янычарскую пехоту, в которую набирали юношей-христиан 8-16 лет, воевших против своих сородичей.
Т-клеточная аутоиммуннная агрессия хорошо изучена при ревматоидном артрите, сахарном диабете первого типа, рассеянном склерозе и многих других болезнях.
Такие же клетки-янычары, не помнящие своего родства, прослеживаются среди В-лимфоцитов:
Например, вследствие срыва иммунологической толерантности происходит активация В-лимфоцитов, продуцирующих антитела. Это приводит к выраженному повышению выработки тиреоидных гормонов (Т4 и Т3), а также к увеличению щитовидной железы в размерах (гипертрофии). Патология носит название болезнь Грейвса.
Еще одним примером может быть миастения гравис, которая характеризуется слабостью скелетной мускулатуры вследствие образования аутоантител против структур, отвечающих за холинергическую передачу и сокращение мышечного волокна;
Как правило, аутоиммунное заболевание возникает внезапно, и невозможно точно определить, что стало его причиной. Считается, что триггером для запуска может послужить практически любая стрессовая ситуация, будь то перенесенная инфекция, травма или переохлаждение. Значительный вклад в вероятность возникновения аутоиммунного заболевания вносит как образ жизни человека, так и генетическая предрасположенность – наличие определенного варианта какого-либо гена.
Гиперчувствительность
Под гиперчувствительностью понимают чрезмерный иммунный ответ на какой-либо антиген. Реакции гиперчувствительности подразделяют на несколько типов в зависимости от их длительности и механизмов, лежащих в их основе:
Эффективные методы воздействия на иммунитет:
Спекулятивные методы вокруг иммунитета:
Заключение
Иммунная система представлена тремя уровнями: органным, клеточным и молекулярным со сложнейшими взаимодействиями между ними.
Современная иммунология различает два взаимодействующих компонента иммунной системы – врожденный и приобретенный (адаптивный) виды иммунитета, обеспечивающие развитие иммунного ответа на генетически чужеродные субстанции, которые представляют собой микроорганизмы, злокачественные опухолевые клетки, пересаженные органы и ткани.
Адаптивный иммунитет основывается на трех главных процессах: распознавание антигенов, их удаление (элиминация) и формирование иммунологической памяти.
Поломки в структуре иммунной системы приводят к развитию иммунодефицитов, аутоиммунным заболеваниям или реакции гиперчувствительности.
Иммунодефицит на генетическом уровне (первичный) или приобретенный (вторичный) может проявиться в любом возрасте и привести к повышенной инфекционной заболеваемости. В последние годы появились средства заместительной терапии, которые продлевают жизнь этим пациентам. Для повышения качества их жизни требуется не только обеспечение дорогостоящим лечением, но и организация поддержки со стороны семьи, психологов и социальных институтов.
Аутоиммунные заболевания и гиперчувствительность – это неспособность организма противостоять разбушевавшейся иммунной системе, которая перепутала свое и чужое.
К сожалению, ни одно из заболеваний иммунной системы медицина еще не научилась излечивать, а только применять заместительную терапию.
Эффективными профилактическими методами воздействия на иммунную систему являются вакцинация и здоровый образ жизни. Купить иммунитет в аптеке пока никому не удалось.