инфаркт септального отдела на экг что это
Инфаркт септального отдела на экг что это
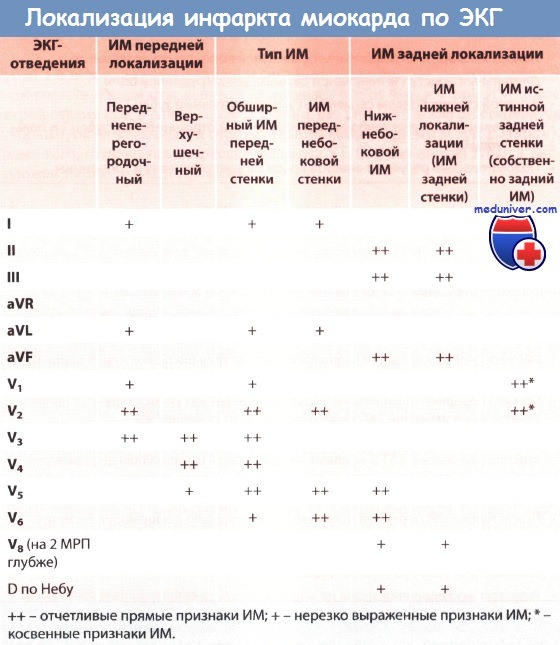
Инфаркт миокарда с подъемом сегмента ST (ИМпST) в зависимости от локализации можно отнести к одному из двух типов: ИМ передней локализации и ИМ задней локализации.
• ИМ передней локализации развивается вследствие окклюзии левой коронарной артерии и/или ее ветвей
• При ИМ передней локализации в грудных отведениях регистрируются более отчетливые изменения ЭКГ, чем в отведениях от конечностей
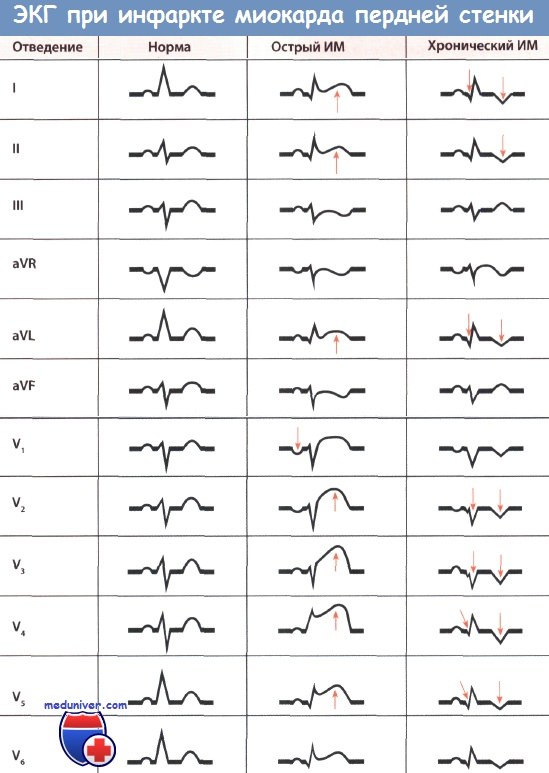
• При остром, или «свежем» инфаркте миокарда (ИМ) передней локализации регистрируется отчетливый подъем сегмента ST и положительный зубец Т (монофазная деформация), особенно отчетливые в грудных отведениях V1-V6 в зависимости от размеров зоны инфаркта. Зубец Q может быть большим.
• При «старом» инфаркте миокарда (ИМ) передней локализации монофазная деформация сегмента ST уже отсутствует. Регистрируются большой зубец Q, депрессия сегмента ST и отрицательный зубец Т во всех или некоторых грудных отведениях V1-V6 в зависимости от размера зоны инфаркта.
• Результат исследования крови на маркеры некроза миокарда положительный.
При инфаркте миокарда (ИМ) передней локализации зона некроза располагается в передней стенке ЛЖ. Инфаркт ПЖ встречается крайне редко. Причиной ИМ передней локализации бывает окклюзия левой коронарной артерии или ее ветвей.
ЭКГ-признаки инфаркта миокарда (ИМ) передней стенки в грудных отведениях и отведениях от конечностей разные. Прежде всего, необходимо оценить изменения ЭКГ в отведениях от конечностей. В отведениях I, II, III, aVR, aVL и aVF признаки ИМ выражены не столь отчетливо. В острой фазе ИМ возможен только небольшой подъем сегмента ST в I, а иногда во II и aVL отведениях; зубец Т в этих отведениях положительный. Итак, в указанных отведениях может регистрироваться монофазная деформация сегмента ST, но выраженная в меньшей степени, чем в грудных отведениях.
Отчетливые изменения ЭКГ при инфаркте миокарда (ИМ) передней локализации регистрируются в грудных отведениях. В отведениях V1-V4 или V4-V6, а при обширном ИМ передней локализации в отведениях V1-V6 регистрируются отчетливые признаки ИМ. В зависимости от размера зоны ИМ эти изменения могут быть над всей передней стенкой, т.е. чем больше зона инфаркта, тем больше отведений, в которых имеются характерные изменения.
В грудных отведениях V1-V6 при обширном инфаркте миокарда (ИМ) передней локализации регистрируются значительный подъем сегмента ST и положительный зубец Т (монофазная деформация). Такая монофазная деформация в грудных отведениях является важнейшим диагностическим признаком острого ИМ передней стенки. Поскольку эти отведения располагаются непосредственно над пораженным миокардом, подъем сегмента ST во многих случаях ИМ передней стенки по сравнению с ИМ задней стенки выражен более отчетливо и не может быть пропущен.
При этом исходят из того, что чем меньше времени прошло после развития инфаркта, тем больше подъем сегмента ST и положительный зубец Т. Таким образом, зубец Т положительный и может быть очень высоким. Иногда может регистрироваться асфиксический зубец Т.
Большой зубец Q необязателен, хотя может появиться уже в острой стадии заболевания. Большой зубец Q характеризуется тем, что он очень глубокий или уширен либо сочетает в себе оба этих признака. Зубец R в большинстве случаев маленький или едва различим.
По прошествии острой фазы или при «старом» инфаркте миокарда (ИМ) передней стенки подъем сегмента ST не определяется, но в отведениях I и aVL регистрируется глубокий зубец Q. В этих отведениях зубец Т часто бывает отрицательным. Однако в отведениях от конечностей описанные изменения, как и в случае острой стадии ИМ, бывают выражены не столь отчетливо.
В грудных отведениях характерные признаки «старого» инфаркта миокарда (ИМ), как и «свежего» инфаркта миокарда (ИМ), выражены более отчетливо. Так, в отведениях V1-V4, а при обширном ИМ в отведениях V1-V6 регистрируется уширенный и глубокий зубец Q (признак некроза). Эти изменения зубца Q при инфаркте передней локализации более отчетливые, чем при ИМ нижней локализации.
Особенно характерным для инфаркта миокарда (ИМ) передней локализации является уменьшение амплитуды зубца R, т.е. небольшие зубцы R, которые в норме имеются в отведениях V1-V3, исчезают и появляется комплекс QS. Это важный признак ИМ, бросающийся в глаза. Если зубец Q очень большой, после него иногда может следовать очень маленький зубец R, который, однако, может и полностью отсутствовать. Позднее зубец R может вновь появиться, постепенно увеличиваясь по амплитуде.
Наряду с большим зубцом Q в диагностике «старого» инфаркта миокарда (ИМ) важную роль играет также изменение интервала ST. Так в типичных случаях появляется глубокий остроконечный отрицательный зубец Т (коронарный зубец Т) в отведениях V1-V6. Кроме того, отмечается также депрессия сегмента ST. Чем больше времени прошло после начала ИМ передней локализации, тем меньше глубина отрицательного зубца Т и меньше депрессия сегмента ST в грудных отведениях.
При инфаркте миокарда (ИМ) как передней, так и задней локализации в тяжелых случаях в острой стадии может появиться левопредсердный зубец Р.
Возможны также нарушения ритма сердца в виде синусовой тахикардии, желудочковой экстрасистолии и желудочковой тахикардии.
Особенности ЭКГ при инфаркте миокарда передней стенки:
• Окклюзия левой коронарной артерии или ее ветвей
• Некроз миокарда передней стенки
• В острой стадии: подъем сегмента ST и положительный зубец Т (во всех отведениях V1-V6 или в некоторых из них в зависимости от размеров зоны некроза)
• В хронической стадии: глубокий отрицательный зубец Т и большой зубец Q
• Положительный результат анализа крови на креатинкиназу и тропонины
Учебное видео ЭКГ при инфаркте миокарда
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Инфаркт миокарда
Факторы риска развития ИМ:
Классификация инфаркта миокарда
Клиническая классификация инфаркта миокарда
Клиническая картина инфаркта миокарда
Самым частым и характерным симптомом инфаркта миокарда является боль. В типичных случаях боль имеет разлитой характер, локализуются в левой части грудной клетки, за грудиной. Иногда боль представлена ощущением тяжести, жжения, давления. Чаще всего боль продолжается более 30 минут, не купируется приемом нитроглицерина и обезболивающих препаратов, сопровождается холодным потом, страхом смерти. Часто боли протекают волнообразно, длительно, то ослабевая, то снова усиливаясь.
Атипичные формы инфаркта миокарда
В некоторых случаях симптомы инфаркта миокарда могут носить атипичный характер. Различают следующие формы ИМ:
Все осложнения инфаркта миокарда являются жизнеугрожающими:
Лечение инфаркта миокарда
Единственным методом лечения инфаркта миокарда, который позволяет в значительной части случаев полностью предотвратить негативные последствия, сохранить жизнеспособность сердечной мышцы, является восстановление коронарного кровотока в первые часы после начала заболевания.
Пациенту необходима срочная госпитализация в стационар, способный к немедленному проведению коронароангиографии, балонной ангиопластики и стентированию коронарных артерий.
Восстановление кровотока по коронарным артериям возможно за счет проведения тромболитической терапии (первые 6-12 часов развития инфаркта миокарда), однако этот метод менее эффективен и имеет свои ограничения.
Профилактика инфаркта миокарда
Под профилактикой инфаркта миокарда подразумевают систему мероприятий, основным направлением которых является предупреждение атеросклероза и исключение, по возможности, факторов риска инфаркта миокарда. Целью профилактики после перенесенного инфаркта миокарда является предотвращение летального исхода, развития повторного инфаркта миокарда и хронической сердечной недостаточности.
Первичная профилактика инфаркта миокарда основана на соблюдении «здорового образа жизни», следовании медицинским рекомендациям для предотвращения развития ИБС (поддержание нормального уровня АД, глюкозы, холестерина). Пациент должен соблюдать правильное питание, регулярную физическую активность, отказаться от вредных привычек.
Вторичная профилактика после перенесенного ИМ необходима для предотвращения летального исхода, развития повторного инфаркта миокарда и хронической сердечной недостаточности. Отдаленный прогноз после ИМ определяется тяжестью и распространенностью стенозирующего атеросклероза коронарных артерий; степенью дисфункции левого желудочка, возрастом больного, наличием потенциально опасных аритмий.
После перенесенного ИМ необходим постоянный врачебный контроль для предотвращения развития отдаленных осложнений инфаркта миокарда (хронической сердечной недостаточности, аритмий). Эти осложнения в большинстве случаев успешно предотвращаются при соответствующем рекомендованном врачом режиме, питании и специальном лекарственном лечении. Рекомендуется регулярно посещать врача-кардиолога (по крайней мере 1 раз в 6 месяцев) для контроля общего состояния и оценки степени эффективности проводимой терапии.
Септальный инфаркт миокарда
Что такое инфаркт?
Инфарктом именуют омертвение тканей человеческого организма. Получается, что данное состояние сопровождается отмиранием того или иного участка живой ткани. Если организм человека утрачивает какой-то участок тканей, значит, он не в состоянии осуществлять и какую-то функцию. Из этого можно сделать вывод, что инфаркт миокарда – это утрата не только участка тканей, но еще и функции, которая была на него возложена. Под термином «инфаркт » скрыты многочисленные патологии, сопровождающиеся отмиранием живых тканей человеческого организма. Прочитав данную статью, Вы сможете ознакомиться не только с самой проблемой инфаркта миокарда, но еще и с различными видами данной патологии.
От чего зависит выживание тканей человеческого организма?
Инфаркт – что же это такое?
Выше представленная информация указала нам на то, что инфаркт представляет собой отмирание живых тканей человеческого организма, являющееся следствием резкого нарушения кровообращения, то есть снабжения того или иного участка необходимым количеством кислорода и питательных веществ. Чаще всего, услышав об инфаркте, люди сразу же представляют себе инфаркт сердечной мышцы, то есть заболевание сердечно-сосудистой системы, сопровождающееся отмиранием участка мышцы сердца. На самом деле данное состояние может развиться в любом другом органе:
Причины, способствующие развитию инфаркта
Что происходит при инфаркте?
В случае развития данного состояния отмершая ткань утрачивает все свои функции столь необходимые ей для нормальной работоспособности: выполнение определенной работы, обмен веществ. Так как ту или иную функцию утрачивает определенный участок ткани, вполне возможно, что это скажется на функционировании всего органа в целом. Сила нарушений функционирования органа напрямую зависит от зоны пораженного участка, а также от функциональной значимости органа. При обширном инфаркте вполне возможно развитие как острой сердечной недостаточности. так и инфаркта головного мозга. то есть пожизненное отсутствие той или иной функции. В данном случае больной может утратить как чувствительность, так и речь либо движение.
Что отмечается после инфаркта?
На консультации кардиолога Вы сможете узнать о том, что все виды данного состояния принято считать весьма серьезными и крайне опасными, так как большинство из них очень часто становятся причиной смерти людей. В случае если больному удалось сохранить жизнь, тогда в месте омертвения начинают происходить процессы восстановления, при которых отмершая зона замещается соединительной тканью. Данного рода восстановительные процессы избавляют от анатомического дефекта, однако им не свойственно восстанавливать функции пораженного участка. На самом деле соединительная ткань представляет собой всего лишь наполнитель, которому не свойственно функционировать также как мозгу, сердечной мышце либо другим органам.
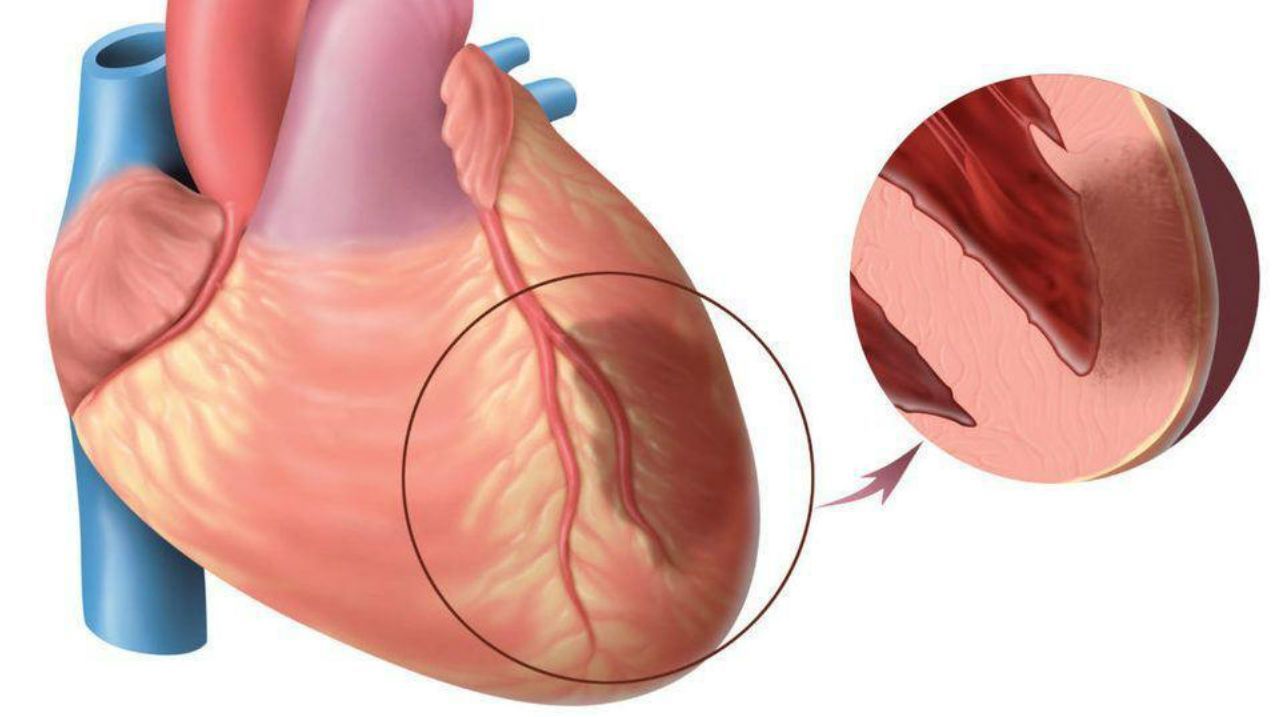
Инфаркт миокарда представляет собой некроз определенного участка мышцы сердца, являющийся следствием нарушения кровообращения в одной из ветвей венечных артерий. Основной причиной развития данного рода нарушения принято считать заболевание под названием атеросклероз, при котором отмечается поражение самых крупных артериальных сосудов человеческого организма.
Несмотря на то, что некроз сердечной мышцы может иметь различное месторасположение, в большинстве случае он наблюдается в левой части сердца, так как именно эта зона подвержена наибольшей нагрузке. Современные врачи-специалисты выделяют:
По типу месторасположения в толще стенки сердца данное состояние подразделяется на:
Перед применением необходимо проконсультироваться со специалистом.
Автор: Пашков М.К. Координатор проекта по контенту.
ЭКГ — диагностика при подозрении на инфаркт миокарда
И. Могельванг, М.Д. Кардиолог отделения интенсивной терапии Госпиталя Хвидовре 1988
Ишемическая болезнь сердца (ИБС)
Основная причина ИБС — обструктивные повреждения главных коронарных артерий и их ветвей.
Прогноз при ИБС определяется:
ЭКГ дает следующую информацию о состоянии миокарда:
Далее ЭКГ дает информацию о:
Информация, которая имеет значение для лечения, контроля и прогнозирования.
1. НОРМАЛЬНАЯ КОРОНАРНАЯ АРТЕРИЯ, ЗДОРОВЫЙ МИОКАРД
2. СУБЭНДОКАРДИНАЛЬНАЯ ИШЕМИЯ
3. ТРАНСМУРАЛЬНАЯ ИШЕМИЯ
Левый желудочек можно разделить на сегменты:
Первые 3 сегмента составляют переднюю стенку, а последние 3 — заднюю стенку. Латеральный сегмент, таким образом может быть вовлечен в инфаркт передней стенки, а также инфаркт задней стенки.
СЕГМЕНТЫ ЛЕВОГО ЖЕЛУДОЧКА
Инфаркт миокарда межжелудочковой перегородки (септальный). Способ визуализации межжелудочковой перегородки при
Изобретение относится к медицине, а именно к кардиологии, и предназначено для определения тактики эндоваскулярного лечения больных обструктивной формой гипертрофической кардиомиопатии. Для этого используют селективное введение в септальную ветвь передней нисходящей артерии физиологического раствора (NaCl 0,9%), насыщенного микропузырьками воздуха. Данный способ визуализации позволяет ввести этиловый спирт в септальные артерии, кровоснабжающие именно ту часть межжелудочковой перегородки, которая вызывает обструкцию в выходном отделе левого желудочка, что позволяет улучшить непосредственные и отдаленные результаты спиртовой аблации межжелудочковой перегородки. 6 ил.
Предлагаемое техническое решение относится к медицине, а именно к кардиологии, и предназначено для определения тактики эндоваскулярного лечения больных обструктивной формой гипертрофической кардиомиопатии.
Гипертрофическая кардиомиопатия (ГКМП) — одна из основных и, вероятно, наиболее распространенных форм кардиомиопатии, заболеваний миокарда, сопровождающихся его дисфункцией [1]. В последнее время можно говорить о значительной эволюции знаний в вопросах изучения проблемы ГКМП, этиологии, патогенеза, диагностики, клинического течения и прогноза, вариантов лечения заболевания. За полувековой период только в англоязычных изданиях опубликованы более 1000 крупных научных работ. Созданный в 2003 г. Международный комитет (ACC/ESC) объединил американских и европейских экспертов по ГКМП и опубликовал сообщение, суммировавшие основные положения, включая стратегию лечебных мероприятий [2]. По современным представлениям ГКМП является преимущественно генетически обусловленным заболеванием мышцы сердца, характеризующимся комплексом специфических морфофункциональных изменений и неуклонно прогрессирующим течением с высокой угрозой развития тяжелых жизнеугрожающих аритмий и внезапной смерти (ВС). ГКМП характеризуется массивной (более 1.5 см) гипертрофией миокарда левого и/или в редких случаях правого желудочка, чаще ассиметричного характера за счет утолщения межжелудочковой перегородки (МЖП) с частым развитием обструкции (систолического градиента давления) выходного тракта левого желудочка (ЛЖ) при отсутствии известных причин (артериальная гипертензия, пороки и специфические заболевания сердца). Основным методом диагностики остается эхокардиографическое исследование. Характерно гиперконтрактильное состояние миокарда при нормальной или уменьшенной полости ЛЖ вплоть до ее облитерации в систолу. При наличии градиента систолического давления в выходном отделе левого желудочка говорят об обструктивной форме ГКМП. При этом различают три гемодинамических варианта обструкции: с субаортальной обструкцией в покое (так называемой базальной обструкцией); с лабильной обструкцией, характеризующейся значительными спонтанными колебаниями внутрижелудочкового градиента давления без видимой причины; с латентной обструкцией, которая вызывается только при нагрузке и провокационных фармакологических пробах (в частности, вдыханием амилнитрита, при приеме нитратов или внутривенным введении изопротеренола).
В настоящее время наблюдается повсеместный рост числа зарегистрированных случаев этой патологии как за счет внедрения в практику современных методов диагностики, так и, вероятно, в связи с истинным увеличением числа больных ГКМП [3]. Согласно данным последних исследований распространенность заболевания в общей популяции является более высокой, чем считалось ранее, и составляет 0.2% [4]. ГКМП может диагностироваться в любом возрасте от первых дней до последней декады жизни независимо от пола и расовой принадлежности, однако преимущественно заболевание выявляется у лиц молодого трудоспособного возраста [5]. Ежегодная смертность больных ГКМП колеблется в пределах от 1 до 6% [6].
В настоящее время стали активно развиваться эндоваскулярные методы лечения обструктивной ГКПМ с использованием катетерных методик — спиртовая аблация межжелудочковой перегородки, проводимая путем введения в септальную ветвь передней нисходящей коронарной артерии 1-1,5 мл этилового спирта. Введение спирта вызывает локальный некроз миокарда, ограниченный зоной кровоснабжения септальной ветви, вследствие чего возникает гипо- и акинез части межжелудочковой перегородки с последующим ее истончением и в результате — снижением градиента артериального давления в выходном отделе левого желудочка (ВОЛЖ). Во время вмешательства необходимо проводить эхокардиографическое исследование с целью оценки результата введения спирта. С помощью ультразвукового исследования оценивается состояние межжелудочковой перегородки. Однако после этого не всегда удается добиться снижения градиента артериального давления, т.к. в некоторых случаях кровоснабжение базальной части межжелудочковой перегородки осуществляется также из второй или третьей септальных ветвей и в ряде случаев идентификация целевой септальной ветви оказывается затруднительной.
Целью предлагаемого способа ультразвуковой визуализации межжелудочковой перегородки является увеличение эффективности эндоваскулярных вмешательств при лечении обструктивной ГКМП, а именно определение источника кровоснабжения части межжелудочковой перегородки, вызывающей обструкцию в выходном отделе левого желудочка. Поставленная цель достигается тем, что для улучшения ультразвуковой визуализации используют селективное введение в септальную ветвь передней нисходящей артерии физиологического раствора (NaCl 0,9%), насыщенного микропузырьками воздуха. Введение выполняется через внутренний просвет баллонного катетера.
Способ осуществляется следующим образом.
Введение раствора осуществляют через двупросветный баллонный катетер в коронарное русло путем пункции бедренной артерии под рентгеновским контролем. Баллон-катетер проводят в первую септальную ветвь передней нисходящий артерии по специальному коронарному проводнику, проводят раздутие баллона до диаметра септальной артерии с целью полного перекрытия ее просвета. Состав раствора: в одном шприце — 9 мл 0.9% физиологического раствора натрия хлорида, во втором 1 мл стерильного воздуха. Шприцы фиксируют к тройнику, который соединен с баллоном-катетером через короткую полимерную трубку. В шприц с физиологическим раствором осуществляют забор 0.5 мл крови пациента. При помощи поршней содержимое двух шприцев смешивают до образования раствора с видимыми микропузырьками воздуха и наполняют им один из шприцев. Затем его содержимое болюсно вводят через внутренний просвет баллонного катетера в септальную артерию, кровоснабжаюшую межжелудочковую перегородку, и одновременно выполняют трансторакальную эхокардиоскопию, регистрируя микроэмболические сигналы. В результате введения раствора улучшается ультразвуковая визуализация, что дает возможность определить локализацию части межжелудочковой перегородки, вызывающей обструкцию в выходном отделе левого желудочка (ВОЛЖ). Далее через внутренний просвет баллонного катетера в септальную артерию вводят 1-1,5 мл этилового спирта, что позволяет устранить обструкцию, препятствующую оттоку крови из левого желудочка. Далее баллонный катетер и проводник удаляют, записывают прямое давление на выведении катетера из полости левого желудочка в аорту и затем завершают основной этап операции.
При необходимости вышеописанную процедуру проводят с септальными ветвями передней нисходящий артерии второго и третьего порядка, что позволяет провести наиболее полное устранение обструкции в межжелудочковой перегородке.
Данный способ визуализации позволяет ввести этиловый спирт в септальные артерии, кровоснабжающие именно ту часть межжелудочковой перегородки, которая вызывает обструкцию в выходном отделе левого желудочка, что позволяет улучшить непосредственные и отдаленные результаты спиртовой аблации межжелудочковой перегородки.
Пример практического использования метода продемонстрирован на пациенте.
Больная Т. 53 г. № истории болезни 801. Диагноз: Гипертрофическая кардиомиопатия, обструктивный вариант. Исходно: выраженная гипертрофия МЖП (2.5 см), систолическое давление в полости ЛЖ резко повышено, систолический градиент на уровне ВОЛЖ составил 99 мм рт.ст. (Фиг.1). Первым этапом выполнялась эхографическое исследование с использованием физиологического раствора, насыщенного микропузырьками воздуха (Фиг.2). Во время процедуры в первую септальную ветвь был введен 1 мл спирта (Фиг.3, 4, 5). После спиртовой редукции первой септальной ветви передней нисходящей артерии систолическое давление в полости ЛЖ снизилось на 128 мм рт.ст. остаточный систолический градиент на уровне ВОЛЖ составил 19-22 мм рт.ст.
Данный метод позволил удостовериться в соответствии зоны кровоснабжения первой септальной ветви области гипертрофированной части ВОЛЖ, что в свою очередь позволило провести процедуру спиртовой аблации с высокой эффективностью.
Данный клинический случай имеет отдаленный результат наблюдения. Спустя 10 месяцев был выполнен ЭХОКГ контроль, во время процедуры исследования было выявлено истончение зоны МЖП в выходном отделе ЛЖ (Фиг.6). Градиент давления на уровне ВОЛЖ составил 20 мм рт.ст.
Предлагаемое техническое решение дает возможность воспроизведения объекта техническими средствами и направлено на сохранение и укрепление здоровья пациента. При этом подтверждена возможность его практической реализации и указан конкретный путь решения поставленной задачи. Ультразвуковое исследование межжелудочковой перегородки с использованием физиологического раствора, насыщенного микропузырьками воздуха при введении в септальные ветви, осуществляется на эхокардиграфическом аппарате типа «Акусон»-128 ХР (Акусон корпорейшен, США), регистрационный номер 92-38.
Новизна предлагаемого способа состоит в том, что впервые для улучшения визуализации МЖП используют введение в септальные ветви физиологического раствора, насыщенного микропузырьками воздуха, и одновременно осуществляют эхокардиографическое исследование МЖП.
В отличие от применяющегося в настоящее время эхокардиографического исследования МЖП без ее «маркировки» данный способ обеспечивает улучшение непосредственных и отдаленных результатов эндоваскулярного лечения обструктивной ГКМП, так как позволяет выявить все септальные ветви, кровоснабжающие гипертофированную часть МЖП.
Предлагаемое техническое решение на данном этапе развития кардиологии применимо практически, а его различие с известным решением — прототипом позволяет изменить его свойство, результатом чего является его эффективность.
Изобретательский уровень предлагаемого способа состоит в использовании для улучшения ультразвуковой визуализации селективного введения в септальные ветви физиологического раствора, насыщенного микропузырьками воздуха. Его применение позволит повысить эффективность снижения градиента давления в выходном отделе левого желудочка. Простота практической реализации и безопасность метода свидетельствует о его преимуществах перед известным прототипом. Все эти достоинства позволяют повысить эффект от проводимой терапии, возвратить утраченную трудоспособность, снизить затраты на лечение.
Предлагаемый способ может иметь большую клиническую значимость.
1. Report of the 1995 WHO/ISFC Task Force on the Definition and Classification of Cardiomyopathies. Circulation. 1996; 93: 841-2.
2. A Report of the American Collage of Cardiology Foundation Task Force on Clinical Expert Consensus Documents and the European Society of Cardiology Committee for Practice Guidelines. Eur Heart J 2003; 24: 1965-91.
3. Maron BJ. Hypertrophic cardiomyopathy. Lancet 1997; 350: 127-33.
4. Maron BJ, Gardin JM, Flack JM et al. Circulation 1995; 92: 785-9.
5. Maron BJ, Casey SA, Poliac LC et al. JAMA 1999; 281: 650-5.
6. Maron BJ, Roberts WC, Epstein SE. Circulation 1982; 65: 1388-94.
7. Merril WH, Friesinger GC, Graham TPJr et al. Ann Thorac Surg 2000; 69: 1732-5.
8. Theodore DA, Danielson GK, Feldt RH, Anderson BJ. J Thorac Cardiovasc Surg 1996; 112: 1589-97.
9. Schulte HD, Borisov К, Gams E et al. J Thorac Cardiovasc Surg 1999; 47: 213.
10. A Report of the American Collage of Cardiology Foundation Task Force on Clinical Expert Consensus Documents and the European Society of Cardiology Committee for Practice Guidelines. Eur Heart J 2003; 24: 1965-91.
Способ визуализации межжелудочковой перегородки при выполнении операции спиртовой аблации септальной артерии, включающий эхокардиографическое исследование межжелудочковой перегородки, отличающийся тем, что после предварительных этапов операции по коронарному проводнику в первую септальную ветвь проводят двухпросветный баллонный катетер, баллон расправляют давлением до перекрытия просвета септальной ветви, далее берут один шприц с 0,9%-ным физиологическим раствором натрия хлорида и второй шприц с объемом стерильного воздуха, шприцы фиксируют к тройнику, который соединен с баллон-катетером через короткую полимерную трубку, в шприц с физиологическим раствором набирают 0,5 мл крови пациента, при помощи поршней содержимое двух шприцев смешивают до образования раствора с видимыми микропузырьками воздуха и наполняют им один из шприцев, затем его содержимое болюсно вводят через внутренний просвет баллонного катетера в септальную артерию, кровоснабжающую межжелудочковую перегородку, и одновременно выполняют трансторакальную эхокардиоскопию, регистрируя микроэмболические сигналы, затем после подтверждения зоны интереса путем регистрации сигналов от введенного физиологического раствора, насыщенного микропузырьками воздуха, на фоне общего внутривенного наркоза в первую септальную ветвь вводят 1 мл 95% этанола, при необходимости вышеописанную процедуру проводят с септальными ветвями передней нисходящей артерии второго и третьего порядка, что позволяет провести наиболее полное устранение обструкции в межжелудочковой перегородке, далее баллонный катетер и проводник удаляют, записывают прямое давление на выведение катетера из полости левого желудочка в аорту и затем завершают основной этап операции.