ингибиторы ароматазы что это такое
Ингибиторы ароматазы что это такое
Ингибиторы ароматазы снижают уровень эстрогенов за счет инактивирования ароматазы — фермента, ответственного за синтез эстрогенов из андрогенов. В противоположность тамоксифену эти препараты не обладают свойствами частичного агониста.
В исследовании монотерапии анастрозолом, тамоксифеном или сочетанной терапии сравнивалась эффективность 5-летнего лечения тамоксифеном, анастрозолом и комбинации этих препаратов.
Выявлено, что при применении анастрозола значительно лучше выживаемость, длительнее ремиссия, ниже показатели отдаленных метастазов и более низкая вероятность контралатерального рака молочной железы (РМЖ) по сравнению с тамоксифеном.
Летрозол, другой ингибитор ароматазы, сравнивался с тамоксифеном в многоцентровом исследовании Breast International Group, включившем 8028 женщин в менопаузе с метастатическим раком молочной железы (РМЖ).
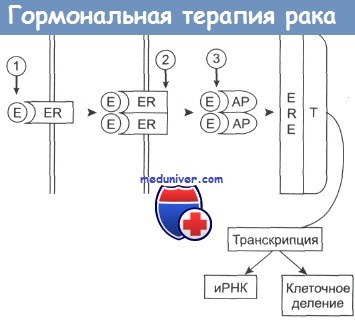
Комплекс приобретает активность (АР) и присоединяется к эстроген-зависимым структурам (ERE) клеточного ядра.
Происходит активация таких белков, участвующих в транскрипции (Т), как РНК-полимераза II, что приводит к синтезу белка и делению клетки.
Гозерелин вызывает снижение уровня эстрогенов в плазме крови (1); фульвестран (2) предотвращает процесс димеризации рецептора и его активацию; тамоксифен (3) связывается с активным комплексом, подавляя его способность инициировать транскрипцию.
Летрозол значительно снизил риск рецидива по сравнению с тамоксифеном, особенно в удаленных участках тела. В другом международном исследовании, которое включало 5187 женщин, летрозол назначали после 5-летнего применения тамоксифена. Результаты показали снижение риска рецидива рака молочной железы (РМЖ) практически на 50 %.
Таким образом, летрозол в настоящее время считается признанным препаратом выбора для тех больных в постменопаузе с ЭР-положительным раком молочной железы (РМЖ), которые принимали тамоксифен на протяжении 5 лет.
The American Society of Clinical Oncology рекомендует использовать ингибиторы ароматазы для снижения риска рецидива рецептор-положительного РМЖ в постменопаузе в качестве начальной терапии или после лечения тамоксифеном. Длительность терапии в настоящее время не определена.
Было проведено несколько исследований химиогормональной терапии у больных раком молочной железы (РМЖ). Многие из этих исследований включали пациенток как с поражением лимфоузлов, так и без него. The Eastern Cooperative Oncology Group провела исследование III фазы, включившее женщин в пременопаузе с наличием метастазов в лимфоузлах, при рецептор-положительном раке молочной железы (РМЖ).
В исследование вошло 1504 пациентки, рандомизированных на следующие группы: получавшие лечение циклофосфамидом, доксорубицином и 5-фторурацилом (CAF); CAF + гозерелин (агонист лютеинизирующего рилизинг-гормона) на протяжение 5 лет; CAF + гозерелин + тамоксифен в течение 5 лет. Добавление тамоксифена улучшало 5-летнюю безрецидивную выживаемость, но добавление гозерелина не превосходило по эффективности применения только схемы CAF. 5-летняя выживаемость была сходной во всех трех группах (85 и 86 %).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Ингибиторы ароматазы в лечении рака молочной железы
Рак молочной железы (РМЖ) — наиболее частая опухоль у женщин, ежегодно в мире регистрируется 1 млн 150 тыс. новых случаев инвазивного РМЖ, а 450 тыс. женщин погибают от этого заболевания. Программы маммографического скрининга и определенные успехи новых терапевтических подходов являются главными факторами, объясняющими высокую распространенность этого заболевания.
Лечение больных гормоночувствительным операбельным РМЖ обычно начинается с хирургического вмешательства, дополняемого при необходимости лучевой терапией с последующей многолетней эндокринотерапией. Уже доказано, что применение послеоперационной (адъювантной) эндокринотерапии препаратом тамоксифен снижает риск рецидива заболевания, увеличивая показатели общей выживаемости. Дополнительно к эндокринотерапии адъювантное лечение может включать первичную химиотерапию, которая также может улучшить отдаленные результаты.
Среди многообразия факторов, вовлеченных в канцерогенез и определяющих терапевтические мишени при этих опухолях, эстрогены и рецепторы к ним (ER) можно отнести к наиболее подходящим признакам, имеющим прогностическое и предсказывающее значение. Доказано, что длительная экспозиция к эстрогенам и высокие уровни плазменных эстрогенов коррелируют с нарастающим риском возникновения РМЖ. Точно так же выявлено увеличение экспрессии ER при сравнении нормального эпителия протоков молочной железы, гиперплазии эпителия и протоковой карциномы in situ. Поэтому антагонистическое противостояние эстрогенам представляется логичным подходом к терапии и профилактике РМЖ.
Задолго до открытия гормонов и рецепторов к ним, 110 лет назад, шотландский хирург Beatson обнаружил, что овариэктомия вызывает иногда регрессию распространенного РМЖ. С этого времени основные терапевтические исследования стали фокусироваться на попытках устранения или максимального подавления периферических эстрогенов или на целенаправленном воздействии на ER и рецепторы прогестерона (PR) как основную мишень гормонозависимого РМЖ.
В течение почти четырех десятилетий селективный модулятор ER — тамоксифен — являлся основным препаратом эндокринотерапии ER+РМЖ. Оксфордский обзор группы EBCTG, куда входит и НИИ онкологии им. Н.Н.Петрова, продемонстрировал, что тамоксифен улучшает показатели безрецидивной и общей выживаемости у больных с потенциально гормонально-чувствительными (т.е. ER+ и/или PR+) опухолями. В противоположность этому больные с ER-отрицательными опухолями или низким уровнем экспрессии рецепторов стероидных гормонов не имели пользы от гормональных воздействий.
Тамоксифен в целом хорошо переносится больными, но иногда способен вызывать опасные, угрожающие жизни эффекты из-за его частичной активности в качестве агониста эстрогенов. С этим связано увеличение риска возникновения рака эндометрия, тромбоэмболических событий, осложнений, учащающихся при многолетнем применении препарата.
Такие наблюдения привели к поиску новых гормональных препаратов с более безопасными терапевтическими параметрами. Среди них оказались ингибиторы ароматазы (ИА). Первое поколение ИА, использовавшихся для лечения метастатических форм РМЖ, не достигло адъювантного применения из-за неблагоприятного «терапевтического индекса» (польза — вред) по сравнению с тамоксифеном.
Механизм действия
ИА блокируют цитохром Р450 — фермент ароматазы, отвечающий за превращение андрогенов в эстрогены, тем самым снижая уровень эстрогенов. В постменопаузе эстрогены синтезируются в надпочечниках, коже, мышцах и в жировой ткани. Кроме того, большинство опухолей молочной железы обладают ароматазной активностью, являясь источником локальных эстрогенов для опухолевых клеток.
В противоположность этому у пременопаузальных женщин ИА индуцируют секрецию гонадотропных гормонов гипофиза через механизм обратной связи, приводя к овариальной стимуляции и развитию овариальных кист. Поэтому применение ИА у женщин с сохраненной менструальной функцией противопоказано.
Существуют два типа ИА. Ингибиторы I типа являются аналогами андрогенов, необратимо инактивируют ароматазу, вступая в ковалентную связь с энзимным протеином. По этой причине их называют инактиваторами ароматазы. Среди них препарат экземестан является наиболее изученным в клинике средством. Ингибиторы II типа — это нестероидные агенты с обратимой связью с активным сайтом ароматазы. Среди них в клинике представлены анастразол и летрозол.
Ингибиторы ароматазы в 1-й линии лечения метастатического РМЖ
Превосходство ИА III поколения над мегестрол-ацетатом во 2-й линии лечения распространенного РМЖ легло в основу решения о замене тамоксифена в 1-й линии лечения метастатического (ER+) РМЖ.
Два крупных рандомизированных клинических испытания показали, что анастразол достоверно улучшает время до прогрессирования (ТТР) в сравнении с тамоксифеном у постменопаузальных женщин с ER+ распространенным РМЖ (10,7 мес против 6,4 мес). Последующий комбинированный анализ также показал, что анастразол оказался, по крайней мере, столь же эффективным, как тамоксифен, при оценке показателей общей выживаемости. Переносимость анастразола была лучше, чем тамоксифена, с меньшей частотой тромбоэмболий и вагинальных (маточных) кровотечений.
В крупном рандомизированном двойном слепом исследовании летрозол превосходил тамоксифен у постменопаузальных больных с ER+ распространенными опухолями по частоте объективных ответов и ТТР (9,4 мес против 5 мес). Толерабельность летрозола была также более благоприятная в сравнении с тамоксифеном, с меньшей частотой тромбоэмболических «событий».
В третьем исследовании III фазы экземестан показал заметное преимущество над тамоксифеном по частоте объективных ответов на лечение, клиническому благополучию и ТТР (10 мес против 6 мес). Профиль безопасности был благоприятнее при лечении экземестаном с меньшей частотой приливов. Высказано также предположение, что экземестан в отличие от нестероидных ИА (летрозол, анастразол) не оказывает столь неблагоприятного воздействия на костный и липидный метаболизм.
Ингибиторы ароматазы в адъювантном лечении РМЖ
Оксфордский мета-анализ установил, что до появления ИА адъювантное лечение тамоксифеном в течение 5 лет при ER+ опухолях снижает ежегодные показатели смертности от РМЖ на 31% (безотносительно возраста пациента, экспрессии рецепторов прогестерона и применявшейся ранее химиотерапии). Пятилетнее лечение тамоксифеном считалось оптимальным и более эффективным, чем более продолжительное лечение, что впоследствии не подтвердилось программами ATLAS и ATTOM, включавшими свыше 20 тыс. больных РМЖ. В абсолютном исчислении 10-летнее адъювантное лечение тамоксифеном увеличивает показатели 10-летней выживаемости на 3% по сравнению с 5-летним лечением.
Было установлено, что риск рецидива заболевания при ER+ опухолях является высоким на протяжении первых 5 лет после установления диагноза РМЖ, особенно высокий риск падает на 2-й и 3-й годы независимо от статуса лимфатических узлов. Именно риск ранних рецидивов, по мнению ряда авторов, оправдывает раннее назначение ИА.
В то же время при ER+ опухолях показатели смертности от РМЖ схожи во временных отрезках: 0—4 года и 5—14 лет с кумуляцией 2/3 смертельных исходов между 5-м и 15-м годами. Это наблюдение свидетельствует о потенциальной пользе «продолженной» адъювантной эндокринотерапии свыше 5 лет.
Кроме того, для более полной оценки реального вклада адъювантного эндокринного лечения необходимо изучение и показателей общей выживаемости после длительного периода наблюдения, порядка от 8 до 15 лет.
Предложены четыре стратегии изучения ИА III поколения в адъювантном лечении РМЖ: первичная (Up-front), последовательная (Sequence), переключающаяся (Switching) и продолженная (Extended) эндокринотерапия.
Первичная стратегия
Представляется чрезвычайно важным, чтобы женщины получили наиболее эффективную адъювантную терапию с целью минимизировать ранний риск рецидива РМЖ. Несколько клинических испытаний сравнили ИА с тамоксифеном, назначаемые на 5 лет (анастразол в испытании АТАС, летрозол в BIG 1-98, экземестан в TEAM).
Испытание АТАС — крупное международное исследование (9366 больных РМЖ), показавшее при первом анализе (при среднем периоде наблюдения 33 мес), что анастразол значительно увеличивает безрецидивную выживаемость, время до прогрессирования и уменьшает частоту контрлатеральных РМЖ по сравнению с тамоксифеном. Однако комбинированная терапия (анастразол + тамоксифен) не имела преимуществ по сравнению с одним тамоксифеном и поэтому была прекращена. Последний анализ при среднем периоде наблюдения 100 мес подтвердил, что у больных с рецептор-положительными опухолями 5-летнее лечение анастразолом достоверно улучшает показатели безрецидивной выживаемости на 15%. Оценка главной цели испытания — TTR показала 24%-ное сокращение риска рецидива РМЖ в пользу анастразола в сравнении с тамоксифеном. Абсолютные отличия в показателях TTR к 9 годам наблюдения равнялись 4,8%, что подтверждает значимый «переносящийся» (carry-over) эффект анастразола, сохраняющийся после окончания лечения, в сравнении с тамоксифеном (абсолютные отличия TTR к 5 года равнялись 2,8%). Кроме того, анастразол вызывал 40%-ное сокращение риска контрлатерального РМЖ с 16%-ным сокращением риска развития отдаленных метастазов.
Испытание BIG 1-98 (Breast International group) — единственное двойное слепое плацебоконтролируемое исследование — включает четыре ветви, хотя первоначально планировалось сравнить летрозол (ветвь А) с тамоксифеном (ветвь В), назначаемые на 5 лет у постменопаузальных женщин с ER+ и/или PR+РМЖ. Позже это испытание было изменено с дополнительным включением двух других групп, в которых пациенты получали последовательно сначала 2 года тамоксифен, а затем 3 года летрозол (ветвь С), или 2 года летрозол, а затем тамоксифен (ветвь D). Восемь тысяч постменопаузальных женщин были рандомизированы в группы А, B, C, D. Первичный промежуточный анализ этого испытания, включавший 4922 пациента (2463 — на летрозоле и 2459 — на тамоксифене), был опубликован при достижении периода наблюдения 51 мес. Безрецидивная выживаемость оказалась лучше при лечении летрозолом по сравнению с тамоксифеном, безотносительно уровня экспрессии PR, с относительным сокращением риска рецидива до 18%. TTR была значительно улучшена при терапии летрозолом, с абсолютным отличием в 3,2% к 5 годам. Как и следовало ожидать, при относительно коротком периоде наблюдения не было достоверных отличий в показателях общей выживаемости. Однако время до возникновения отдаленных метастазов опухоли оказалось достоверно продолжительнее при лечении летрозолом.
Последовательная стратегия
Переключающая стратегия
Переключающую стратегию нередко путают с последовательной стратегией. Отличие между двумя подходами заключается в том, что «переключающие» испытания исключают пациентов с рецидивом опухоли в первые 2—3 года терапии тамоксифеном, отбирая субпопуляцию пациентов с более высокой эндокринной чувствительностью (пациенты с ранним рецидивом должны быть менее чувствительны к гормонотерапии). «Последовательные» испытания включают всех пациентов от начала адъювантной терапии, включая больных с рецидивом на тамоксифене в первые 2—3 года лечения. Поэтому представляется обманчивым использовать данные и результаты «переключающих» испытаний с целью достичь определенного заключения о последовательной стратегии адъювантной эндокринотерапии.
Испытание IES представляет собой двойное слепое рандомизированное исследование, оценивающее, является ли переключение на экземестан после 2—3 лет терапии тамоксифеном более эффективным, чем продолжение лечение тамоксифеном до 5 лет. Общая продолжительность гормонотерапии была одинаковой в обеих группах (5 лет), а среднее время лечения тамоксифеном до рандомизации равнялось 2,4 года. После среднего периода наблюдения за 4724 больными опубликован анализ этого испытания. Безрецидивная выживаемость в популяции с ER+ и ER-неизвестным статусом оказалась достоверно лучше при переключении на экземестан против продолжения лечения тамоксифеном, при абсолютном улучшении в 3,5% к 5 году. Время до возникновения отдаленных метастазов также оказалось более благоприятным для экземестана, с достоверным улучшением общей выживаемости. Кроме того, снижалась частота контрлатерального РМЖ в группе с экземестаном на 44% по сравнению с терапией тамоксифеном.
Испытание ITA – открытое исследование III фазы, сравнивающее 5-летнее лечение тамоксифеном с 2—3-летним лечением также тамоксифеном с переключением на анастразол на 2—3 года (общая продолжительность лечения в обеих группах 5 лет). После включения в исследование 448 больных выявлено значительное преимущество анастразола над тамоксифеном в показателях выживаемости без «событий». Однако многообещающие результаты в этом испытании нуждаются в подтверждении в более крупных испытаниях, таких как Австрийское исследование.
Результаты комбинированного Австрийского исследования АBCSG8/ARNO 95 были представлены после включения 3224 больных при среднем периоде наблюдения 28 мес. Оказалось, что переключение на анастразол пролонгирует и увеличивает «бессобытийную» выживаемость по сравнению с продолжающимся до 5 лет лечением тамоксифеном. Безметастатическая выживаемость также улучшалась с переключением на анастразол, улучшалась и общая выживаемость.
Продолженная стратегия
Продолжительность адъювантной гормонотерапии — старый вопрос, но остается фундаментальной загадкой для будущих решений. Результаты Оксфордского анализа EBCTG показали ясно, что 5-летняя адъювантная терапия тамоксифеном лучше, чем более короткая. Промежуточный анализ проектов ATLAS и ATTOM продемонстрировал улучшение показателей выживаемости на 3—5% при десятилетнем лечении тамоксифеном по сравнению со стандартным 5-летним лечением.
Учитывая, что адъювантный тамоксифен вызывает так называемый переносящий эффект до 10 лет, даже когда терапия прекращается рано, и тот факт, что у многих больных с эндокриночувствительными опухолями рецидив заболевания возникает через длительные сроки (5—15 лет), ИА считаются хорошими кандидатами для оптимизации продолжительной эндокринотерапии, сохраняя при этом преимущества последовательной стратегии. Эти соображения привели к проведению двух клинических испытаний, оценивавших роль включения ИА после 5 лет адъювантного лечения тамоксифеном: одно с применением летрозола — в Национальном онкологическом институте Канады (MA 17), другое с подключением анастразола (Австрийский проект ABCSG 6а). Третье испытание, предусматривающее применение экземестана (NSABP В-ЗЗ), было закрыто после публикации результатов исследования MA 17.
В испытании MA 17 были рандомизированы 5187 постменопаузальных больных, получавших летрозол в сравнении с плацебо после почти 5-летнего адъювантного лечения тамоксифеном. Испытание было закрыто досрочно после первого запланированного промежуточного анализа при среднем периоде наблюдения 2,4 года. Показатель 4-летней безрецидивной выживаемости достиг 93% у получавших летрозол против 87% — у получавших плацебо. Иными словами, риск рецидива заболевания благодаря продолженному лечению летрозолом сокращался на 43%. Однако к этому периоду наблюдения еще не отмечались достоверные отличия показателей 4-летней общей выживаемости. Несмотря на тот факт, что большинство больных не завершили полный курс предписанной терапии летрозолом, исследование было досрочно прервано, а коды на пациентов открыты. Дальнейший анализ со слегка более длительным средним периодом наблюдения (30 мес) подтвердил улучшение показателя безрецидивной выживаемости с 40%-ным сокращением риска появления отдаленных метастазов в группе принимавших летрозол и достоверным улучшением общей выживаемости у больных с метастазами в регионарных лимфатических узлах.
В Австрийском испытании ADCSG 6а изучалась роль одного анастразола в течение 3 лет против контроля (без гормонального лечения) после 5-летнего лечения тамоксифеном в комбинации (или без) с аминоглютетимидом. После среднего периода наблюдения 60 мес за 856 больными риск рецидива заболевания достоверно снизился у получавших анастразол в сравнении с контролем (без терапии), риск развития отдаленных метастазов снизился на 47%, но не выявлено влияние на показатели общей выживаемости.
Токсический профиль ингибиторов ароматазы в адъювантном лечении
В целом анастразол при 5-летней терапии представляется менее токсичным, чем тамоксифен при общем анализе серьезных побочных событий. Предварительные результаты испытания BIG 1-98 при 55-месячном среднем периоде наблюдения не свидетельствуют о достоверных отличиях между летрозолом и тамоксифеном по частоте серьезных неблагоприятных событий; однако необходим более длительный период наблюдения для точного установления финального профиля безопасности летрозола при терапии, превышающей 5 лет.
Одна серия побочных эффектов специфична и благоприятна для ИА (реже приливы, гинекологические побочные эффекты и сердечно-сосудистые события, включая тромбоэмболию), вторая серия «событий» специфична для всех ИА, но благоприятна для тамоксифена (реже артралгия, остеопороз/переломы) и третья серия событий более специфична для конкретных ИА (липидный обмен, кардиальные и цереброваскулярные «события»).
Заключение
ИА III поколения являются сейчас неотъемлемой частью гормонотерапии постменопаузальных женщин с эндокриночувствительным РМЖ. Недавние результаты клинических исследований показывают преимущество этих препаратов над тамоксифеном. Однако наилучшие и оптимальные терапевтические стратегии адъювантного применения ИА пока не определены, особенно в отношении «последовательной» эндокринотерапии и продолжительности терапии свыше 5 лет.
Общий терапевтический индекс ИА выше, чем при лечении тамоксифеном с доказанным улучшением эффективности и более безопасным профилем токсичности.
Эндокринная терапия (гормонотерапия) при раке молочной железы
Это метод лечения с применением гормональных и антигормональных препаратов. Цель гормонотерапии – устранить воздействие на опухоль гормонов (эстрогенов), к которым она чувствительна. Добиться этого можно разными способами: снижением уровня эстрогенов, образующихся в яичниках (путем удаления яичников или выключения их функции с помощью лекарств) или блокадой рецепторов к эстрогенам и прогестерону.
Существует неоадъювантная (проводится перед оперативным лечением) и адъювантная (дополнительная) гормонотерапия.
Приблизительно у 2/3 пациенток рак молочной железы является гормонозависимой опухолью. Раковые клетки содержат рецепторы, с которыми связываются эстрогены, стимулирующие рост опухоли.
Эстрогены – женские половые гормоны. Они вырабатываются яичниками, которые в свою очередь контролируются гормонами гипофиза. Чтобы исключить влияние эстрогенов на клетки рака молочной железы, применяют антиэстрогены или ингибиторы ароматазы.
Антиэстроген – основное достижение гормонотерапии 70–80 гг. XX в. В течение 30 лет они занимали лидирующее положение в лечении рака молочной железы и используются до сих пор. Антиэстрогены блокируют рецепторы эстрогенов и препятствуют их связыванию с эстрогенами.
У молодых женщин снизить содержание эстрогенов можно путем удаления яичников (овариоэктомия) либо с помощью их облучения. В последнее время все чаще используются методы медикаментозного подавления функции яичников с помощью препаратов, которые имитируют действие гормонов гипофиза и в определенных дозах угнетают функцию яичников.
У женщин в период менопаузы источниками эстрогенов являются не яичники, а надпочечники и жировая ткань. В этом случае с успехом используют ингибиторы ароматазы.
Введение в практику ингибиторов ароматазы – достижение конца 90 годов прошлого века и начала нашего. К настоящему времени хорошо изучены их возможности как в плане послеоперационной химиотерапии, так и в лечении больных с диссеминированным (метастатическим) опухолевым процессом.
Ингибиторы ароматазы препятствуют реакции ароматизации, которая превращает надпочечниковые андрогены в эстрогены.
Многолетние мультицентровые международные исследования, включающие тысячи пациентов, показали, что у женщин в менопаузе с рецепторположительным операбельным раком молочной железы адъювантное (после основного лечения) использование ингибиторов ароматазы снижает риск рецидива заболевания.
Безусловно, вопрос о выборе гормонотерапии решается индивидуально с учетом всех особенностей течения заболевания. Важное значение при этом имеют данные о наличии рецепторов гормонов в опухоли.
Определить степень гормоночувствительности рака молочной железы помогает иммуногистохимическое исследование опухоли. Оно выполняется в специализированной лаборатории сразу после операции или через некоторое время, если доступны парафиновые блоки удаленной опухоли. Обнаружение этих рецепторов в опухолевых клетках указывает на перспективность гормонотерапии и, как правило, является благоприятным прогнозом на будущее.
В некоторых случаях врач вынужден назначать лечение, не имея рецепторной характеристики опухоли, ориентируясь только на клинические данные. При этом должны учитываться и возможные побочные эффекты гормонотерапии: для антиэстрогенов – возможность гиперплазии эндометрия, повышение риска рака эндометрия и тромбоэмболических осложнений, для ингибиторов ароматазы – усиление признаков остеопороза, характерных для женщин в период менопаузы.
Но регулярное врачебное наблюдение, адекватное применение лекарственных препаратов, назначенных врачом, правильный образ жизни, сбалансированная диета с достаточным содержанием витаминов, кальция, отказ от курения и употребления алкоголя, дозированная нагрузка, соответствующая психоэмоциональная обстановка – моменты, благоприятно отражающиеся на течении заболевания и качестве жизни пациенток.
У больных с метастатическим раком молочной железы, ответивших на гормонотерапию, прием оказавшегося эффективным препарата продолжается длительно, в течение многих месяцев, пока сохраняется эффект лечения. В случае прогрессирования процесса возможна замена данного препарата на лекарственные средства той же группы либо переход на прием препаратов другой группы (например, переход с антиэстрогенов на ингибиторы ароматазы).
Последовательное использование гормональных препаратов разных групп позволяет максимально продлить клинический эффект гормонотерапии. При операбельном раке молочной железы послеоперационная лекарственная терапия способна предупредить возобновление роста опухоли и добиться полного излечения.
Современная гормонотерапия – это наиболее щадящий и эффективный метод лекарственной терапии для больных раком молочной железы с гормоночувствительной опухолью. Оказывая противоопухолевый эффект, она позволяет сохранить качество жизни на хорошем уровне, так как не вызывает характерных для химиотерапии побочных эффектов – угнетение кроветворения, алопецию (выпадение волос), тошноту и рвоту.
Вопросы, чаще всего возникающие у пациентов, которым назначена гормонотерапия
Что представляют собой ингибиторы ароматазы и каков механизм их действия?
Кому назначают лечение ингибиторами ароматазы?
Больным гормоночувствительным раком молочной железы в менопаузе. Женщинам с сохраненной менструальной функцией такое лечение не назначается! Вопрос о выборе препаратов должен решать лечащий врач.
Чем отличаются ингибиторы ароматазы от антиэстрогенов?
И ингибиторы ароматазы, и антиэстрогены препятствуют стимулирующему влиянию эстрогенов на рост гормонозависимого рака молочной железы. Однако механизм их действия различен: ингибиторы ароматазы сдерживают образование эстрогенов у менопаузальных больных, а антиэстрогены блокируют рецепторы эстрогенов в опухоли. Поэтому эти препараты не вызывают перекрестной резистентности, то есть если перестали действовать одни из них, могут быть эффективны другие.
Ингибиторы ароматазы и антиэстрогены входят в арсенал современной гормонотерапии. Их правильное использование улучшает перспективы лечения больных с гормоночувствительным раком молочной железы.
— Н.И. Переводчикова. По материалам журнала «Вместе против рака»