изоэхогенная печень что означает
Доброкачественные очаговые образования печени: возрастные психосоматические аспекты
Непаразитарные кисты печени (НКП) относятся к доброкачественным очаговым образованиям печени и представляют собой полость (или полости) в печени, заполненную жидкостью. Повсеместно отмечается рост заболеваемости НКП, что связано главным образом
Непаразитарные кисты печени (НКП) относятся к доброкачественным очаговым образованиям печени и представляют собой полость (или полости) в печени, заполненную жидкостью.
Повсеместно отмечается рост заболеваемости НКП, что связано главным образом с широким использованием современных методов диагностики, позволяющих визуализировать интраструктуру печени: ультразвуковое исследование (УЗИ), компьютерная томография (КТ), магнитно-резонансная томография (МРТ), ангиографии и пр. По данным H. Sancher et al. (1991), НКП выявляют у 5–10 % населения. При этом у женщин они встречаются в 3–5 раз чаще. Заболевание, как правило, развивается в период между 30 и 50 годами жизни.
Причины возникновения НКП до настоящего времени до конца не выяснены. Так, по мнению Е. Moschowitz, R. Virchow, образование кист связано с воспалительной гиперплазией желчных путей в момент эмбриогенеза с последующей их обструкцией. S. Henson и соавторы считают, что данный процесс служит основой новообразования.
В настоящее время преобладает мнение, что кисты печени возникают из аберрантных желчных ходов, т. е. во время эмбрионального развития не происходит подключения к системе желчных путей отдельных внутридольковых и междольковых желчных ходов. Отсутствие инволюции этих ходов и является причиной развития кист печени, в результате секреции их эпителия в них постепенно происходит накопление жидкости, и они превращаются в кисту. Такое происхождение кист печени подтверждается тем, что в секрете нет желчи, кроме того, кисты печени почти никогда не сообщаются с нормальными желчными ходами. Многие ученые исходят из того, что поражение кистами печени является либо самостоятельной генетической единицей с аутосомальной доминантной наследственностью, либо кистозные изменения различных органов вызываются единым генетическим дефектом с различной распространенностью.
Обсуждается также возможность возникновения кист печени при приеме некоторых лекарственных препаратов (эстрогены, пероральные контрацептивы).
Выделяют истинные и ложные кисты. Истинные кисты отличаются от ложных наличием на внутренней поверхности эпителиального покрова из цилиндрического или кубического эпителия. Ложные кисты развиваются обычно после травмы.
Общепринятой классификации кист печени не существует. На практике наиболее удобной представляется классификация НКП, предлагаемая А. А. Шалимовым и соавторами (1993), согласно которой НКП различают следующим образом:
К осложнениям относят: нагноение, кровотечение в полость кисты, разрыв стенки, портальную гипертензию, механическую желтуху, печеночную недостаточность. При разрыве кисты возможны вторичная инфекция, образование наружных и внутренних свищей, перекрут ножки кисты. Эти осложнения встречаются в 5% случаев. Злокачественные перерождения наблюдаются редко.
Считается, что клиническая картина НКП скудна и неспецифична. Чаще всего кисты печени случайно выявляются при УЗИ органов брюшной полости. Проявления болезни зависят от размера кисты, ее локализации, а также от воздействия кисты на соседние органы. Увеличение кисты приводит и к атрофическим изменениям ткани печени.
Наиболее распространенной жалобой при солитарных кистах печени является боль в верхнем правом квадранте или в эпигастральной области. Боль во многих случаях носит постоянный характер. Пациенты также отмечают быстро наступающее чувство насыщения и дискомфорт в животе после приема пищи.
Раньше важным симптомом считалось обнаружение при пальпации умеренно напряженного массивного опухолевидного образования, смещающегося при дыхании вместе с печенью. Сообщалось, что доступные пальпации кисты печени обычно прощупываются как тугоэластические и легко флюктуирующие безболезненные опухоли. Следует отметить, что даже крупные кисты печени недоступны пальпации из-за расположения глубоко в паренхиме печени или локализации на диафрагмальной поверхности органа.
Появление других, также неспецифических симптомов: слабости, повышенной потливости, потери аппетита, тошноты, одышки — обычно связывают с увеличением размеров кист, но, вероятнее всего, это следствие реагирования других органов — желчного пузыря, двенадцатиперстной кишки и др.
Разнообразие и неспецифичность клинических симптомов диктуют необходимость обследования пациента с целью определения или исключения сопутствующей соматической и психической патологии.
НКП в первую очередь следует дифференцировать с паразитарными кистами. Для этого выполняют специфические серологические исследования крови (реакция непрямой гемагглютинации и иммуноферментного анализа на эхинококкоз). В ряде случаев возникает необходимость дифференциальной диагностики с гемангиомой, цистоаденомой, ретроперитонеальными опухолями, опухолями кишки, брыжейки, поджелудочной железы, водянкой желчного пузыря и метастатическими опухолевыми поражениями печени.
Поликистоз печени часто сочетается с поликистозом почек, поджелудочной железы, яичников. Поликистоз печени, как и солитарная киста, чаще протекает бессимптомно и выявляется случайно при обследовании по поводу другой патологии. В большинстве случаев течение заболевания благоприятное. Клинические симптомы наблюдаются при прогрессировании заболевания, что, как правило, происходит после 40–50 лет. При увеличении объема поликистозных образований больные жалуются на дискомфорт в правом подреберье и эпигастрии, изжогу, отрыжку, что связывают с давлением увеличенной печени на соседние органы. В ходе исследования определяется гепатомегалия. Пальпаторно: печень плотная, бугристая. Функциональные пробы печени обычно не изменяются. Нарушение синтетической функции печени выявляют на поздних стадиях при выраженном перерождении печеночной паренхимы. При массивном распространении процесса, когда происходит замещение большей части паренхимы печени, развивается терминальная печеночная недостаточность. Ситуация усугубляется хронической почечной недостаточностью — исходом поликистоза почек.
Ведущее место в диагностике НКП занимает эхография, благодаря высокой информативности, безвредности и общедоступности этого метода. Эхографически кисты печени представляют собой отграниченные тонкой стенкой (1–2 мм) полости с безэхогенным внутренним пространством, что объясняется разностью плотности жидкости и паренхимы печени. Форма их может быть круглой или овальной. Диагноз основывается на следующих признаках, выявляемых с помощью УЗИ: 1) наличие четких, ровных контуров с хорошо различимой задней стенкой; 2) отсутствие внутренних отражений; 3) выявление усиления эхо-сигналов за образованием.
При наличии внутрипросветной перегородки УЗ-изображение кисты печени может иметь пятнистый рисунок. При осложненных кистах (кровоизлияние или инфицирование), когда выявляются внутрипросветные «эхо»-сигналы, трудно исключить злокачественную опухоль. В сомнительных случаях используют КТ, МРТ, ангиографические и радиологические методы исследования. В определенных ситуациях считается целесообразным проведение чрескожной пункции кисты под контролем УЗИ с последующим бактериологическим и цитологическим исследованием материала.
Традиционно проблемой НКП занимались хирурги, которые разрабатывали методы диагностики и тактику хирургического лечения. В поле зрения хирурга больные с НКП попадали при выявлении очагового образования печени, при этом хирургическое лечение получали пациенты с осложнениями и неосложненными кистами, превышающими 5 см в диаметре.
Терапевтическая тактика при НКП до сих пор не разработана. Целью нашей работы было изучение терапевтических, возрастных и психосоматических аспектов НКП.
Представленный материал базируется на результатах обследования 93 больных (72 женщины и 21 мужчина) в возрасте от 20 до 82 лет, средний возраст — 56,9+11,3 лет. Больные были разделены на две группы по возрастному признаку.
Солитарная НКП была выявлена у 37 человек, 56 больных НПК имели две и более кисты. Средний возраст больных с солитарными кистами печени (27 женщин и 10 мужчин) составил 53,5+11,6 лет. Средний возраст больных с множественными кистами печени составил 59,3+10,6 лет (р Таблица 2. Клинические результаты применения хофитола и эглонила
В анализах крови на фоне двухнедельной терапии отмечалось снижение уровня печеночных ферментов — АСТ и АЛТ, достоверно (р
По вопросам литературы обращайтесь в редакцию.
Ультразвуковая диагностика заболеваний органов пищеварения
Клинический случай
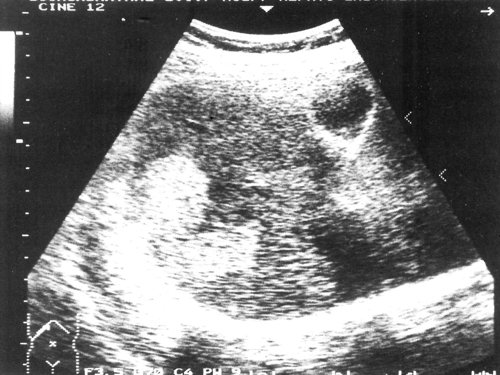
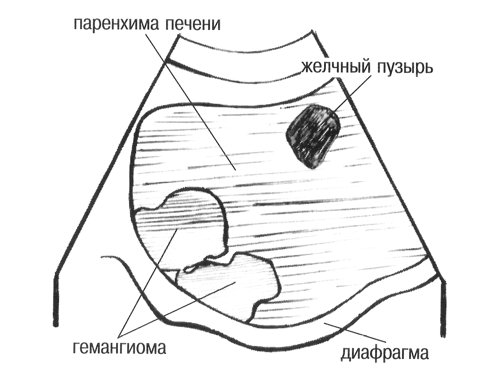
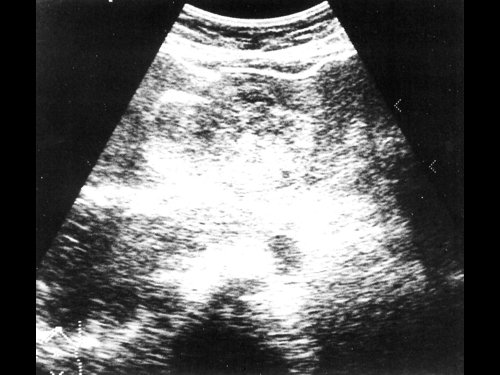
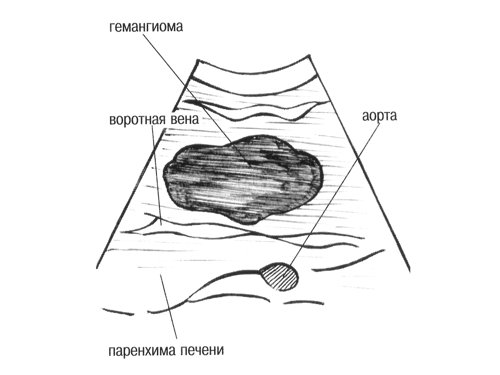
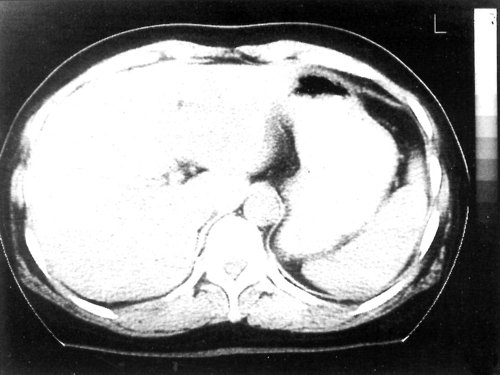
Женщина 50 лет, госпитализирована с болями в верхнем правом квадранте живота. Ультразвуковое исследование органов брюшной полости было проведено в день поступления (рис. 1а, б).
Рис. 1. УЗИ печени.
a) На эхограмме в правой доле печени видны два гиперэхогенных образования с четкими контурами (3,0×1,5 см, 2,5×1,5 см).
б) На эхограмме в левой доле печени видно большое гетерогенное образование (5.0×4.0 см), имеющее дольчатое строение.
Боли в животе, как правило, наблюдаются при обширных образованиях в результате роста опухоли и развития тромбоза, либо из-за сдавления прилежащих органов.
Редко встречающимися осложнениями являются тромбоцитопения, гиперфибриногенемия и спонтанный разрыв гемангиомы [5,6]. Ряд продолжительных наблюдений показал, что в большинстве случаев гемангиомы остаются неизменными, хотя иногда их размеры могут увеличиваться или уменьшаться [6,7]. Было замечено влияние гормонов на рост некоторых гемангиом: увеличение их во время беременности и инволюция под действием кортикостероидной терапии [2,8].
Небольшие гемангиомы обычно состоят из больших наполненных кровью кавернозных полостей, ограниченных слоем плоскоклеточного эпителия и разделенных фиброзными перегородками [12]. При микроскопии образование имеет ячеистую структуру. Множественные перегородки внутри гемангиомы создают характерную гиперэхогенность структуры [7]. Однако по мере роста гемангиомы могут произойти различные изменения: внутреннее кровотечение с некрозом, миксоматозные изменения, тромбоз, фиброз, кальцификация [13]. Эти изменения при эхографии могут проявляться гипоэхогенными, смешанной эхогенности и анэхогенными участками. Более того, исследование гемангиом размером более 4 см в диаметре показало, что некоторые из них имеют дольчатый контур, который соотвествует капсуле, определяемой при гистологическом исследовании и являющейся стенкой опухоли [5].
Если ультразвуковые признаки достаточно типичны, пациенты с асимптоматичной гемангиомой и отсутствием риска малигнизации могут проходить повторные обследования с интервалом в 3-6 месяцев. У пациентов с риском малигнизации ситуация более сложная. В частности, гипоэхогенный ореол вокруг повреждения более соответствует метастазам, чем гемангиоме [15]. У большинства гемангиом имеется гиперэхогенный ободок по периферии, но нет периферического ореола или боковой тени. Так как гепатоцеллюлярная карцинома и метастазы рака толстой кишки, опухоли островковых клеток, карциноида, хориокарциномы могут манифестировать ультразвуковыми признаками, идентичными таковым при гемангиоме, ультразвуковое исследование не может быть единственным достоверным методом дифференциальной диагностики гемангиомы и рака. Поэтому для более точной диагностики необходимо проведение компьютерной томографии с контрастированием, радионуклидные исследования с мечеными эритроцитами, либо ядерно-магнитный резонанс.
В связи с тем, что неосложненные гемангиомы состоят из заполненных кровью сосудистых полостей, при стандартной компьютерной томографии они определяются как хорошо очерченные гомогенные образования, идентичные по плотности внутрипеченочным сосудам, и пониженной плотности по отношению к печеночной паренхиме [16]. Очаги пониженной по сравнению с кровью плотности могут быть видны внутри гемангиомы и представлять собой участок внутреннего фиброза. В печени с жировой инфильтрацией гемангиомы при компьютерной томографии выглядят гиперэхогенными, затрудняя тем самым точную оценку их структуры.
Компьютерные томограммы гемангиом после введения внутривенного контраста зависят от кровотока внутри образования и времени визуализации печеночного кровотока. Характерно, что кровь внутри гемангиомы медленно центростремительно течет от периферических синусоидов к центральным. Поэтому динамическая усиленная компьютерная томография с внутривенным контрастированием показывает центростремительное увеличение гемангиомы, плотность которой одинакова с плотностью прилежащих сосудов на том же уровне визуализации.
Общая интенсивность повреждения будет наибольшей по периферии на ранних стадиях введения контраста и уменьшается по мере снижения концентрации йода в кровотоке. Визуализация через 30 минут после введения контраста показывает изоэхогенность гемангиомы и окружающей печеночной паренхимы. Визуализация во время печеночной артериальной фазы внутривенного контрастирования (25-50 с после введения контраста) дает ярко выраженные пристеночные очаги по периферии гемангиомы. Эти узлы, считающиеся питающим сосудистым центром гемангиомы, характерны в диагностическом плане для гемангиом [18,19].
В нашем случае при ультразвуковом исследовании брюшной полости выявлено атипичное строение гемангиомы, динамическая компьютерная томография указывает на типичную гемангиому (рис. 2а, б). При этом важно знать, что только приблизительно в 54% случаев у больных с гемангиомами имеет место характерная перфузия с центростремительным усилением и поздним заполнением [20]. Однако в связи с тем, что этот тип усиления встречается только у 1,6% первичных и вторичных злокачественных опухолей печени, определение структуры данного усиления позволяет уверенно дифференцировать гемангиомы от злокачественных печеночных опухолей [20].
Диагностика и лечение опухолей печени (рака печени)
Статья проверена 30.03.2021. Статью проверил специалист: Трандофилов Михаил Михайлович, профессор, д.м.н., хирург-онколог, специалист по онкологии печени и желчевыводящих путей.
Печень – жизненно важный орган, без которого наш организм не может функционировать. Печень выполняет важнейшие функции – очищает организм от токсинов и шлаков, синтезирует необходимые биологически активные вещества, поддерживает и защищает нас от инфекций, участвует в обменных процессах, накапливает питательные вещества…
Любое заболевание печение нарушает работу этих функций, что, естественно, сразу же сказывается на здоровье человека. Одной из самых серьезных проблем являются опухоли печени.
Опухоли в печени возникают в том случае, если в ткани органа присутствует хотя бы одна генетически поврежденная раковая клетка. Она начинает неконтролируемо делиться и, через некоторое время, значительно увеличивает число раковых клеток в этом месте. Если при помощи диагностических исследований можно обнаружить эту область, то можно говорить о том, что у человека опухоль печени.
Злокачественные опухоли печени делятся на две группы – это первичные опухоли печени и вторичные метастатические опухоли.
Первичные опухоли печени
Гепатоцеллюлярная карцинома
Гепатоцеллюлярная карцинома (ГЦК) – одна из самых распространенных первичных опухолей печени. Она встречается в 85% случаев первичных злокачественных поражений печени.
Заболевание широко распространено в Южной Африке, Японии, Китае, Юго-Восточной Азии. Опухоль исходит из гепатоцитов (клеток печени). Макроскопически опухоль представлена солитарным (одиночным) или несколькими узлами плотно-эластичной консистенции, белесоватого цвета, на разрезе с множественными очагами геморрагии, некроза и локального пропитывания желчью. Опухоль может иметь четко ограниченную капсулу, диффузно инфильтрировать печень или выступать над ней.
Реже встречаются такие опухоли, как холангиокарциномы (опухоли из эпителия внутрипеченочных желчных протоков). Опухоль диагностируется преимущественно у больных старше 50 лет и составляет до 25 % от всех злокачественных опухолей печени. Опухоль представлена каменистой плотности узлами белесовато-серого цвета. Выделяют также смешанные гепатохолангиокарциномы, и фиброламеллярные карциномы. Значительно реже встречаются саркомы печени, ангиосаркомы (опухоли исходящие из сосудов печени), цистоаденокарциномы.
Чаще всего опухолевый процесс развивается на фоне цирроза и хронических вирусных гепатитов. Как правило, с момента заболевания печени до клинически определяемой опухоли предположительно проходит 20-30 лет. Однако в 25% случае при гепатоцеллюлярной карциноме у пациентов не выявляется ни цирроз, ни какие-либо другие факторы риска развития опухоли.
По статистике, гепатоцеллюлярная карцинома занимает 6 место среди других онкологических заболеваний в мире и весьма высокое 3 место среди причин смертности от онкологических заболеваний. Распространенность опухоли составляет 2-3 случая на 1000000 человек. Среди пациентов преобладают мужчины 40-50 лет.
Симптомы
На ранних стадиях первичные опухоли печени протекают бессимптомно. Симптомы заболевания проявляются, как правило, при уже распространенном процессе. Больной, в основном, жалуется на тяжесть и боль в правом подреберье и правой половине брюшной полости, потерю веса. Как правило, при осмотре у таких пациентов есть признаки увеличения печени. Кроме того, могут выявляться симптомы цирроза и/или печеночной недостаточности (желтушность кожных покровов). Край печени выступает из-под края реберной дуги на 2-3 см, на ощупь – бугристый, при больших размерах опухолей пальпируются узлы в печени.
Диагностика
Для определения точного диагноза необходимо выполнение ультразвукового исследования (УЗИ) и компьютерной томографии печени с контрастированием для определения уровня специфического онкомаркера Альфа-фетопротеина (АФП), который повышен у 90% больных с гепатоцеллюлярной карциномой. Его выявление служит подспорьем в уточнении и подтверждении диагноза.
При наличии цирроза и гиперваскулярного узлового образования в печени (2 см), выявляемого при динамическом контрастном исследовании, при повышении уровня АФП выше 400 нг/мл ставится предварительный диагноз ГЦК.
Также с целью постановки диагноза больным выполняется биопсия печени с гистологическим исследованием материала, позволяющая в 100 % случаев поставить диагноз.
Методы лечения
Трансплантация печени – единственный путь к полному выздоровлению при гепатоцеллюлярной карциноме.
В России за последние 10 лет произведено около 40 трансплантаций при первичных опухолях печени.
При выполнении трансплантации печени соблюдаются строгие критерии отбора больных (миланские критерии), при которых максимальный размер одной опухоли не должен превышать 5 см или три опухолевых узла не больше 3 см в максимальном размере. При соблюдении вышеперечисленных критериев, 10-летняя выживаемость больных составляет 50-60 %.
К сожалению, существует большая проблема нехватки донорских органов и, вследствие этого, возникает длительный лист ожидания трансплантации. Кроме того, пациенты часто обращаются в такой момент, когда опухоль уже превышает размеры, допустимые для трансплантации печени.
Для увеличения продолжительности жизни пациентов, находящихся в листе ожидания на трансплантацию печени, им проводится радиочастотная деструкция опухолей печени.
Для того чтобы вовремя выявить пациентов с первичными опухолями печени, проводятся различные скрининговые программы ранней диагностики. К этой группе относят всех больных с циррозом печени, хроническими вирусными гепатитами и наличием очаговых поражений печени.
Этим больным в ходе диагностического поиска активно применяется алгоритм Bruix et al. (2001), основанный на мониторинге изменений при динамических сонографических исследованиях, компьютерной томографии и контроле уровня альфа-фетопротеина каждые 6 месяцев. При наличии очаговых образований в печени превышающих 1 см, повышении уровня альфапротеина, а также при усилении образования в артериальную фазу при контрастировании, больным выполняется биопсия печени с целью ранней диагностики первичных опухолей печени. И, в частности, гепатоцеллюлярной опухоли, как самой встречающейся формы рака печени.
Резекция печени – этот метод оперативного лечения рака печени проводится только в том случае, если у пациента нет цирроза печени, при отсутствии прорастания опухолью крупных сосудов печени и нижней полой вены, при поражении одной доли печени и отсутствии внеорганных метастазов. К сожалению, к этой подгруппе относится только около 20% больных.
Резекция может быть проведена у некоторых больных с циррозом только при условии сохранной функции печени, нормальном уровне билирубина и без портальной гипертензии.
Пациентам с высоким риском развития декомпенсации печеночной функции резекцию печени не проводят.
Наилучшие результаты после резекции получены в группе больных с опухолью менее 5 см, ограниченной пределами органа и без признаков проникновения опухоли в магистральные сосуды.
Проводятся следующие виды операций анатомические резекции печени различных объемов:
Радиочастотная деструкция (абляция) – проводится тем больным, которым противопоказано проведение резекции опухоли печени или невозможна трансплантация печени (вследствие наличия тяжелой сопутствующей патологии, выряженных явлений цирроза).
Проведение радиочастотной деструкции показано при максимальном размере опухоли до 5 см. Также возможно проведение деструкции при одновременном поражении двух долей печени, наличием внеорганных метастазов, печеночной недостаточности.
При таком лечении рака печени соблюдаются те же критерии, что и при резекции. Обязательно отступают на 10 мм от видимой зоны опухоли, с увеличением зоны термодеструкции превышающим размер опухоли на 10 мм (так называемая зона абластики).
Радиочастотная абляция выполняется чрескожно чреспеченочно под контролем ультразвука или лапароскопическим контролем. Вследствие этого наблюдается минимальное количество осложнений и отсутствуют летальные исходы.
Группе пациентов со стадией С, которым противопоказано хирургическое лечение рака печени, как правило проводится эмболизация питающей опухоль артерии, таргетная терапия.
Вторичные опухоли печени
Метастатические опухоли
Одним из характерных свойств опухолей является их способность метастазировать – раковые клетки «отрываются» от первичной опухоли, распространяются через кровь или лимфатические сосуды в другие, здоровые органы и ткани и дают в них начало новым очагам роста. Так образуются метастазы в печени.
Метастатическими опухолями называются опухоли, являющиеся злокачественными клетками первичной опухоли, попавшими в другой орган различными путями:
Этот процесс приводит к развитию в органе вторичной опухоли. Причем размер такой опухоли может превышать размер первичной опухоли в несколько раз.
Чаще всего метастазы в печени возникают при поражении опухолями желудочно-кишечного тракта, молочной железы, почек.
В последние годы увеличилось количество онкологических больных с метастазами в печени. Так в России раком ободочной кишки ежегодно заболевают 23 000 человек и раком прямой кишки – 17 000 человек. К тому времени, как устанавливается диагноз, метастазы в печени выявляются у 30 % больных. При раке молочной железы метастазы в печени обнаруживаются в 15-67 % случаев.
Симптомы
Клинические проявления заболевания, как правило, отсутствуют. При больших размерах опухолей или множественном поражении обоих долей печени появляются жалобы на общую слабость, тяжесть и боли в правом подреберье, желтушность склер и кожных покровов. При пальпации в области правого подреберья ощущаются плотные, не смещаемые бугристые образования, болезненные при глубоком нажатии.
Диагностика
Всем, кто уже ранее оперировался по поводу злокачественных опухолей желудка, толстой и прямой кишки, почки и молочной железы, необходимо проведение ультразвукового исследования печени, определения онкомаркеров, рентген грудной клетки раз в 3-6 месяцев – в зависимости от стадии развития первичной опухоли.
При проведении УЗИ возможно выявление опухолей более 1 см в диаметре, в виде гиперэхогенной опухоли с гипоэхогенным ободком.
При наличии подозрений на метастатическую опухоль печени выполняют рентгенкомпьютерную томографию печени с контрастированием или позитронно-эмиссионную томографию печени (ПЭТ). Контраст накапливается в опухоли и позволяет увидеть все опухоли печени диаметром от 0,5 см. С целью дифференциальной диагностики выполняется биопсия печени чрескожно чреспеченочно под контролем ультразвука.
Методы лечения
Показаниями к оперативному лечению больных с метастазами в печени традиционно является наличие одиночного метастаза большого размера (I стадия) или опухолей небольших размеров при их унилобарной локализации (II cтадия).
Количество больных с одиночными метастазами небольших размеров или одиночными метастазами больших размеров не превышает 14-18 % от числа всех больных с метастатическим поражением печени. Вследствие этого, резектабельность больных с метастатическим раком печени составляет 14-18%.
Резекция печени
При хирургическом лечении метастаз в печени применяются различные виды операций в зависимости от этиологии поражения органа.
Резекция печени – одна из наиболее часто встречающихся операций при лечении рака печени. По принципу выполнения в настоящее время их принято делить на типичные резекции (анатомические, центральные) и атипичные (периферические).
Атипичными периферическими резекциями печени называются резекции, при которых выделение удаляемой части печени осуществляется с помощью метода дигитоклазии с поэтапной перевязкой сосудов и желчных протоков. К атипичным резекциям относятся операции, выполненные без предварительной перевязки сосудисто-секторальной ножки.
При лечении рака печени больным выполняются анатомические и атипичные резекции различных объемов, такие как:
В настоящее время, несмотря на использование при резекциях печени современной хирургической техники и физических методов воздействия, остается довольно высокой частота интраоперационных и послеоперационных осложнений при выполнении резекции печени при метастатических раках печени. Эти показатели колеблются от 23 до 55 %.
При билобарной локализации вторичных опухолей печени (в двух долях), множественном распространении II и III степени объемов поражения печени с поражением забрюшинных лимфоузлов, лечение рака печени 4 стадии при помощи традиционных оперативных вмешательств затруднено из-за превышения риска оперативного пособия над эффектом от операции. Таким онкологическим больным требуется паллиативная помощь.
Вследствие этого, проводятся активные поиски новых малоинвазивных технологий хирургического лечения с целью улучшения качества и продолжительности жизни этой тяжелой и обреченной категории больных.
Радиочастотная деструкция (абляция)
Одной из современных малоинвазивных технологий при лечении рака печени является использование радиочастотной абляции метастазов в печени.
Радиочастотная деструкция проводится пациентам с размером опухоли до 50 мм, с увеличением зоны деструкции превышающим размер опухоли на 10 мм (так называемая зона абластики). Малоинвазивные операции выполняются чрескожно чреспеченочно под контролем ультразвука или лапароскопическим контролем.
Прогноз результатов лечения метастаз в печени методом радиочастотной деструкции благоприятный – наблюдается минимальное количество осложнений, отсутствую летальные исходы.
Преимуществами данной методики перед традиционными резекциями являются:
Всем больным после проведения радиочастотной деструкции проводится полихимиотерапия.
Непаразитарные кисты печени
Кисты печени делятся на паразитарные и непаразитарные кисты. В свою очередь непаразитарные кисты печени бывают:
Кисты в печени возникают в результате нарушения формирования желчных ходов в процессе внутриутробного развития. При этом образуются группы аберрантных (закупоренных) желчных капилляров, которые в последствие постепенно расширяются в связи со скоплением в них серозной жидкости. Кроме того, кисты могут образоваться на фоне воспалительных и дегенеративных изменений в желчных путях и печени.
В упрощенном варианте кисты печени можно подразделить:
Симптомы
Кисты печени в большинстве случаев протекают без клинических проявлений. Симптомы заболевания появляются только при наличии больших кист (чувство дискомфорта, ноющие боли в области правого подреберья), а также при возникновении осложнений (кровоизлияние, нагноение, перфорация, желтуха).
Простые кисты печени в 50% бывают одиночными, в остальных случаях — множественными. Размеры их могут достигать от 1,0 до 20 см. В редких случаях простые кисты могут по неизвестным причинам быстро увеличиваться в размерах, вызывая соответствующую болевую симптоматику, что наблюдается преимущественной у женщин старше 50 лет.
Диагностика
Для диагностирования кисты необходимо пройти ультразвуковое исследование (УЗИ) или компьютерную томографию.
Методы лечения
К радикальному удалению кисты следует прибегать только в случае цистаденомы и опасности ее опухолевого перерождения. Кисты печени менее 5 см в диаметре подлежат динамическому контролю, кисты диаметром от 5,0 до 10,0 см и более подлежат оперативному лечению
Операции на печени при непаразитарных кистах варьируются от простой пункции до резекции печени. Операции можно условно разделить на следующие основные группы:
1. Условно-радикальные:
2. Паллиативные:
Рациональный выбор паллиативной помощи онкологическим больным зависит от вида кисты, ее взаимоотношения с печенью, наличием или отсутствием осложнений, ее размеров и тяжести состояния больного.
Чрескожное чреспеченочное дренирование кисты под контролем ультразвука.
Кисты диаметром от 5,0 до 10,0 см в 90% случаев излечиваются пункционно-склерозирующим способом.
Под контролем УЗИ в полость кисты чрескожно чреспеченочно вводят дренаж, и после удаления содержимого кисты ее полость промывается спиртовым раствором. Содержимое кисты отправляют на цитологическое исследование. В редких случаях приходится прибегать к повторным пункциям. Дренаж в полости кисты оставляется на несколько дней. До склерозирования кисты, после сокращения кисты в размерах дренаж удаляют. Процесс лечения контролируется ультразвуковым исследованием в динамике.
Необходимость оперативного вмешательства возникает при симптоматических и рецидивирующих после пункций больших кистах печени (более 10,0 см), а также цистаденомах. С развитием эндоскопической хирургии появилась возможность иссечения кист под контролем видеолапароскопии.
Вылущевание, экстирпация или перицистэктомия кист печени – одна из самых распространенных операций. Оперативное вмешательство заключается в полном удалении стенок кисты.
Частичное иссечение стенок кисты
Паллиативная помощь онкологическим больным методом частичного иссечения стенок кисты с ушиванием и дренированием остаточной полости, обычно применяется при больших размерах кист, при расположении кист вблизи ворот печени, крупного сосуда или желчного протока. Важно отметить, что лишь при отсутствии примеси желчи в содержимом возможно иссечение купола стенки кисты, оставляя ее основание интактным в толще паренхимы печени.
Инфицированные кисты паразитарной и непаразитарной этиологии требуют выполнения наружного дренирования или марсупилизации.
При кистах, содержащих желчь необходима цистоэтеро- или гастростомия.