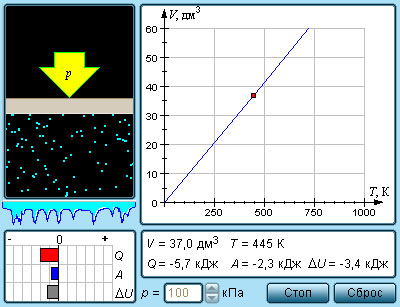
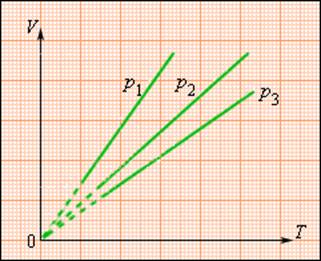
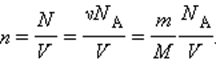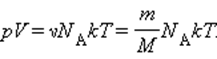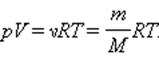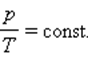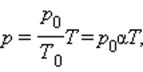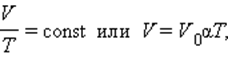изопроцессы в газах что такое
Изопроцессы в газах что такое
| Законы идеальных газов |   |
| В XVII – XIX веках были сформулированы опытные законы идеальных газов. Кратко напомним их. Изопроцессы идеального газа – процессы, при которых один из параметров остаётся неизменным. 1. Изохорический процесс. Закон Шарля. V = const. Изохорическим процессом называется процесс, протекающий при постоянном объёме V. Поведение газа при этом изохорическом процессе подчиняется закону Шарля: При постоянном объёме и неизменных значениях массы газа и его молярной массы, отношение давления газа к его абсолютной температуре остаётся постоянным: P/Т = const. График изохорического процесса на РV-диаграмме называется изохорой. Полезно знать график изохорического процесса на РТ— и VT-диаграммах (рис. 1.6). Уравнение изохоры: Изобарическим процессом называется процесс, протекающий при постоянном давлении Р. Поведение газа при изобарическом процессе подчиняется закону Гей-Люссака: При постоянном давлении и неизменных значениях массы и газа и его молярной массы, отношение объёма газа к его абсолютной температуре остаётся постоянным: V/T = const. График изобарического процесса на VT-диаграмме называется изобарой. Полезно знать графики изобарического процесса на РV— и РT-диаграммах (рис. 1.8). Изотермическим процессом называется процесс, протекающий при постоянной температуре Т. Поведение идеального газа при изотермическом процессе подчиняется закону Бойля – Мариотта: При постоянной температуре и неизменных значениях массы газа и его молярной массы, произведение объёма газа на его давление остаётся постоянным: PV = const. График изотермического процесса на РV-диаграмме называется изотермой. Полезно знать графики изотермического процесса на VT— и РT-диаграммах (рис. 1.10). Адиабатический процесс – термодинамический процесс, происходящий без теплообмена с окружающей средой. 5. Политропический процесс. Процесс, при котором теплоёмкость газа остаётся постоянной. Политропический процесс – общий случай всех перечисленных выше процессов. 6. Закон Авогадро. При одинаковых давлениях и одинаковых температурах, в равных объёмах различных идеальных газов содержится одинаковое число молекул. В одном моле различных веществ содержится NA=6,02·10 23 молекул (число Авогадро). 7. Закон Дальтона. Давление смеси идеальных газов равно сумме парциальных давлений Р, входящих в неё газов: При В соответствии с законами Бойля – Мариотта (1.4.5) и Гей-Люссака (1.4.3) можно сделать заключение, что для данной массы газа ИзопроцессыАвтор статьи — профессиональный репетитор, автор учебных пособий для подготовки к ЕГЭ Игорь Вячеславович Яковлев Темы кодификатора ЕГЭ: изопроцессы — изотермический, изохорный, изобарный процессы.На протяжении этого листка мы будем придерживаться следующего предположения: масса и химический состав газа остаются неизменными. Иными словами, мы считаем, что: Эти два условия выполняются в очень многих физически интересных ситуациях (например, в простых моделях тепловых двигателей) и потому вполне заслуживают отдельного рассмотрения. Если масса газа и его молярная масса фиксированы, то состояние газа определяется тремя макроскопическими параметрами: давлением, объёмом и температурой. Эти параметры связаны друг с другом уравнением состояния (уравнением Менделеева — Клапейрона). Термодинамический процесс (или просто процесс) — это изменение состояния газа с течением времени. В ходе термодинамического процесса меняются значения макроскопических параметров — давления, объёма и температуры. Особый интерес представляют изопроцессы — термодинамические процессы, в которых значение одного из макроскопических параметров остаётся неизменным. Поочерёдно фиксируя каждый из трёх параметров, мы получим три вида изопроцессов. Изопроцессы описываются очень простыми законами Бойля — Мариотта, Гей-Люссака и Шарля. Давайте перейдём к их изучению. Изотермический процессКак мы сказали с самого начала,масса и молярная масса предполагаются неизменными. Поэтому правые части выписанных уравнений равны. Следовательно, равны и левые части: Поскольку два состояния газа были выбраны произвольно, мы можем заключить, что в ходе изотермического процесса произведение давления газа на его объём остаётся постоянным: Данное утверждение называется законом Бойля — Мариотта. Записав закон Бойля — Мариотта в виде можно дать и такую формулировку: в изотермическом процессе давление газа обратно пропорционально его объёму. Если, например, при изотермическом расширении газа его объём увеличивается в три раза, то давление газа при этом в три раза уменьшается. Как объяснить обратную зависимость давления от объёма с физической точки зрения? При постоянной температуре остаётся неизменной средняя кинетическая энергия молекул газа, то есть, попросту говоря, не меняется сила ударов молекул о стенки сосуда. При увеличении объёма концентрация молекул уменьшается, и соответственно уменьшается число ударов молекул в единицу времени на единицу площади стенки — давление газа падает. Наоборот, при уменьшении объёма концентрация молекул возрастает, их удары сыпятся чаще и давление газа увеличивается. Графики изотермического процессаВообще, графики термодинамических процессов принято изображать в следующих системах координат: График изотермического процесса называется изотермой. Рис. 2. Чем выше температура, тем выше изотерма В оставшихся двух системах координат изотерма выглядит очень просто: это прямая, перпендикулярная оси (рис. 3 ): Изобарный процессНапомним ещё раз, что изобарный процесс — это процесс, проходящий при постоянном давлении. В ходе изобарного процесса меняются лишь объём газа и его температура. где — атмосферное давление. Выпишем уравнения состояния: Поделив их друг на друга, получим: В принципе, уже и этого могло бы быть достаточно, но мы пойдём немного дальше. Перепишем полученное соотношение так, чтобы в одной части фигурировали только параметры первого состояния, а в другой части — только параметры второго состояния (иными словами, «разнесём индексы» по разным частям): А отсюда теперь — ввиду произвольности выбора состояний! — получаем закон Гей-Люссака: Иными словами, при постоянном давлении газа его объём прямо пропорционален температуре: Почему объём растёт с ростом температуры? При повышении температуры молекулы начинают бить сильнее и приподнимают поршень. При этом концентрация молекул падает, удары становятся реже, так что в итоге давление сохраняет прежнее значение. Графики изобарного процессаПунктирный участок графика означает, что в случае реального газа при достаточно низких температурах модель идеального газа (а вместе с ней и закон Гей-Люссака) перестаёт работать. В самом деле, при снижении температуры частицы газа двигаются всё медленнее, и силы межмолекулярного взаимодействия оказывают всё более существенное влияние на их движение (аналогия: медленный мяч легче поймать, чем быстрый). Ну а при совсем уж низких температурах газы и вовсе превращаются в жидкости. Рис. 5. Чем ниже изобара, тем больше давление В оставшихся двух системах координат изобара является прямой линией, перпендикулярной оси (рис. 6 ): Изохорный процессИзохорный процесс, напомним, — это процесс, проходящий при постоянном объёме. При изохорном процессе меняются только давление газа и его температура. Изохорный процесс представить себе очень просто: это процесс, идущий в жёстком сосуде фиксированного объёма (или в цилиндре под поршнем, когда поршень закреплён). Делим эти уравнения друг на друга: Как и при выводе закона Гей-Люссака, «разносим» индексы в разные части: Ввиду произвольности выбора состояний мы приходим к закону Шарля: Иными словами, при постоянном объёме газа его давление прямо пропорционально температуре: Увеличение давления газа фиксированного объёма при его нагревании — вещь совершенно очевидная с физической точки зрения. Вы сами легко это объясните. Графики изохорного процессаСмысл пунктирного участка тот же: неадекватность модели идеального газа при низких температурах. Рис. 8. Чем ниже изохора, тем больше объём В оставшихся двух системах координат изохора является прямой линией, перпендикулярной оси (рис. 9 ): Законы Бойля — Мариотта, Гей-Люссака и Шарля называются также газовыми законами. Мы вывели газовые законы из уравнения Менделеева — Клапейрона. Но исторически всё было наоборот: газовые законы были установлены экспериментально, и намного раньше. Уравнение состояния появилось впоследствии как их обобщение. «Изопроцессы»Разделы: Физика Цели, ориентированные на развитие личности учащегося: Единый план изучения газовых законов: Основные понятия урока: изопроцессы, изотермический, изобарный, изохорный, изотерма, изобара, изохора. I. Организационный момент Сообщение целей и задач урока. II. Актуализация знаний Проверка домашнего задания III. Объяснение нового материала Количественные зависимости между двумя параметрами газа одной и той же массы при неизменном значении третьего параметра называют газовыми законами. Первый газовый закон был открыт английским ученым Р. Бойлем. Работа называлась «Новые эксперименты, касающиеся воздушной пружины». Бойль изучал давление газа в зависимости от объема при постоянной температуре. Данный процесс называется изотермическим.
Теперь давайте сформулируем изотермический закон: Для газа данной массы произведение давления газа на его объем постоянно, если температура газа не меняется. А сам процесс изменения состояния термодинамической системы при постоянной температуре называется изотермическим процессом.
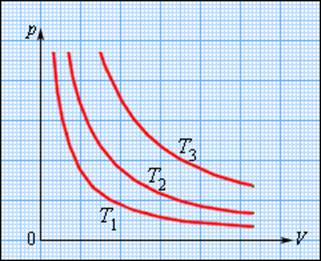
Зависимость давления газа от объема при постоянной температуре графически изображается кривой, которая называется изотермой. Изотерма газа изображает обратно пропорциональную зависимость между давлением и объемом. Кривую такого рода в математике называют гиперболой. Разным постоянным температурам соответствуют различные изотермы. При повышении температуры давление согласно уравнению состояния Изотермическим процессом приближенно можно считать процесс медленного сжатия воздуха или расширения газа под поршнем насоса при откачке его из сосуда. Провожу закрепление нового материала: Мини-тест, решение задач Следующий закон называется законом Гей-Люссака и происходит при постоянном объеме.
Теперь давайте, ребята, вместе сформулируем закон Гей-Люссака: Для газа данной массы отношение объема к температуре постоянно, если давление газа не изменяется. Сам же процесс изменения состояния термодинамической системы при постоянном давлении называется изобарным. Объем данной массы газа при р = const зависит от температуры по линейному закону
Различным давлениям соответствуют разные изобары. С ростом давления объем газа при постоянной температуре согласно закону Бойля-Мариотта уменьшается. Поэтому изобара, соответствующая более высокому давлению р2, лежит ниже изобары, соответствующей более низкому давлению (Рисунок 4) В области низких температур все изобары идеального газа сходятся в точке Т = 0. Но это не означает, что объем реального газа действительно обращается в нуль. Все газы при сильном охлаждении превращаются в жидкости, а к жидкостям уравнение состояния Изобарным можно считать расширение газа при нагревании его в цилиндре с подвижным поршнем. Постоянство давления в цилиндре обеспечивается атмосферным давлением на внешнюю поверхность поршня. При V = const давление данной массы газа при постоянном объеме зависит от температуры по линейному закону: В результате эксперимента получаем таблицу и график зависимости (Р, T) откуда видно, что
Теперь давайте, ребята, вместе сформулируем закон Шарля: Для газа данной массы отношение давления к температуре постоянно, если объем не меняется. Сам же процесс изменения состояния термодинамической системы при постоянном объеме называется изохорным.
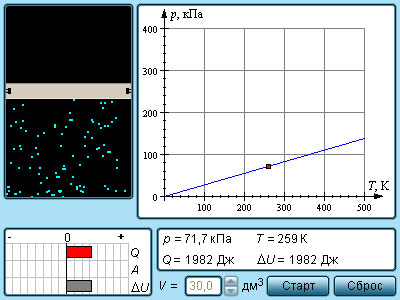
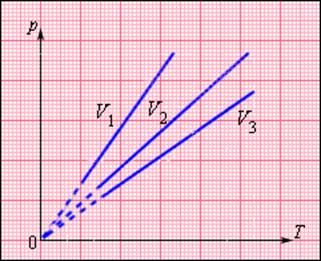
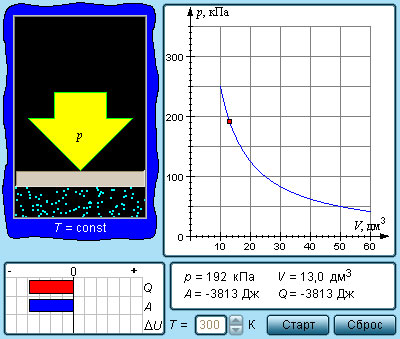
Эта зависимость давления от температуры изображается прямой, называемой изохорой. Разным объемам соответствуют разные изохоры. С ростом объема газа при постоянной температуре давление согласно закону Бойля – Мариотта падает. Поэтому изохора, соответствующая большему объему V2, лежит ниже изохоры, соответствующей меньшему объему V1. В соответствии с законом Шарля все изохоры начинаются в точке Т = 0. Значит, давление идеального газа при абсолютном нуле равна нулю. Увеличение давление газа в любой емкости или в электрической лампочке при нагревании является изохорным процессом. Изохорный процесс используется в газовых термометрах постоянного объема. IV. Структурированный комплексный тест по всем газовым законам Тест составлен в EXSEL (приложение 2). Программа сразу же автоматически выставляет полученную оценку и указывает на ошибки. Причем она позволяет при соответствующем навыке работы с ней исправлять эти ошибки. Это вырабатывает у учащихся уверенность в своих в себе, веру в свои знания, повышает познавательный интерес. V. Домашнее задание На рисунке (смотри слайд №26) дан график изменения состояния идеального газа в координатных осях V, T. Представьте этот процесс в координатных осях P, T и P, V. Уравнение состояния идеального газа. ИзопроцессыСоотношение p = n k T – это формула, связывающая значение давления газа с его температурой и концентрацией молекул на единицу объема. Значением N является количество молекул данного сосуда, N А – постоянной Авогадро, m – массой газа в емкости, М – молярной массой газа. Исходя из этого, формула примет вид: Соотношение p V = ν R T = m M R T получило название уравнения состояния идеального газа. Если имеется смесь невзаимодействующих газов, то формулу запишем как: Еще в ХХ веке Б. Клапейрон получил уравнение, показывающее связь между давлением и температурой: Впоследствии оно было записано Д.И. Менделеевым. Позже его назвали уравнением Клапейрона-Менделеева. Задолго до получения уравнения состояния идеального газа на основе молекулярно-кинетической теории поведения газов изучались в различных условиях экспериментально. То есть уравнение p V = ν R T = m M R T служит обобщением всех опытных фактов. При протекании процессов медленно, система находится в состоянии, близком к равновесному. Процесс получил название квазистатического. Соотнеся с происхождением процессов в нашем времени, то его протекания нельзя считать медленными. Обычное время для разрежения и сжатия газа сотни раз в секунду. Это рассматривается как квазистатический процесс. Они изображаются с помощью диаграммы состояний параметров, где каждая из точек показывает равновесное состояние. Уравнение состояния идеального газа. Изопроцессысвязывающее давление газа с его температурой и концентрацией молекул, получено в 3.2 для модели идеального газа, молекулы которого взаимодействуют между собой и со стенками сосуда только во время упругих столкновений. Это соотношение может быть записано в другой форме, устанавливающей связь между макроскопическими параметрами газа – объемом V, давлением p, температурой T и количеством вещества ν. Для этого нужно использовать равенства Здесь N – число молекул в сосуде, NА – постоянная Авогадро, m – масса газа в сосуде, M – молярная масса газа. В итоге получим: Произведение постоянной Авогадро NА на постоянную Больцмана k называется универсальной газовой постоянной и обозначается буквой R. Ее численное значение в СИ есть: называется уравнением состояния идеального газа. Для одного моля любого газа это соотношение принимает вид: Если температура газа равна Tн = 273,15 К (0 °С), а давление pн = 1 атм = 1,013·10 5 Па, то говорят, что газ находится при нормальных условиях. Как следует из уравнения состояния идеального газа, один моль любого газа при нормальных условиях занимает один и тот же объем V0, равный V0 = 0,0224 м 3 /моль = 22,4 дм 3 /моль. Это утверждение называется законом Авогадро. Для смеси невзаимодействующих газов уравнение состояния принимает вид где ν1, ν2, ν3 и т. д. – количество вещества каждого из газов в смеси. Уравнение, устанавливающее связь между давлением, объемом и температурой газа было получено в середине XIX века французским физиком Бенуа Клайпероном, в форме (*) оно было впервые записано Дмитрием Ивановичем Менделеевым. Поэтому уравнение состояния газа называется уравнением Клапейрона–Менделеева. Следует отметить, что задолго до того, как уравнение состояния идеального газа было теоретически получено на основе молекулярно-кинетической модели, закономерности поведения газов в различных условиях были хорошо изучены экспериментально. Поэтому уравнение (*) можно рассматривать как обобщение опытных фактов, которые находят объяснение в молекулярно-кинетической теории. Газ может участвовать в различных тепловых процессах, при которых могут изменяться все параметры, описывающие его состояние (p, V и T). Если процесс протекает достаточно медленно, то в любой момент система близка к своему равновесному состоянию. Такие процессы называются квазистатическими. В привычном для нас масштабе времени эти процессы могут протекать и не очень медленно. Например, разрежения и сжатия газа в звуковой волне, происходящие сотни раз в секунду, можно рассматривать как квазистатический процесс. Квазистатические процессы могут быть изображены на диаграмме состояний (например, в координатах p, V) в виде некоторой траектории, каждая точка которой представляет равновесное состояние. Интерес представляют процессы, в которых один из параметров (p, V или T) остается неизменным. Такие процессы называются изопроцессами. Изотермический процесс (T = const) Изотермическим процессом называют квазистатический процесс, протекающий при постоянной температуре T. Из уравнения (*) состояния идеального газа следует, что при постоянной температуре T и неизменном количестве вещества ν в сосуде произведение давления p газа на его объем V должно оставаться постоянным: |
 |

 , давление смеси газов:
, давление смеси газов:










 увеличивается, если V = const. Поэтому изотерма, соответствующая более высокой температуре Т2, лежит выше изотермы, соответствующей более низкой температуре Т1 (Рисунок 2).
увеличивается, если V = const. Поэтому изотерма, соответствующая более высокой температуре Т2, лежит выше изотермы, соответствующей более низкой температуре Т1 (Рисунок 2).



 (Рисунок 5)
(Рисунок 5)