изоциановая кислота для чего используется
Изоциановая кислота
| Изоциановая кислота | |
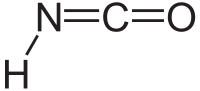 | |
| Общие | |
|---|---|
| Химическая формула | HN=C=O |
| Эмпирическая формула | CHNO |
| Физические свойства | |
| Молярная масса | 43.03 г/моль |
| Плотность | 1.14 г/см³ |
| Термические свойства | |
| Температура плавления | -86 °C [1] °C |
| Температура кипения | 23.5 °C |
| Энтальпия образования (ст. усл.) | -153.3 кДж/моль |
| Удельная теплота испарения | 28,4 кДж/моль |
| Давление пара | 36,13 кПа (273,16 К) |
| Химические свойства | |
| pKa | 3,47 (в водн. растворах) |
| Структура | |
| Кристаллическая структура | кристаллы ромбической сингонии (а = 1,082 нм, b = 0,523 нм, с = 0,357 нм, Z = 4, пространств. группа Pnma [2] ) |
| Классификация | |
| Рег. номер CAS | 75-13-8 |
| SMILES | O=C=[N@H] |
Свойства и реакционная способность
Изоциановая кислота является слабой кислотой (Ka = 3,47·10 −4 в водных растворах), стабильна в растворах в диэтиловом эфире, бензоле и толуоле; в водных растворах гидролизуется с образованием диоксида углерода и аммиака, гидролиз ускоряется в присутствии минеральных кислот:
HNCO + H2O 
Атом углерода изоциановой кислоты является электрофильным центром: циановая кислота взаимодействует с такими нуклеофилами, как аммиак, амины и спирты, образуя соответствующие продукты присоединения.
При взаимодействии изоциановой кислоты со спиртами образуются уретаны:
которые с избытком изоциановой кислоты образуют эфиры аллофановой кислоты:
HNCO + H2N-CO-COOR 
Взаимодействие изоциановой кислоты с аммиаком ведет к образованию цианата аммония, который при нагревании изомеризуется в мочевину, эта реакция, открытая Вёлером в 1828 г., стала первым синтезом органического соединения из неорганических веществ [4] :
RNH2 + HNCO 
и гидразин, образующий в реакции с изоциановой кислотой семикарбазид:
NH2NH2 + HNCO 
Безводная изоциановая кислота самопроизвольна полимеризуется в твердую белую массу, состоящую преимущественно из циамелида — линейного полимера (-O-C(=NH)-)n, который при нагревании деполимеризуется с образованием исходной кислоты.
Под действием триэтилфосфина и третичных аминов изоциановая кислота тримеризуется с образованием циануровой кислоты (2,3,5-тригидрокси-сим-триазина).
Подобно минеральным кислотам, изоциановая кислота присоединяется к алкенам с образованием алкилизоцианатов, легче всего реагируют алкены с терминальной двойной связью и электрондонорным заместителем при двойной связи, например, виниловые эфиры:
RO-CH=CH2 + HNCO 
Синтез
Лабораторным методом синтеза изоциановой кислоты является термическое разложение циануровой кислоты. Реакцию проводят при
400 °C, используя очищенную циануровую кислоту (примеси могут привести к взрывному разложению), в промышленности изоциановую кислоту получают каталитическим окислением синильной кислоты при 630—650 °C на контактной сетке из золота.
Цианаты могут быть получены окислением цианидов щелочных металлов: так, при плавлении цианида калия на воздухе происходит его загрязнение образующимся вследствие окисления цианатом калия, окисление цианидов натрия и калия воздухом или кислородом в присутствии никеля является промышленным методом синтеза цианатов. Цианаты натрия и калия также синтезируют сплавлением соответствующих цианидов с оксидом свинца или свинцовым суриком Рb3О4. Перекись водорода также окисляет цианиды до цианатов.
Примечания
Полезное
Смотреть что такое «Изоциановая кислота» в других словарях:
изоциановая кислота — izocianato rūgštis statusas T sritis chemija apibrėžtis Cianato rūgšties tautomeras. formulė HNCO atitikmenys: angl. isocianic acid rus. изоциановая кислота … Chemijos terminų aiškinamasis žodynas
ЦИАНОВАЯ КИСЛОТА — (цианатная к та) в своб. виде существует в виде изоформы (изоциановая к та) HN = C = O, мол. м. 43,03; бесцв. жидкость с резким запахом, напоминающим запах уксусной к ты; т. пл. от 81 до 79 … Химическая энциклопедия
Спирты — Отличительная особенность спиртов гидроксильная группа при насыщенном атоме углерода на рисунке выделена красным (кислород) и серым цветом (водород). Спирты (от лат. … Википедия
Ядовитые животные — такие, которые или имеют ядоносные аппараты, являющиеся органами защиты и нападения, или такие, которых ткани содержат ядовитые вещества, делающие этих животных негодными к употреблению в пищу. По всей вероятности, выделение трихоцист из тела… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
isocianic acid — izocianato rūgštis statusas T sritis chemija apibrėžtis Cianato rūgšties tautomeras. formulė HNCO atitikmenys: angl. isocianic acid rus. изоциановая кислота … Chemijos terminų aiškinamasis žodynas
izocianato rūgštis — statusas T sritis chemija apibrėžtis Cianato rūgšties tautomeras. formulė HNCO atitikmenys: angl. isocianic acid rus. изоциановая кислота … Chemijos terminų aiškinamasis žodynas
Неорганические кислоты — Основная статья: Кислота Неорганические (минеральные) кислоты неорганические вещества, обладающие комплексом физико химических свойств, которые присущи кислотам. Вещества кислотной природы известны для большинства химических элементов за… … Википедия
Гидроксиды — (гидроокиси) соединения оксидов химических элементов с водой. Известны гидроксиды почти всех химических элементов; некоторые из них встречаются в природе в виде минералов. Гидроксиды щелочных металлов называются щелочами. Классификация В… … Википедия
Теллуроводород — Общие сведения Систематическое наименование Теллуроводород Прочие наименования Гидрид теллура Теллурид водорода Дигидрид теллура Дигидротеллурид Теллан Молекулярная формула H2Te Молярная масса 129,6159 г/моль … Википедия
Вода — У этого термина существуют и другие значения, см. Вода (значения). Вода … Википедия
Изоциановая кислота
Содержание
Структура [ править ]
Свойства [ править ]
Физический [ править ]
Кислотность [ править ]
В водном растворе это слабая кислота с p K a 3,7: [12]
Разложение [ править ]
Изоциановая кислота гидролизуется до диоксида углерода и аммиака :
Олигомеризация [ править ]
Стабильность в растворе [ править ]
Разбавленные растворы изоциановой кислоты стабильны в инертных растворителях, например эфире и хлорированных углеводородах. [13]
Реакции [ править ]
Изоциановая кислота реагирует с аминами с образованием мочевины (карбамидов):
HNCO присоединяется через богатые электронами двойные связи, такие как виниловые эфиры, с получением соответствующих изоцианатов.
Таутомерия [ править ]
При низкотемпературном фотолизе твердых веществ, содержащих HNCO, образуется таутомер циановой кислоты HOC≡N, также называемый цианатом водорода. [16] Чистая циановая кислота не была выделена, и изоциановая кислота является преобладающей формой во всех растворителях. [13] Иногда информация, представленная в справочниках для циановой кислоты, на самом деле относится к изоциановой кислоте. [ необходима цитата ]
Подготовка [ править ]
HNCO также может быть получен путем высокотемпературного термического разложения тримера циануровой кислоты:
образуется изоциановая кислота, которая быстро тримеризуется в циануровую кислоту.
Возникновение [ править ]
Изоциановая кислота была обнаружена во многих межзвездных средах. [7]
Caluanie (Окислительный партеризационный термостат, Тяжёлая вода)
Caluanie (Окислительный партеризационный термостат, Тяжёлая вода)
muelear oxidize parteurize
Muelear Oxidize Parteurize Thermostat Harmfu Thermos
Фасовка: 1 л., 5 л. и 25 л.
Изоциановая кислота Общие Хим. формула Рац. формула Физические свойства Молярная масса Плотность Термические свойства Т. плав. Т. кип. Энтальпия образования Удельная теплота испарения Давление пара Химические свойства pKa Структура Кристаллическая структура Классификация Рег. номер CAS PubChem Рег. номер EINECS SMILES InChI ChEBI ChemSpider Безопасность Токсичность
Свойства и реакционная способность
Изоциановая кислота является слабой кислотой ( Ka = 3,47⋅10 −4 в водных растворах), стабильна в растворах в диэтиловом эфире, бензоле и толуоле; в водных растворах гидролизуется с образованием диоксида углерода и аммиака, гидролиз ускоряется в присутствии минеральных кислот:
H N C O + H 2 O → N H 3 + C O 2 <\displaystyle <\mathsf
Атом углерода изоциановой кислоты является электрофильным центром: циановая кислота взаимодействует с такими нуклеофилами, как аммиак, амины и спирты, образуя соответствующие продукты присоединения.
При взаимодействии изоциановой кислоты со спиртами образуются уретаны :
которые с избытком изоциановой кислоты образуют эфиры аллофановой кислоты :
Безводная изоциановая кислота самопроизвольно полимеризуется в твёрдую белую массу, состоящую преимущественно из циамелида — линейного полимера (-O-C(=NH)-)n, и тримера — циануровой кислоты которые при нагревании деполимеризуется с образованием исходной кислоты.
Под действием триэтилфосфина и третичных аминов изоциановая кислота тримеризуется с образованием циануровой кислоты (2,3,5-тригидрокси-сим- триазина ).
Синтез
400 °C, используя очищенную циануровую кислоту (примеси могут привести к взрывному разложению), в промышленности изоциановую кислоту получают каталитическим окислением синильной кислоты при 630—650 °C на контактной сетке из золота.
Цианаты могут быть получены окислением цианидов щелочных металлов: так, при плавлении цианида калия на воздухе происходит его загрязнение образующимся вследствие окисления цианатом калия, окисление цианидов натрия и калия воздухом или кислородом в присутствии никеля является промышленным методом синтеза цианатов. Цианаты натрия и калия также синтезируют сплавлением соответствующих цианидов с оксидом свинца или свинцовым суриком Рb3О4. Пероксид водорода также окисляет цианиды до цианатов.
Токсичность
Изоциановая кислота ядовита, как и все циановые кислоты.