Сухая батарея что это
Сухозаряженный аккумулятор — что это и как его использовать
Как известно, ничто не вечно, и одному из главных элементов автомобиля — АКБ, когда-то приходит время отправляться на покой. Выбирая новый источник питания, автовладельцы могут увидеть сухозаряженный аккумулятор. Что это такое? С какой стороны к нему подойти и как использовать? Как зарядить сухозаряженный аккумулятор? На эти и другие вопросы мы дадим ответы в нашей статье.
Сухозаряженный аккумулятор: что это такое, зачем они производятся и сколько стоят
Этот вид АКБ получил своё название благодаря отсутствию электролита в банках на момент окончания изготовления. Производство сухозаряженных батарей предполагает, что свинцовые пластины заряжены, а само изделие герметично закрыто в заводских условиях. Цена такого источника питания — от 1500 рублей.
Что заливать в сухой аккумулятор? Так как сухозаряженный аккумулятор является обычной свинцово-кислотной батареей, заправлять его следует электролитом. Последний можно, как приобрести в готовом виде в магазине, так и приготовить самостоятельно из кислоты и дистиллированной воды.
Cухозаряженные батареи выпускаются для того, чтобы у владельца была возможность долгосрочного хранения АКБ перед ее первым использованием, например, при складском хранении. Благодаря низкой скорости протекания химических процессов аккумуляторы без электролита практически не подвержены саморазряду. Это позволяет хранить из невероятно долго.
Срок хранения и годности сухозаряженного аккумулятора
Популярность этого вида источников питания связана с тем, что в банках отсутствует электролит, а значит, нет химической реакции. Свинцовые пластины герметично закрыты, на них не воздействуют влага и воздух. Поэтому срок хранения сухозаряженного источника питания для авто в заводском состоянии может достигать 40 лет. Несмотря на продолжительный срок хранения, срок годности сухозаряженной АКБ равен примерно 7 годам. Дело в том, что химический процесс в сухих батареях хоть и значительно замедлен, но все равно протекает. Поэтому после длительного хранения (30—40 лет), возможно, пластины будут в нерабочем состоянии.
Храниться батарея должна в вертикальном положении без прямые солнечные лучи. Также следует проследить за тем, чтобы пробки батареи были закрыты.
Сухозаряженный аккумулятор: ввод в эксплуатацию
Сухозаряженные аккумуляторы нельзя установить на транспортное средство сразу после покупки. Этот фактор зачастую заставляет автовладельцев сделать выбор в пользу привычных батарей. Однако начало эксплуатации сухозаряженного аккумулятора не столь проблематично, как кажется. Перед выполнением работ необходимо подготовить все инструменты: электролит, ареометр, вольтметр и зарядное устройство.
Что заливать в сухой аккумулятор
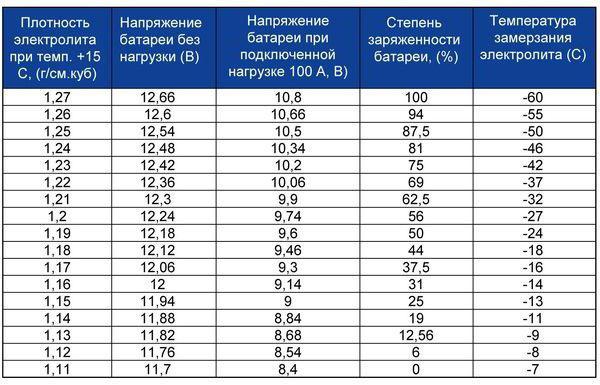
Перед установкой сухозаряженного аккумулятора в него надо залить электролит плотностью 1,27-1,28 г/см куб. Можно приобрести готовый раствор или смешать его самостоятельно.
Как заправить сухозаряженный аккумулятор
Заправлять эту батарею рекомендуется при комнатной температуре и в соответствии со строгим соблюдением последовательности:
Таблица 1. Показания плотности электролита и напряжения батареи в зависимости от степени её заряженности.
Ниже представлены примерный объём электролита для разных аккумуляторных батарей разной емкости.
Минусы и плюсы сухозаряженного аккумулятора
Сухозаряженный аккумулятор — это такой аккумулятор, с отформованными и заряженными во время производства пластинами, но в продажу он отправляется незаполненным электролитом. После того как такой аккумулятор был собран на заводе, его герметично запечатывают пробками во избежание попадания в него влаги и воздуха. Ещё одним плюсом сухозаряженных аккумуляторных батарей является срок их хранения, ведь в таком не заполненном виде их можно содержать 5 лет и причём очень удобно осуществлять транспортировку.
Как Вы уже поняли, такой тип аккумуляторов не готов к эксплуатации сразу же после приобретения. Для того, чтобы аккумулятор сухозаряженного типа привести в эксплуатационное состояние, необходимо проделать некоторые манипуляции.
В первую очередь надо иметь при себе кислотный электролит. Для автомобильных аккумуляторных батарей кислотный электролит – это растворённая в воде серная кислота с плотностью в 1,27 г/см3. Кислотный электролит можно как самостоятельно приготовить, так и купить, что несомненно проще. Электролит заготовить необходимо в большем объёме, чем есть в самой батареи. Во время работы может потребоваться ещё и дистиллированная вода. Во-вторых, Вам понадобиться ареометр для аккумулятора, чтобы проверять плотность кислотного электролита. В-третьих, также «вооружитесь» специальной нагрузочной вилкой или вольтметром. Нагрузочной вилкой Вы будете измерять напряжение аккумуляторной батареи с нагрузкой и без неё. И в последнюю уже очередь Вам нужно будет зарядное аккумуляторное устройство.
Теперь приступаем к подготовке сухозаряженного аккумулятора к эксплуатационному состоянию. Перед заправкой аккумулятора электролитом, его необходимо разгерметизировать. Для этого выньте герметизирующие диски из-под пробок, заглушки по бокам крышки батареи или срежьте приливы на пробках. Заполните аккумуляторную батарею электролитом, соблюдая все меры безопасности. Заливаемый электролит должен быть в температурных рамках от 15 до 30 градусов по Цельсию. Заливаем электролит до максимальной отметки. Если же такие отметки отсутствуют, тогда ориентируйтесь на то, чтобы пластины были погружены в серный раствор на 2 сантиметра. После заливки электролита в аккумуляторную батарею, ее надо оставить на два часа. За это время пластины пропитаются электролитом. Пластины должны пропитаться электролитом около двух часов, после необходимо долить электролит до первоначального уровня. После замерьте напряжение аккумуляторной батареи вольтметром или нагрузочной вилкой без нагрузки. Отталкиваясь от показаний вольтметра, Вы уже решите, что далее делать с аккумулятором: заряжать или нет.
Если напряжение аккумулятора уже пропитанного электролитом будет не меньше или даже больше 12,5 Вольт, значит батарея уже готова к эксплуатации. Если напряжение меньше 12,5, но выше 10,5, следовательно его необходимо подзарядить. А если напряжение меньше 10,5 Вольт, то вероятно, что аккумулятор а негодном состоянии. В том случае, когда аккумулятор готов к эксплуатации, заверните обратно пробки, протрите корпус и очистить клеммы, а затем уже ставьте на свой автомобиль.
Если аккумулятору необходима зарядка, тогда внимательно прочтите далее, как это делать:
Понять, что аккумулятор зарядился можно по следующим признакам:
Как работает сухозаряженный аккумулятор?
Сухозаряженные аккумуляторные батареи занимают больший процент автомобильного рынка аккумуляторов. Ассортимент их очень широк, а стоимость различается в зависимости от компании производителя. В работе и обслуживании эти аккумуляторы не имеют каких-либо жёстких ограничений. Сухозаряженные аккумуляторы оснащаются баком специальной конструкции, который оснащён маленькими крышками, что контролируют уровень электролита. По мере того, как происходит испарение электролита, требуется осуществлять его долив до определённой установленной нормы.
Сухозаряженные батареи хорошо выдерживают повышенное зарядное напряжение и устойчивы к быстрой зарядке. Эти аккумуляторы включают в себя положительные и отрицательные электроды, раствор серной кислоты и сепаратор, который разделяет «минус» и «плюс» пластинчатых элементов. Такие аккумуляторы работают по принципу «установил и забыл», ведь срок их службы может доходить и до 10 лет. Главные характерные особенности таких аккумуляторов – это длительный эксплуатационный срок и нарабатывание количества циклов. Ухудшение параметров аккумуляторных батарей и их поломка происходит, зачастую, из-за коррозийных изменений в решётке и оползания активной консистенции положительного электрода. Эксплуатационный срок сухозаряженных аккумуляторов зависит от типа «плюсовых» пластин и рабочих условий.
Преимущества и недостатки сухозаряженного аккумулятора
Часто, обращаясь в магазине к продавцам-консультантам, мы сталкиваемся с тем, что нам предлагают лишь сухозаряженные аккумуляторные батареи. И это вовсе не пережиток прошлого, ведь такие батареи наделены многими преимуществами, которые мы осветим далее. Но сладкое оставим на потом и выловим ту самую ложку дёгтя – недостатки сухозаряженных аккумуляторов. Первое – это невозможность его работы сразу же после приобретения. Тоесть, поставить АКБ на автомобиль и сразу стартануть двигатель не получится, придётся приложить немного усилий и времени.
Второе – это неудобство, которое мы хотим отметить. Для приведения батареи в рабочее состояние, необходимо смешать серную кислоту и дистиллированную воду, доведя раствор до необходимой плотности, а потом залить в полость батареи. Также может быть вариант использования зарядного устройства, а это снова же лишние 5-7 часов. В-третьих, поговорим о безопасности. Работать с кислотным электролитом необходимо очень и очень осторожно, ведь эта жидкость весьма токсична и может вызвать ожоги слизистой оболочки и кожных покровов.
Итак, с минусами мы разобрались, теперь возьмёмся за разбор положительных моментов, которых явно больше чем недостатков, но назовём три основных положительных момента в использовании сухозаряженных аккумуляторов. Заряженные аккумуляторы без электролита хранятся гораздо дольше, чем с кислотным раствором внутри. В среднем этот срок составляет приблизительно 5-7 лет. Причём для обеспечения надлежащих условий не требуется каких-либо особых мер. Сухозаряженные аккумуляторы можно хранить в любом месте, где нет проникания прямых солнечных лучей. Это достоинство выгодно производителям и продавцам, но и покупатели от этого не окажутся в минусе. Так, например, если Вы приобрели аккумулятор в период сильных морозов ставить её на автомобиль сразу необязательно совсем.
Вы можете на своё усмотрение регулировать плотность. После приобретения батареи Вы самостоятельно можете определить нужную плотность и довести её до необходимого уровня в банках батареи. Он зависит от климатических условий и эксплуатации техники. Осуществлять транспортировку сухозаряженных аккумуляторов гораздо удобнее и безопаснее чем тех, что внутри с электролитом. У них меньше масса, а опасность того, что вытечет электролит, полностью исключена.
Получается, что счёт равный? Не совсем так! Давайте более детально разберём вышеуказанные минусы. Действительно, после того, как Вы приобретёте сухозаряженный аккумулятор и поставить его на автомобиль, завести его не выйдет. Но что Вам может помешать это сделать, например, возле магазина. Неудобно, скажете Вы? Да ничего такого в этом нет, можно приобрести готовую смесь в магазине, а в некоторых комплектах она идёт по умолчанию. Раствор выверен в оптимальной плотности и поставляется в специальных ёмкостях с горлышками, рассчитанными под отверстие в источнике питания. Но ведь это опасно! Да, никто и не спорит! Если Вы не понимаете какими свойствами обладает кислота и пренебрегаете мерами безопасности, тогда это действительно проблема, в результате которой опасность неминуема.
Критерии выбора сухозаряженного аккумулятора?
Мы рады Вам представить 7 основных критериев, по которым следует делать правильный выбор сухозаряженного аккумулятора:
Сухой элемент: Типы, принцип работы. Батарейка. Марганцево-цинковый.
Сухой элемент – тип электрических батарей, часто используемый в портативных электронных устройствах. Он был создан немецким ученым Карлом Гасснером в 1886 году после изобретения влажных марганцево-цинковых элементов Жоржем Лекланше.
Говоря простыми словами, сухой элемент — это батарейка.
Типы сухих элементов
1. Первичный элемент:
2. Вторичный элемент
Первичные элементы не являются перезаряжаемыми, и, в основном, перерабатываются после того, как внутренняя реакция в элементе потребляет реактивные стартовые химикаты.
Вторичные элементы являются перезаряжаемыми и могут использоваться многократно.
Принцип работы сухого элемента, батарейки
Сухой элемент использует активную пасту в качестве электролита, влажности которой достаточно только для движения тока. В отличие от влажного элемента, сухой элемент может работать в любом положении без протечек, так как не содержит свободной жидкости, что делает его подходящим для портативной электроники.
Для сравнения, первые влажные элементы представляли собой хрупкие стеклянные контейнеры со свинцовыми стержнями, свисающими с открытой верхушки и требующими тщательного ухода во избежание утечек. Свинцово-кислые батареи не смогли дать той безопасности и портативности сухих элементов до момента создания гелевых батареи.
Влажные элементы продолжали использовать для высокозатратных отраслей, к примеру – старт двигателей внутреннего сгорания, так как ухудшение тока в электролите приводит к уменьшению возможностей тока.
Распространенным примером сухого элемента является марганцево-цинковый элемент, иногда называемый сухим Элементом Лекланше, стандартное напряжение которого составляет 1,5 В, как и у щелочных элементов (так как у них используется то же сочетание цинка и оксида марганца (IV)).
В состав стандартного сухого элемента входит цинковый анод, обычно – в виде цилиндрического бака, и угольный катод в виде центрального резервуара. Электролитом служит хлорид аммония в виде активной пасты, расположенной сразу после цинкового анода.
Оставшееся между электролитом и угольным катодом пространство занято вторым видом активной пасты, состоящей из хлорида аммония и оксида марганца (IV), где последний выступает в роли деполяризатора. В некоторых конструкциях оксид марганца (IV) заменяется хлоридом цинка.
Видео
История
Многие экспериментаторы пытались лишить подвижности электролит в электрохимическом элементе, чтобы сделать его более удобным для использования. Замбониев столб, созданный в 1812 году, представлял собой сухую батарею высокого давления, способную передавать ток всего лишь несколько минут.
Различные эксперименты проводились с целлюлозой, древесными опилками, стеклянным волокном, асбестом, волокном и желатином.
В 1886 году Карл Гасснер получил немецкий патент (№ 37758) на модификацию (влажного) Элемента Лекланше, который стал известен, как сухой элемент, так как не содержал свободного жидкого электролита.
Вместо него для создания активной пасты были смешаны хлорид аммония и гипс, а для продления срока жизни было добавлено немного хлорида цинка. Катод из оксида марганца (IV) был погружен в эту активную пасту, и все это было запечатано в цинковую оболочку, также выполняющую функцию анода.
В отличие от прежних влажных элементов, сухой элемент Гасснера был гораздо прочнее, не требовал технического обслуживания, не протекал и мог использоваться в любом положении. Он выдавал напряжение в 1,5 В.
Компания улучшила модель Гасснера за счет замены гипса свернутым картоном, что оставило больше места для катода и сделало батарею более легкой в сборке. Эта батарея стала первой стандартной батареей для массового потребления, и сделала портативную электронику реальной.
Марганцево-цинковый элемент (который стал известен под этим названием) все еще производится.
Уникальная статья на нашем сайте — electricity220.ru.
Сухая батарея
Марганцево-цинковый элемент, солевой элемент питания, также известный как элемент Лекланше — это первичный химический источник тока, в котором катодом является диоксид марганца MnO2 (пиролюзит) в смеси с графитом (около 9,5 %), электролитом — раствор хлорида аммония NH4Cl, анодом — металлический цинк Zn.
Является самым известным первичным элементом питания (химический источник тока одноразового использования), который сегодня широко используется в переносных устройствах. Изначально элементы заполнялись жидким электролитом. В дальнейшем электролит стали загущать с помощью крахмалистых веществ — это позволяло сделать более практичные элементы питания, называемые сухими, в которых сведена к минимуму возможность вытекания электролита. В отличие от щелочного элемента, в котором в качестве электролита используется щелочь KOH, марганцево-цинковый элемент является солевым, так как в нем в качестве электролита используется соль — хлорид аммония.
Содержание
История изобретения
Характеристики
Принцип действия
При потреблении тока электроны поступают через внешнюю электрическую цепь с цинкового электрода на угольный стержень. Происходят следующие реакции:
Таким способом избегают поляризации электрода, а диоксид марганца называют деполяризатором. Электролит NH4Cl диссоциирует и частично протолизируется. В общем:
Образующиеся на аноде ионы Zn 2+ поступают в раствор и образуют труднорастворимую соль:
Анод: Zn — 2e − → Zn 2+ Катод: 2MnO2 + 2H3O + + 2e − → 2MnO (OH) + 2H2O Раствор электролита: Zn 2+ + 2NH4 + + 2Cl − + 2H2O ↔ [Zn (NH3)2]Cl2 + 2H3O +
Общая реакция: Zn + 2MnO2 + 2NH4Cl → 2MnO (OH) + [Zn (NH3)2]Cl2 Во время разрядки цинковый стакан растворяется. Во избежание вытекания электролита или продуктов реакции цинковый стакан имеет запас по толщине или окружён железной защитной оболочкой.
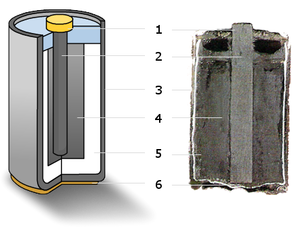
Устройство
В качестве электродов в «сухом элементе» выступают цинковый стакан и угольный стержень. Поэтому сухой элемент называют ещё угольно-цинковым элементом. Положительным электродом «+» является угольный стержень, отрицательным — цинковый стакан. Угольный стержень окружен смесью диоксида марганца MnO2 и угля (сажи). В качестве электролита выступает раствор хлорида аммония NH4Cl с небольшой добавкой хлорида цинка ZnCl2, загущённый крахмалом и мукой — это необходимо для того, чтобы электролит не мог вытечь или высохнуть при хранении и эксплуатации элемента. Тем не менее при неправильной эксплуатации или слишком длительном хранении электролит всё же может потечь или высохнуть.
Производство
Хранение и эксплуатация
Восстановление работоспособности
По мере разрядки цинковый стакан покрывается слоем цинкдиамминхлорида, за счёт чего увеличивается внутреннее сопротивление элемента. Частично восстановить ёмкость элемента можно, если удалить слой цинкдиамминхлорида с поверхности цинкового стакана. Сделать это удаётся несколькими способами:
Второй способ нередко ошибочно называют перезарядкой. Стоит, однако, отметить, что оба способа сопряжены с риском повреждения цинкового стакана и подтекания электролита, а второй способ может также привести к взрыву элемента.
Другой распространённой причиной потери ёмкости является высыхание электролита. Это обычно происходит в тех случаях, когда элемент используется в течение длительного времени в устройствах, потребляющих небольшой ток (например, электронных часах), либо после длительного хранения. В этом случае восстановление работоспособности возможно после шприцевания батарейки водой, однако после необходимо плотно закрыть отверстие, иначе электролит может в скором времени снова высохнуть либо начать подтекать.
Ещё одной известной неисправностью является коррозия (окисление) цинкового стакана. В результате окисления происходит истончение стакана, а также (при окислении контактных площадок) — увеличение сопротивления элемента. Коррозия в дальнейшем может также перекинуться на другие металлические детали, расположенные близко к батарее. Окислившийся элемент восстановлению не подлежит.
Цинковый стаканчик («-» электрод) частично вскрыт, под ней бумажный стаканчик, пропитанный электролитом и залитый битумной мастикой
Цинковый стаканчик удалён, угольный стержень («+» электрод), впрессованный в «+» контакт-крышку, демонтирован
Внутри бумажного стаканчика прессованный марганцево-графитный порошок с каналом для «+» электрода
Области применения
Наиболее эффективной областью применения солевых батареек являются приборы со средним и низким энергопотреблением, например, в ДУ пультах и часах, по причине более медленного саморазряда [ источник не указан 278 дней ] солевой батарейки (в сравнении с щелочными элементами питания).
Сухие батарейки
Когда-то давно, самыми первыми большими партиями стали производить сухие батарейки. По сути это предки ученого Лекланше. Сейчас эти элементы питания самые популярные в мире. Вы только представьте, одна фирма Energizer делает продажи на 6 миллиардов каждый год.
Сухие элементы обладают самой малой удельной энергетической емкостью из всех имеющихся на рынке. Это связано с их низкой стоимостью. Щелочные, марганцево-цинковые и хлорно-цинковые это все сухие батарейки, которые используют в разных электронных приборах. Их названия позволяют нам разобраться в химической структуре.
Данные элементы питания по своей центральной оси имеют угольный стержень. Это так называемый токоотводник катода. По сути катод — это сложная вселенная имеющая электрод, выполненный на основе угля, диоксид марганца и особый электролит.
Анодом у dry battery является цинковый стакан. Так же одновременно он играет роль корпуса батареи. Электролит в нем является загустевающим содержимым. В него входит диоксид марганца, нашатырный спирт и хлорид цинка.
Такие источники энергии как хлорно цинковые и марганцево цинковые различимы между собой только внутренней начинкой в виде электролита. Вторые содержат хлорид цинка и нашатырный спирт. Все это приправлено водой. Первые на сто процентов выполнены из хлорида цинка. По напряжению разница совсем небольшая это 0.05 вольта.
Могут ли сухие батарейки вытягивать современную технику?
Хлорно цинковые обладают повышенной емкостью если их сравнивать с батареями Лекланше. Но данное преимущество исчезает, когда применяется малая нагрузка. На их привлекающей этикетке можно углядеть надпись “heavy-duty”. Это значит сухие батарейки повышенной мощности. Как бы там не было дайте большую нагрузку и мощность данных элементов заметно упадет. В связи с этим современные цифровые фотоаппараты они просто не потянут. Но зато от них будут прекрасно работать фонарики, пульты для телевизора и другая подобная техника.
Щелочные батарейки это по сути и есть угольно-цинковые, то есть сухие накопители энергии из прошлого столетия. Все отличие заключается лишь в специализированной электролитической массе. Именно он позволяет увеличить период хранения и повысить энергетический объем.
Почему же так происходит? Такая смесь более щелочная, чем у 2-х выше указанных разновидностей. Химический состав у щелочных элементов питания почти ничем не отличим от батарей Лекланша. А вот конструкция обладает характерными отличиями.
По сути щелочная батарейка — это сухой элемент, вывернутый наизнанку. Их корпус не равно анод. Он обычная защитная оболочка. В качестве анода выступает густая смесь, состоящая из порошка цинка и электролита. А электролит это водяной раствор гидроксида калия.
Из чего же состоит катод? Его сердцем является диоксид марганца и угля. Он обволакивает электролит и анод. Используя специальные технологии ученые научились отделять его слоем нетканного материала. В качестве него обычно применяют полиэстер.
Сколько же служат сухие батарейки?
На работу оказывает влияние нагрузка прибора. В нетребовательных гаджетах щелочные сухие батарейки могут проработать по времени в пять раз дольше по сравнению с обычными угольными батареями с элементами цинка.
Это очень заметно, когда коротенькие промежутки времени сильным потребителем прерываются долгими периодами неиспользования.
Если вы размышляете о том, что dry battery это аккумулятор или батарейка? То это однозначно батарейки. Поэтому перезаряжать их ни в коем случае нельзя. Все процессы, происходящие в них необратимы. Поместив такой источник энергии, она станет греться и в конечном итоге либо взорвется, либо вообще выйдет полностью из строя.