Токсико анемический синдром в онкологии что это
Рак ободочной кишки
Рак ободочной кишки является наиболее часто встречаемой патологией в онкологической практике и занимает третью позицию среди всех злокачественных раковых образований органов системы пищеварения. Как правило, заболевание поражает различные слои населения, преимущественно в возрастной категории старше 55-ти лет, независимо от половой принадлежности.
Ведущую роль в образовании атипичных клеток играют предраковые патологические процессы в органах системы пищеварения, а также употребляемая пища с низким содержанием клетчатки. К предраковым состояниям относятся полипы (полипоз), хронический неспецифический язвенный колит, дивертикулярная болезнь и болезнь Крона.
Что представляет собой рак ободочной кишки?
В большинстве случаев злокачественное новообразование образуется в результате трансформации полипов, возникших в толстой кишке. Таким образом, своевременное удаление полипов снижает вероятность развития онкологического заболевания и является хирургической профилактикой рака.
Опухоль ободочной кишки формируется в одном из ее отделов:
Несмотря на возможность формирования рака в любом из отделов ободочной кишки, частота поражения в каждом из участков значительно отличается. Так, в 50% случаев опухоль поражает сигмовидную кишку, более 20% приходится на слепую, 10% на поперечную ободочную и около 15% на участки физиологических изгибов кишки. И только в 2% случаях рак первоначально поражает несколько отделов ободочной кишки.
О заболевании
Распространение опухолевых клеток по организму происходит несколькими путями:
Гематогенные метастазы локализуются преимущественно в печени, иногда в легких.
Классификация рака ободочной кишки
Различают несколько клинических проявлений опухолевого процесса и их признаки:
Симптомы рака ободочной кишки
Первые симптомы патологического процесса практически отсутствуют, но при этом отмечается незначительное ухудшение общего самочувствия, снижение активности и аппетита. На ранних этапах развития болезни человек начинает прибавлять в весе.
Симптомы рака ободочной кишки полностью зависят от места расположения опухоли, размеров, степени распространения, наличия других заболеваний ЖКТ и возникающих осложнений.
Клинический комплекс проявляется ощущением болезненности и дискомфорта, запорами либо поносами, кровяными и слизистыми выделениями при опорожнении кишечника, ухудшением самочувствия.
Более подробная характеристика проявляющихся симптомов:
Фото рака ободочной кишки
Диагностика ракового заболевания ободочной кишки
Диагностика рака ободочной кишки состоит из комплекса мероприятий:
Методы лечения рака ободочной кишки
Основным методом лечения рака ободочной кишки является хирургический, иногда с проведением в послеоперационном периоде химиотерапии.
Метод оперативного лечения определяется после проведения соответствующих диагностических мероприятий для выявления степени распространения опухолевого процесса:
После проведения операции в течение первых 24 часов запрещается употреблять пищу, в это время проводится противошоковая терапия, а также мероприятия для устранения интоксикации и обезвоживания организма.
Начиная со второго дня больному разрешается принимать жидкую, полумягкую пищу и употреблять теплое питье. Со временем в дневной рацион включают такие блюда, как нежирные бульоны, протертые каши, пюре из овощей, омлет на пару, чаи на травяных отварах, различные соки и компоты из свежих либо замороженных фруктов и ягод.
Возможные последствия
Рак ободочной кишки — это серьезное заболевание, которое требует оперативного вмешательства. При отсутствии лечения на ранних стадиях существует риск развития осложнений:
Прогноз выживаемости
Прогноз при опухолях ободочной кишки во многом зависит от стадии патологического процесса, распространения атипических клеток на близлежащие органы, ткани и лимфатические узлы, а также от гистологической структуры злокачественного новообразования.
Лечебные мероприятия после операции
Лечение опухолевого процесса после операции продолжается с помощью химиотерапии.
Применение химиотерапии
Основными препаратами являются фторафур и 5-фторурацил. Большинство пациентов переносят лечение хорошо, реже возникают побочные эффект в виде тошноты, аллергических высыпаниях, рвоте и изменений анализа крови.
Анемия и метаболические расстройства у онкологических больных
«ПРАКТИЧЕСКАЯ ОНКОЛОГИЯ» »» Т. 10, № 3 – 2009
А.В. Новик
ФГУ НИИ онкологии им. Н.Н.Петрова, г.Санкт-Петербург
В предыдущих лекциях в рамках Российской школы онкологов уже достаточно подробно разбирались некоторые из указанных синдромов [7, 9, 10]. В этой лекции мы остановимся на синдроме анемии и гипонатриемии.
Синдром анемии
Под анемией понимают снижение уровня гемоглобина ниже 120 г/л [13]. Такое состояние встречается у половины онкологических больных, особенно при распространенном процессе [14]. Злокачественные опухоли легкого и гинекологические раки чаще всего сопровождаются анемией (71 и 63% соответственно).
На основание преобладающего механизма развития синдрома возможно выделение следующих групп анемий [12]: железодефицитные, сидероахрестические (железонасыщенные), железоперераспределительные, В12-дефицитные и фолиеводефицитные, гемолитические, анемии при костно-мозговой недостаточности, анемии при уменьшении объема циркулирующей крови и анемии со смешанным механизмом развития.
Последствия развития анемии для организма заключаются в развитии гемической гипоксии органов и тканей. Описание механизмов её развития и цепи патологических процессов, с ними связанных, выходит за рамки данного обзора. Хотелось бы, однако, кратко отметить роль гипоксии в развитии опухоли. Снижение содержания кислорода менее 1% стимулирует выработку факторов транскирипции, таких как HIF1-α, NFk-b и АР-1[29]. Индуцируемые ими изменения активности генома приводят к адаптации клеток к этому состоянию, стимулируют ангиогенез, блокируют апоптоз и тем самым способствуют стимуляции опухолевого роста, инвазии и метастазированию. Ещё более низкие концентрации кислорода способны оказывать мутагенное действие, усиливать нестабильность генома и, соответственно, вариабельность опухолевых клеток, что является основой для дальнейшей клональной селекции наиболее устойчивых линий. Низкое содержание кислорода в клетке является фактором химио- и радиорезистентности опухоли. Гипоксическое состояние способствует развитию агрессивного фенотипа и является универсальным фактором неблагоприятного прогноза. Таким образом, анемия является независимым прогностическим фактором для целого ряда опухолей, что было подтверждено соответствующими исследованиями [17]. В связи с этим, лечение анемии должно приводить к повышению оксигенации опухоли и таким образом повышать эффект противоопухолевой терапии.
Клиническая картина
Диагностика анемий
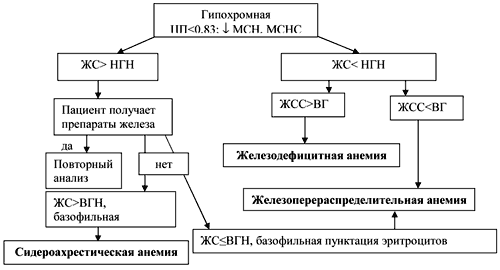
Диагностический алгоритм для гипохромных анемий представлен на рис.1 (по Л.И. Дворецкому, с изменениями) [4].
При выявлении гиперхромных анемий следует прежде всего думать о В12-фолиеводефицитной анемии. Их диагностическими критериями являются высокий цветовой показатель, макроцитоз, мегалоцитоз, эритроциты с остатками ядер (тельца Жолли, кольца Кэбота), ретикулоцитопения, гиперсегментация нейтрофилов, лейкопения (нейтропения), тромбоцитопения, повышение содержания железа в сыворотке, мегалобластическое кроветворение в костном мозге, пониженный уровень данных витаминов в крови. Возможны неврологические нарушения и психические расстройства.
| Рис. 1. Алгоритм диагностики гипохромных анемий. ЦП – цветовой показатель; ЖС – железо сыворотки; ЖСС – железосвязывающая способность сыворотки, YUY – нижняя граница нормы, ВГН – верхняя граница нормы, МСН – среднее содержание гемоглобина в эритроците, МСНС – средняя концентрация гемоглобина в эритроците. |
 |
Лечение анемий
Основой лечения любой анемии, связанной с опухолевым процессом, является лечение самой опухоли. При значительном снижении гемоглобина (менее 80 г/л) пациентам показано проведение гемотрансфузий. Последние позволяют быстро поднять уровень гемоглобина, однако обладают кратковременным эффектом. Переливание эритроцитарной массы сопровождается риском развития целого ряда нежелательных явлений [11]. Выделяют следующие посттрансфузионные реакции и осложнения: острые иммунные (гемолитические, фебрильные негемолитические, аллергические и гемотрансфузионное острое поражение легких); острые неиммунные (бактериальные и вирусные инфекции, циркуляторная перегрузка, физический и/или химический гемолиз, эмболия, цитратная интоксикация, гиперкальциемия); отсроченные иммунные (гемолитические, болезнь «трансплантат против хозяина», посттрансфузионная пурпура) и неимунные (гемосидероз). Уже сам список возможных нежелательных явлений свидетельствует о необходимости ограничения гемотрансфузий и использования их лишь в крайней необходимости. Кроме того, исследования E.C.Vamvakas и H.F. Taswell, в которых изучалось влияние переливания крови на продолжительность жизни больных, выявили увеличение риска смерти в течение 10 лет на 4,1% после переливания 1 дозы эритроцитарной массы [28]. Альтернативные средства лечения анемий зависят от их патогенетического типа. Для анемий, связанных с дефицитом витаминов или железа патогенетической терапией является восполнение такого дефицита. Для В12-дефицитной анемии достаточной терапией в нетяжелых случаях является введение препаратов этого витамина в дозе 100-200 мкг ежедневно в течение 1 недели с последующим переходом на введение через день до достижения полной гематологической ремиссии (нормализация кроветворения и купирование анемии). В тяжелых случаях (снижение эритроцитов менее 1*10 12 /л, неврологическая симптоматика) используется от 300 до 1000 мкг цианкобаламина в течение 2 недель с дальнейшим переходом на поддерживающий режим до достижения стойкой ремиссии. При дефиците фолиевой кислоты последнюю назначают по 3 мг ежедневно на 1 мес.
Для гемолитических анемий, с учетом иммунного механизма их развития, показано применение глюкокортикоидов. При неэффективности такого подхода используют иммунодепрессанты или спленэктомию. Для лечения данного состояния также используют антигормоны (даназол), моноклональные антитела к лимфоцитам (ритуксимаб, алемптузумаб), иммуноглобулины [22]. Описано также применение методов эфферентной терапии [3].
Вместе с тем, проведенные доклинические исследования и изучение роли рецепторов эритропоэтинов на цитоплазматический характер. При культивировании 23 клеточных линий, экспрессирующих на поверхности рецепторы эритропоэтина, стимуляции опухолевого роста выявлено не было. В 23 исследованиях на животных было выявлено 3 вида воздействия эритропоэтинов: 1) торможение опухолевого роста, 2) усиление воздействия стандартной терапии и 3) отсутствие влияния на стандартную терапию. Стимуляции опухолевого роста не было выявлено ни в одном исследовании [19]. Интересно отметить, что при окраске тканей мышей, нокаутных по рецепторам эритропоэтина коммерчески доступными антителами было выявлено позитивное окрашивание. Изучение этого феномена выявило перекрестную реакцию у этих антител с белком теплового шока 70.
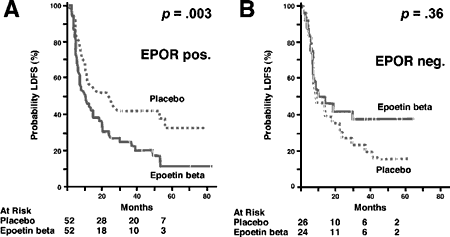
| Рис. 2. Выживаемость больных, получавших терапию рекомбинантным эритропоэтином, в зависимости от экспрессии рецепторов эритропоэтина [19]. |
 |
Таким образом, роль рецепторов эритропоэтинов на негемопоэтических клетках, в том числе на опухолевых, требует дальнейшего выяснения. Тем не менее, клинические данные свидетельствуют о наличии отдельных групп больных, использование эритропоэтинов у которых может существенно ухудшить результаты лечения. В связи с этим, согласно рекомендациям ESMO [26], эритропоэтины могут применяться только у больных с анемией, являющейся осложнением химиотерапии. Начало терапии возможно при гемоглобине ниже 100 г/л (анемия >1 ст.) или при анемии 1 ст., сопровождающейся выраженной клинической симптоматикой. Алгоритм назначения препаратов в соответствии с данными рекомендациями представлен в табл. 1. Необходимо отметить, что у пациентов с потенциально излечимыми опухолями употребления эритропоэтинов следует избегать.
Гипонатриемия
Под гипонатриемией понимают снижение уровня натрия в крови ниже 133 ммоль/л. Это состояние встречается у 3,7-3% онкологических больных и иногда предшествует выявлению опухолевого процесса [23]. Снижение уровня натрия в крови ниже 130 ммоль/л является неотложным состоянием, а уровень ниже 123 ммоль/л опасен для жизни. В нескольких исследованиях этот синдром связывался с повышенной летальностью, при этом частота таких исходов достигала 70% [16]. В связи с этим выявление данного состояния требует выявления его причины и незамедлительного начала коррекции.
Таблица 1. Рекомендации по проведению терапии эритропоэтинами Европейского общества клинической онкологии
Таблица 2. Классификация гипонатриемий и основные причины их развития
| Группа | Механизм развития | Причины |
| 1 | Нормальный баланс натрия | |
| 1а | Избыток АДГ | Избыток АДГ Паранеопластические синдромы Цитостатики (винка алкалоиды, циклофосфамид, ифосфамид и др. алкилирующие агенты) Недостаточность глюкокортикоидов Гипотиреоз |
| 1б | Избыток потребления воды (псевдогипонатриемия) | Опухолевые белки Иммуноглобулины Парапротеины Избыточное введение гипотонических растворов |
| 2 | Нарушение баланса натрия | |
| 2а | Реабсорбция натрия в почках | Снижение ОЦК Нарушения со стороны ЖКТ: Сниженное потребление жидкости Тошнота, рвота Перераспределение жидкости в третьи пространств (асцит, плеврит) Уменьшение эффективного ОЦК Сердечная недостаточность Цирроз печени |
| 2б | Выведение натрия почками | Недостаточность надпочечников Избыток предсердного или мозгового натрийуретического пептида Противоопухолевые препараты (производные платины) |
Кроме того, эту группу нарушений вызывает эктопическая продукция АДГ и аргинин-вазопрессина, наблюдающаяся как компонент паранеопластического синдрома при плоскоклеточных раках головы и шеи, нейроэндокринных опухолях, мезотелиомах, опухолях мочеточников, мочевого пузыря, предстательной железы, эндометрия, цистаденокарциномах, саркоме Юинга [18].
Уменьшение эффективного ОЦК как причина гипонатриемии редко встречается у онкологических больных. Чаще всего, к таким последствиям приводят сердечная недостаточность от использования антрациклинов или развитие нефротического синдрома. Патогенетические механизмы связаны с парадоксальным сокращением ОЦК на фоне гипергидрата и организма, что проявляется отеками, повышенной жаждой, повышенной продукцией АДГ и сниженной клубочковой фильтрацией [23].
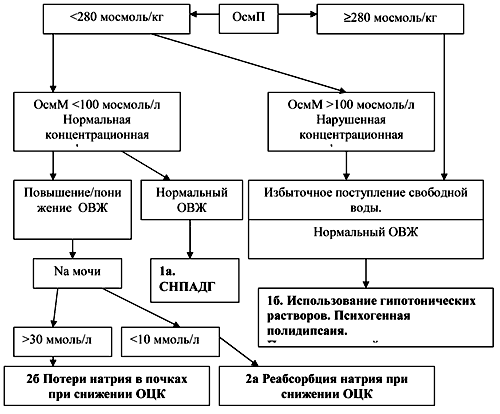
| Рис.3. Алгоритм диагностического поиска при гипонатриемии. ОВЖ – объем внеклеточной жидкости, СНПАДГ – синдром неадекватной продукции антидиуретического гормона, ОЦК – объем циркулирующей крови. |
 |
Диагностика гипонатриемии
Натрий играет важную роль в поддержании осмолярности плазмы крови. В связи с этим на концентрацию натрия влияют 2 основных фактора: распределение жидкости между компартментами (внеклеточным и внутриклеточным) и баланс воды в организме, с одной стороны, и выведение натрия и воды почками, с другой. Сбор анамнеза и определение проводимой лекарственной терапии для выявления потенциальных причин этого нарушения, оценка функции надпочечников, щитовидной железы и сердечно-сосудистой системы чрезвычайно важны для понимания причин гипонатриемии. Из лабораторных показателей особую важность представляют осмолярность (ОсмП) плазмы крови и мочи (ОсмМ) клиренс свободной воды (КСВ). Первые два показателя могут быть определены фактически с помощью приборов осмомометров или рассчитаны по формуле [5]
ОСмП, мосмоль/кг = глюкоза/18 + мочевина/2,8 + 1,86Na
ОсмМ, мосмоль/кг =33,3 х две последние цифры плотности мочи.
Диагностический алгоритм при гипонатриемии включает в себя несколько шагов.
1. Определение острой (до 48 часов) и хронической гипонатриемии. При первой состояние развивается остро, чаще связано с хирургическими манипуляциями. В связи с быстротой развития органы и системы (прежде всего, головной мозг) не успевают достаточно адаптироваться к низкому уровню натрия, что приводит к проявлению клинической симптоматики. Последняя проявляется анорексией, тошнотой, рвотой, запорами, мышечной слабостью, миалгиями, судорогами. Возможно развитие нарушений сознания вплоть до комы, дыхательных нарушений и, вследствие этого, смерти больного [23]. Острая гипонатриемия является неотложным состоянием и требует быстрой коррекции. Хроническая гипонатриемия гораздо реже сопровождается развитием клинической симптоматики. Постепенное нарастание процесса позволяет компенсаторным механизмам приспособиться к пониженному уровню натрия. Такое состояние требует длительной и медленной коррекции, в противном случае возможна быстрая дестабилизация основных жизненных функций.
2. Исключение возможных причин гипонатриемии. Этот этап требует анализа сопутствующей терапии. Важным является определение уровня глюкозы как первичной причины гипонатриемии, поскольку повышение глюкозы на 3 ммоль/л приводит к уменьшению концентрации натрия на 1,6 ммоль/л. Также необходима оценка функции надпочечников, щитовидной железы.
Терапия гипонатриемии включает в себя, помимо попытки устранения её причины, инфузионную терапию с использованием нормотонических и гипертонических растворов, применение диуретиков. Наиболее эффективным считается использование комбинированного подхода, учитывающего скорость развития симптомов и патогенетический вариант процесса [23]. При острой гипонатриймии терапию начинают с введения гипертонического раствора хлорида натрия в/в в течение 13 мин. в дозе 4 мл/кг в сочетании с лазиксом 1 мл/кг [8].
Темп инфузии, мл/час = (0ЦК-с)*300/(Nа]*с
Таким образом, гипонатриемия представляет собой достаточно частое осложнение течения опухолевого процесса и противоопухолевой терапии, требующее немедленной коррекции для улучшения прогноза пациента.
Список использованной литературы
Рак ободочной кишки
Общая информация
Краткое описание
Конфликта интересов нет.
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Клиническая классификация TNM (ICD-O C18-20)
Т – размеры первичной опухоли и степень ее инвазии в стенку кишки.
Тх – недостаточно данных для оценки первичной опухоли.
Т0 – первичная опухоль не определяется.
Tis – интраэпителиальная-преинвазивная карцинома (carcinomainsitu): внутрислизистая или инвазия в собственную пластинку слизистой оболочки (включает раковые клетки до базальной мембраны или в слизистом слое без распространения в подслизистый слой).
Т1 – опухоль инфильтрирует подслизисгую основу.
Т2 – опухоль инфильтрирует мышечный слой стенки кишки.
Т3 – опухоль инфильтрирует в субсерозную основу или в непокрытые брюшиной ткани вокруг толстой либо прямой кишки.
Т4 – опухоль распростаняется на соседние органы или структуры/ткани или в висцеральную брюшину.
Т4а – опухоль прорастает в висцеральную брюшину.
Т4b – опухоль прорастает в другие органы или структуры*.
*Примечания:
1. Непосредственная инвазия при Т4b включает прорастание в другие органы или сегменты толстой кишки и прямой кишки через серозную оболочку, что подтверждается при микроскопическом исследовании, или для опухолей, локализующихся в забрюшинном и подбрюшинном пространствах, а также непосредственную инвазию в другие органы и структуры.
2. Опухоль, которую макроскопически определяют как сросшуюся с другими органами или структурами, классифицируют как сТ4b.
3. Если при микроскопическом исследовании не выявляются элементы опухоли в месте адгезии, то такой случай следует классифицировать как рТ1-3 в зависимости от глубины инвазии в стенку кишки.
N – региональные лимфатические узлы.
Nх – недостаточно данных для оценки региональных лимфатических узлов N0. Нет метастазов в региональных лимфатических узлах.
N0–нет признаков метастатического поражения регионарных лимфатических узлов.
N1–метастазы в 1-3 региональных лимфатических узлах.
N1а – метастаз в 1 региональном лимфатическом узле.
N1b – метастазы в 2-3 региональных лимфатических узлах.
N1с – опухолевые депозиты* в подсерозной основе или в не покрытых брюшиной мягких тканях вокруг толстой кишки и прямой кишки без метастазов в региональных лимфатических узлах
N2 – метастазы в 4 и более региональных лимфатических узлах.
N2a – метастазы в 4-6 региональных лимфатических узлах.
N2b – метастазы в 7 и более региональных лимфатических узлах
* Опухолевые депозиты (сателлиты) – макроскопически или микроскопически выявляемые гнезда или очаги опухолевой ткани в жировой ткани вокруг толстой и прямой кишки, находящейся в области лимфатического дренирования от первичной карциномы при отсутствии ткани лимфатических узлов в этих участках, подтверждаемом при гистологическом исследовании, могут рассматриваться как прерывистое распространение опухоли, инвазия в венозные сосуды с внесосудистым распространением (V1/2) или полное замещение лимфатических узлов (N1/2). Если такие депозиты выявляют при наличии опухоли, то их следует классифицировать.
Примечание. Опухолевые узлы размерами более 3 мм в диаметре в околоободочной и околопрямокишечной жировой ткани с гистологическим обнаружением остатков лимфоидной ткани узла расцениваются как регионарные метастазы в околоободочных или околопрямокишечных лимфатических узлах. Однако опухолевые узлы до 3 мм в диаметре классифицируются как Т-категория, как перемежающееся распространение Т3.
М – отдаленные метастазы.
Мх – недостаточно данных для определения отдаленных метастазов.
М0 – нет отдаленных метастазов.
М1 – есть отдаленные метастазы.
рTNM патоморфологическая классификация
Категории pT, pN и рМ отвечают категориям Т, N и М.
Гистологически должны быть исследованы не менее 12 регионарных лимфатических узлов. Если исследованные лимфоузлы без опухолевого роста, то категория N классифицируются как pN0.
Гистологическая классификация опухолей толстой кишки
2. Слизистая аденокарцинома.
3. Перстневидно-клеточная карцинома.
4. Плоскоклеточная карцинома.
5. Железисто-плоскоклеточная карцинома.
6. Недифференцированная карцинома.
7. Неклассифицируемая карцинома.
Группировка по стадиям
| Стадия | TNM | Распространенность | ||
| Стадия 0 | Tis | N0 | M0 | Carcinoma in situ |
| Cтадия I | T1 | N0 | M0 | Слизистая или подслизистая |
| T2 | N0 | M0 | Собственная мышечная оболочка | |
| Cтадия II | T3 | N0 | M0 | Брюшина/ткани вокруг кишки |
| T4 | N0 | M0 | Перфорация или инвазия в другие органы | |
| Cтадия IIIА | Т1, T2 | N1 | M0 | ≤3 пораженных лимфоузлов |
| Cтадия IIIВ | T3, T4 | N1 | M0 | ≤3 пораженных лимфоузлов |
| Cтадия IIIС | Любая T | N2 | M0 | ≥4 пораженных лимфоузлов |
| Cтадия IV | Любая T | Любая N | M1 | Отдаленные метастазы |
Для червеобразного отростка, слепой кишки, восходящей ободочной кишки регионарными лимфатическими узлами являются периколярные узлы, а также лимфатические узлы, расположенные вдоль подвздошно-ободочной, правой толстокишечной и правой ветви средней толстокишечной артерии.
Для печеночного изгиба ободочной кишки и проксимальной части поперечной ободочной кишки регионарными лимфатическими узлами являются вышеперечисленные, а также узлы, расположенные вдоль средней толстокишечной артерии.
Диагностика
Диагностические критерии
Жалобы и анамнез
Желудочный дискомфорт (потеря аппетита, отрыжка, иногда рвота, чувство тяжести в верхней половине живота). Эти симптомы чаще наблюдаются при поражении поперечной ободочной кишки, ее правой половины, реже – при левосторонней локализации опухоли.
Кишечные расстройства (запоры, поносы, чередование запоров с поносами, урчание и вздутие живота). Эти симптомы расстройства кишечного пассажа чаще всего наблюдаются при левосторонней локализации опухоли. Конечным этапом нарушения кишечного пассажа является развитие обтурационной кишечной непроходимости.
Патологические выделения в виде крови, слизи, гноя во время акта дефекации – частое проявление рака дистальных отделов сигмовидной кишки.
Нарушение общего состояния больных выражающееся общим недомоганием, повышенной утомляемостью, слабостью, похуданием, лихорадкой, бледностью кожных покровов и нарастающей анемией. Все эти общие симптомы заболевания связаны с интоксикацией организма от распадающейся опухоли и инфицированного кишечного содержимого. Токсико-анемический синдром является наиболее характерным для рака правой половины ободочной кишки. Он обусловлен функциональной особенностью (всасывательной способностью) слизистой этого отдела толстой кишки.
Наличие пальпируемой опухоли редко бывает первым симптомом заболевания, ему, как правило, предшествуют другие симптомы. Тем не менее, пальпаторное определение опухоли зачастую служит основанием для постановки правильного диагноза.
Физикальное обследование
Совершенствование методов клинического обследования больного с применением современной рентгенологической и эндоскопической техники, использование широкого арсенала скриннинговых методов диагностики до последнего времени существенно не улучшило раннее выявление рака ободочной кишки. Более чем 70% больных раком ободочной кишки на момент госпитализации имеют III и IV стадии заболевания. Только 15% из них обращаются к специалисту в сроки до 2 месяцев с момента появления первых симптомов заболевания. Менее чем у половины больных диагноз устанавливают в сроки до 2 месяцев от начала заболевания.
Диагноз рака ободочной кишки устанавливают на основании инструментальных (рентгенологического и эндоскопического) методов исследований.
Тем не менее, не менее важными являются клинические методы:
— жалобы пациента позволяют выявить симптомы, связанные с недостаточностью переваривания, всасывания, кишечным дискомфортом, патологическими выделениями;
— анамнез – здесь могут быть получены данные о наличии семейного полипоза, колита или других предшествующих заболеваний;
— данные объективного исследования: осмотр, пальпация и перкуссия живота, позволяющая не только выявить опухоль в брюшной полости, но и оценить ее консистенцию, размеры, мобильность;
— пальцевое исследование прямой кишки.
Инструментальные исследования
При подозрении на рак ободочной кишки необходимо немедленно направить пациента на углубленное комплексное обследование, включающее рентгенологический, эндоскопический методы с биопсией. Схематично алгоритм действий можно представить следующим образом: Опрос → Осмотр → R-исследование → Эндоскопия → Биопсия.
Рентгенологические исследования наряду с колоноскопией, является ведущим в диагностике рака ободочной кишки.
Эндоскопическое исследование позволяет, наряду с визуализацией злокачественной опухоли, получить материал для гистологического исследования, являющегося необходимым атрибутом предоперационной диагностики злокачественного новообразования. Наиболее простым и широко распространенным методом эндоскопического исследования толстой кишки является ректороманоскопия при которой возможно оценить состояние дистального отдела кишечной трубки.
При выполнении ректороманоскопии исследователь оценивает состояние слизистой оболочки толстой кишки, сосудистый рисунок, наличие патологических примесей в просвете кишки, эластичность и подвижность кишечной стенки. При выявлении опухоли толстой кишки изучают ее размеры, внешний вид, консистенцию, подвижность при инструментальной пальпации, производят биопсию опухоли для микроскопического исследования, позволяющего определить гистогенез опухоли толстой кишки.
С целью уточнения распространенности опухолевого процесса в малом тазу, а именно выхода опухоли за пределы стенки кишки, выявления метастазов в лимфатических узлах применяют дополнительные методы исследования (компьютерная томография, магнитно-резонансная томография, лапароскопия).
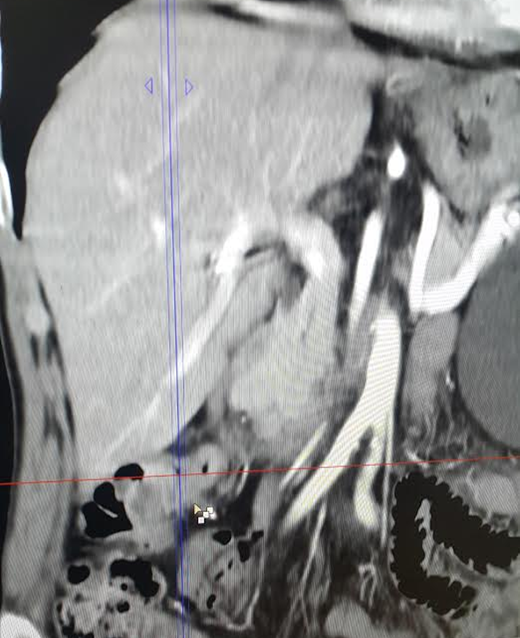
Одним из наиболее информативных из доступных методов выявления отдаленных метастазов в печени и забрюшинных лимфоузлах является компьютерная томография. С ее помощью выявляют метастазы в печени, воротах печени размерами более 1 см, портальных, парааортальных лимфатических узлах.
Одним из наиболее чувствительных и информативных методов выявления «маленьких» опухолей, рецидивов, микрометастазов является протонно-эмиссионная томография (ПЭТ).
Комплексное обследование больных раком ободочной кишки позволяют уточнить степень распространения опухоли, избрать оптимальный метод лечения, определить объем операции и оценить прогноз.
Основные диагностические мероприятия
На догоспитальном этапе:
— общий анализ крови, общий анализ мочи;
— биохимический анализ крови (общий белок, мочевина, билирубин, глюкоза);
— коагулограмма;
— группа крови и резус-фактор;
— ЭКГ;
— пальцевое исследование прямой кишки;
— ирригоскопия;
— колоноскопия с биопсией опухоли;
— рентгенологическое исследование легких;
— ультразвуковое исследование органов брюшной полости, забрюшинного пространства.
Дополнительные диагностические мероприятия
Лапароскопия, ангиография, МРТ, КТ, сцинтиграфия костей скелета, ИГХ-исследование, ПЭТ-исследование, молекулярно-генетическое определение статуса гена KRAS.
Лабораторная диагностика
Дифференциальный диагноз
Лечение
Схемы лечения больных раком ободочной кишки в зависимости от стадии заболевания
Режимы:
| Схема химиотерапии | Схема таргетной терапии |
| FOLFOX | Бевацизумаб 5,0 мг/кг, в/в, 30-90 минутная инфузия, 1 раз в 2 недели |
| FOLFIRI | |
| IFL | |
| De Gramon | |
| Rosvell Park | |
| XELOX | Бевацизумаб 7,5 мг/кг, в/в, 30-90 минутная инфузия, 1 раз в 3 недели |
| XELIRI |
| Схема химиотерапии | Схема таргетной тарпии |
| FOLFOX | |
| САPOX | |
| FOLFIRI | |
| XELIRI | |
| UFT/LV | |
| Иринотекан 350мг/м2, в/в, 1-й день. Повторять курс каждые 3 недели. | |
| Монорежим | |
| XELOX | Цетуксимаб не назначается |
| FLOX |
Примечание. Сочетание моноклональных антител к EGFR и к VEGF ухудшает результаты лечения и допустимо только в рамках специальных исследований.
Госпитализация
Информация
Источники и литература
Информация
Организационные аспекты внедрения протокола
Критерии оценки для проведения мониторинга и аудита эффективности внедрения протокола (четкое перечисление критериев и наличие привязки с индикаторами эффективности лечения и/или создание специфических для данного протокола индикаторов):
1. Процент вновь выявленных пациентов со злокачественным новообразованием ободочной кишки, получающих начальное лечение в течение двух месяцев после начала заболевания = (Количество пациентов, с установленным диагнозом рака ободочной кишки, получающих начальное лечение в течение двух месяцев после начала заболевания/Все пациенты с впервые установленным диагнозом рака ободочной кишки) х 100%.
2. Процент онкологических больных, получающих химиотерапию в течение двух месяцев после проведения оперативного лечения = (Количество онкологических больных, получающих химиотерапию в течение двух месяцев после проведения оперативного лечения/Количество всех больных раком ободочной кишки после проведения оперативного лечения, которым требуется проведение химиотерапии) х 100%.
3. Процент рецидивов рака ободочной кишки у пациентов в течение двух лет = (Все пациенты с рецидивами рака ободочной кишки в течение двух лет/Все прооперированные пациенты с диагнозом рака ободочной кишки) х 100%.
Рецензенты:
1. Кожахметов Б.Ш. – зав. каф. онкологии Алматинского государственного института усовершенствования врачей, д.м.н., проф.
2. Абисатов Г.Х. – зав. каф. онкологии, маммологии Казахстанско-Российского медицинского университета, д.м.н., проф.
Результаты внешнего рецензирования: положительное решение.