Триаксон и цефтриаксон чем отличается
Стратегические подходы к выбору цефалоспориновых антибиотиков при инфекциях дыхательных путей
Проблема рациональной антибиотикотерапии остается одной из самых сложных в клинической практике. Если ранее врач в вопросе выбора лекарственного препарата ориентировался на его эффективность, переносимость и безопасность, то сегодня этого оказыва
 |
Проблема рациональной антибиотикотерапии остается одной из самых сложных в клинической практике. Если ранее врач в вопросе выбора лекарственного препарата ориентировался на его эффективность, переносимость и безопасность, то сегодня этого оказывается недостаточно. Фактор удобства приема препарата и, что особенно непривычно для нашего понимания, вопросы цены и стоимости лечения в условиях серьезного ограничения финансирования здравоохранения часто могут оказаться определяющими. На приобретение лекарственных средств лечебные учреждения тратят 15–20% своего бюджета, причем 50–60% этих расходов приходится на долю антибактериальных препаратов, что заставляет пересмотреть существующие и искать новые подходы к их применению.
Путаница, возникающая при использовании различных антибактериальных препаратов, в том числе и цефалоспориновых антибиотиков (ЦА), связана с недопониманием или просто незнанием основных принципов клинической химиотерапии. В связи с этим мы хотели бы остановиться на некоторых ошибках и «заблуждениях» практикующих врачей, возникающих при назначении антибактериальных препаратов, на примере ЦА, а также определить их место в лечении инфекции дыхательных путей.
Часто от практикующих врачей приходится слышать о безусловных преимуществах IV поколения препаратов перед III, III поколения перед II и т. д. Это абсолютно неверно. Такая точка зрения приводит к использованию «резервных» и мощных препаратов при лечении банальной инфекции, способствует развитию резистентности, а значит, лишает возможности применять препараты первых поколений и, наконец, вызывает значительное и неоправданное увеличение стоимости курса лечения.
ЦА занимают одно из важных мест в лечении инфекций верхних и нижних дыхательных путей. Наиболее ответственным этапом в антибактериальной терапии данной категории пациентов является выбор первоначального препарата. От адекватности выбора зависит эффективность и безопасность лечения, а также его комфортность, переносимость, стоимость, эпидемиологическая ситуация.
Анализ имеющихся данных об использовании ЦА в России за 1997–1998 гг. позволяет выявить предпочтения врачами того или иного препарата (группы препаратов) и определенных методов его введения. Как видно из рис. 1, при назначении цефалоспориновых антибиотиков подавляющее большинство врачей выбирают парентеральные препараты.
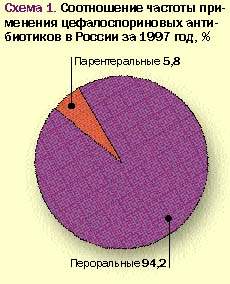 |
Данный факт лишь подтверждает, что в нашей стране пероральные лекарственные средства, и особенно пероральные цефалоспорины, очень мало популярны и практически не используются. Такое отношение к таблетированным формам отражает некоторый консерватизм практических врачей, связанный с тем, что еще 15-20 лет назад существовавшие тогда пероральные средства не выдерживали сравнения с парентеральными препаратами ни по эффективности терапии, ни по ее переносимости. Лишь последние десятилетия с момента создания первого перорального цефалоспорина — цефалексина и появления новых пероральных бактерицидных препаратов эта лекарственная форма несколько укрепила свои позиции не только в амбулаторной, но и в стационарной практике. Однако радикально на положении дел это не сказалось.
Очевидно, что такая форма назначения препаратов имеет безусловные преимущества. Это проявляется и в возможности амбулаторного ведения больного, и в удобстве приема препарата, и в снижении риска постинъекционных осложнений и длительности пребывания в стационаре, и даже в избавлении от психологического дискомфорта, связанного с инъекциями.
Наличие антибактериальных препаратов в двух формах — для парентерального и перорального применения — делает возможным их использование для проведения так называемой ступенчатой терапии. Суть такого лечения состоит в назначении внутривенного или внутримышечного препарата и в последующем, через двое-трое суток после достижения клинического эффекта, переводе на пероральный прием. Возможность проведения ступенчатой терапии одним и тем же препаратом является существенным преимуществом данного лекарственного средства перед его аналогами. Ступенчатая терапия предоставляет клинические и экономические преимущества как пациенту, так и лечебному учреждению.
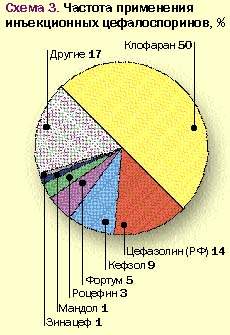
На основании приведенных данных трудно понять логику выбора цефалоспоринового антибиотика того или иного поколения и принципы, которыми руководствуется врач при назначении препарата. Анализ использования цефалоспориновых антибиотиков по поколениям (см. рис. 2 и 3) свидетельствует о предпочтительном назначении препаратов I и III поколений, причем из препаратов III поколения (61%) половина приходится на цефотаксим, а из препаратов I поколения большая часть приходится на цефазолин.
 |
В клинической практике врач начинает проводить антибактериальную терапию, в большинстве случаев не имея результатов микробиологической верификации инфекционного агента, а зачастую и без перспектив получения такого рода данных. Поэтому при выборе антибактериального препарата по-прежнему приходится ориентироваться на сведения, полученные из литературы, данные микробиологического мониторинга, а также на особенности клинической ситуации. Все это позволяет с большей или меньшей долей вероятности определить этиологический инфекционный агент с учетом клинической формы инфекции дыхательных путей (пневмония, хронический бронхит, синусит и т. д.), возраста (дети, старики), сопутствующих заболеваний (сахарный диабет, хроническая алкогольная интоксикация, лечение глюкокортикоидами и цитостатиками). Необходимо также иметь в виду особенности развития инфекции в амбулаторных условиях или в стационаре (лечение по поводу другого заболевания, пребывание в реанимации) при соответствующей эпидемиологической ситуации. Следует отметить, что при выборе препарата важно отличать «госпитальную», или нозокомиальную инфекцию, возникшую спустя двое суток после поступления в стационар, от «амбулаторной» инфекции, долечиваемой в стационаре. В последнем случае тактика антибактериальной терапии должна существенно отличаться.
Таким образом, ориентировочная этиология бронхолегочной инфекции служит основанием для выбора среди ЦА конкретного препарата (или поколения препаратов) с соответствующей антимикробной активностью.
У больных с амбулаторной инфекцией верхних и нижних дыхательных путей, основными возбудителями которых являются стрептококки, Н. influenzae, Moraxella catarrhalis, — препаратами выбора могут быть ЦА I или II поколения. В амбулаторных условиях предпочтение следует отдавать оральным цефалоспоринам (цефаклор, цефуроксим аксетил, цефтибутен). В то же время необходимо иметь в виду недостаточную активность ЦА в целом в отношении атипических бактерий (8–35% в этиологии «домашней» пневмонии) и некоторых анаэробных микроорганизмов, вероятность влияния которых увеличивается у больных с хроническими синуситами и отитами.
При обострениях хронического бронхита особое значение приобретают препараты, высокоустойчивые к действию b-лактамаз, продуцируемых как грамотрицательными, так и грамположительными микроорганизмами (цефуроксим аксетил), и обладающие высокой активностью против Н.influenzae (цефтибутен).
 |
При выявлении показаний для госпитализации больных с «домашней» инфекцией, подразумевающих более тяжелое течение, чаще обнаруживаются Streptococcus pneumonia, Staphylococcus aureus, Н.influenzae и Еntеrobacteriacea. В этом случае более обосновано назначение парентеральных цефалоспоринов II поколения (цефуроксим, цефамандол). Однако именно в таких ситуациях чаще всего и допускаются ошибки: при госпитализации больного в стационар с «домашней» пневмонией нередко назначают бензилпенициллин, аминопенициллины и ЦА I поколения (малоэффективные ввиду высокой резистентности патогенной флоры), либо, для «перестраховки» и при наличии в стационаре, ЦА III поколения (цефотаксим, реже цефтриаксон). Однако более обосновано — и это определяется спектром активности препарата — назначение ЦА II. Среди больных, получающих терапию в стационаре по поводу инфекций нижних дыхательных путей, преобладают нетяжелые случаи. Поэтому идеология назначения ЦА II поколения в качестве «стартовых» препаратов должна доминировать как с позиции адекватной клинической эффективности, экономической целесообразности, так и с позиции сохранения резерва в более тяжелых ситуациях.
Выбор ЦА в качестве первоначального антибиотика при внебольничной пневмонии у больных моложе 60 лет без сопутствующей патологии следует считать, по-видимому, не всегда оправданным. Это обусловлено этиологически широким спектром пневмоний в данной ситуации, который может включать не только пневмококки и Н.influenzae, но и так называемые атипичные возбудители — Мусорlаzma pneumоniaе, Legionella, Chlamidia pneumоniaе, которые не чувствительны к цефалоспоринам всех генераций. Между тем рациональная эмпирическая антибактериальная терапия бронхолегочных инфекций, в том числе пневмоний, должна предусматривать выбор препарата, по возможности активного против всех вероятных в данной ситуации возбудителей. К сожалению, сегодня трудно назвать препарат, полностью удовлетворяющий этим требованиям, за исключением нового поколения фторхинолонов или «респираторных» фторхинолонов. Некоторые из них — например, грепафлоксацин — проходят сейчас в нашей стране регистрацию. В случаях назначения ЦА при данном варианте пневмоний предпочтение следует отдавать ЦА I и II поколения. Применение в подобных ситуациях ЦА III поколения нерационально ввиду высокого риска развития резистентности. Выбор конкретного препарата среди ЦА I–II поколения должен осуществляться исходя из преимущества лекарственных форм, фармакокинетических свойств, стоимости и др. При нетяжелых пневмониях возможно назначение оральных цефалоспоринов. При этом необходимо иметь в виду их различную противомикробную активность по отношению к различным микроорганизмам. Так, например, цефтибутен обладает наибольшей активностью в отношении Н.influenzae, а цефуроксим аксетил — в отношении S.аureus.
Общие принципы выбора первоначального ЦА сохраняются и у больных пневмонией на фоне тяжелых сопутствующих заболеваний (ХОЗЛ, сердечная недостаточность, сахарный диабет, алкогольная интоксикация и др.) и в возрасте старше 60 лет. Этиологическое значение в данной клинической ситуации приобретают Н.influenzae, S.аureus, некоторые грамотрицательные микроорганизмы (Е.соli, Сlebsiella), возрастает частота бета-лактамазопродуцирующих бактерий. В связи с этим возрастает значение препаратов, активных в отношении названных возбудителей. Известно, что противомикробное действие ЦА при переходе активности от первого поколения к последующим характеризуется снижением противостафилококковой активности и преобладанием активности против некоторых грамотрицательных микроорганизмов. Ценным свойством является устойчивость ЦА II поколения к b-лактамазам. В связи с этим врач должен ориентиро-ваться в данной ситуации на цефалоспорины II или по крайней мере III поколения.
Иной подход, определяющий выбор ЦА для лечения бронхолегочной инфекции, наблюдается у больных с «госпитальной» инфекцией. Госпитальные пневмонии занимают особое место среди всех внутрибольничных инфекций из-за тяжести течения и трудностей терапии. Основными возбудителями госпитальных пневмоний являются грамотрицательные микроорганизмы семейства Еntеrobacteriacea — Сlebsiella, Protei, Enterobacter, Providencia, Serracia, а также Staphylococcus аureus, как чувствительный, так и устойчивый к метициллину. Вероятность этиологической роли того или иного инфекционного агента при госпитальных пневмониях определяется особенностями клинической ситуации (послеоперационный период, пребывание в реанимации, искусственная вентиляция легких и т. д.). У больных реанимационных и ожоговых отделений, с иммунодефицитами и муковисцидозом основным микроорганизмом бактериальных осложнений является синегнойная палочка, выявляемая в 70–95% случаев. Наряду с ней у таких больных высевается золотистый стафилококк или гемофильная палочка, устойчивая к ЦА II–III поколения. Основное место в лечении госпитальных пневмоний среди ЦА занимают препараты III (цефтазидим, цефоперазон) и IV поколений (цефпиром, цефепим). С учетом вероятности этиологической роли Pseudomonas aeruginoza в соответствующих ситуациях (ИВЛ, наличие трахеостомы, предшествующая глюкокортикоидная терапия) назначаемые ЦА должны обладать антисинегнойной активностью. Среди имеющихся в распоряжении врача ЦА наибольшей активностью в отношении Pseudomonas aeruginoza обладают цефалоспорины III поколения (цефтазидим, цефоперазон) и IV поколения (цефпиром), которые, однако, не имеют серьезных преимуществ в отношении синегнойной палочки перед цефтазидимом. Появление в терапевтическом арсенале ЦА IV поколения расширяет возможности антибактериальной терапии госпитальных пневмоний с высокой вероятностью грамотрицательной флоры, в том числе золотистого стафилококка, и могут рассматриваться как препараты ургентных ситуаций.
| Цефалоспорины, открытые более 50 лет тому назад, продолжают занимать прочные позиции в лечении различных бактериальных заболеваний, несмотря на появление новых антимикробных средств. Цефалоспориновые антибиотики подразделяются на четыре поколения, отличающиеся по спектру действия, антибактериальной активности, стабильности в присутствии b-лактамаз, фармакокинетическому профилю. Все это наряду с многообразием лекарственных форм и стоимостью определяет их различные показания. Очевидно, что по мере появления новых поколений цефалоспориновых антибиотиков в клинической практике возникает немаловажная проблема дифференцированного назначения препарата с учетом свойств как самого антибиотика, так и особенностей инфекционно- воспалительного процесса у конкретного больного |
Таким образом, рациональный выбор первоначального ЦА для лечения инфекций верхних и нижних дыхательных путей определяется в первую очередь вероятностью этиологической роли того или иного микроорганизма в конкретной клинической ситуации. Такой подход требует от практического врача (а именно от него зависит адекватный выбор препарата) умения выявлять особенности каждого случая пневмонии (эпидемиологическую обстановку, фоновую патологию, факторы риска и др.) и ориентировки в антимикробном спектре назначаемого антибиотика. Однако в клинической практике при выборе ЦА, как, впрочем, и других антибиотиков, приходится наряду с ориентировочной этиологией бронхолегочной инфекции учитывать и другие факторы. Среди последних имеет значение фармакокинетика препарата, наличие разнообразных лекарственных форм, риск развития побочных эффектов, стоимость и др.
В настоящее время не окончательно определено место пероральных препаратов III поколения в клинической практике, так как их сравнительная клиническая и бактериологическая эффективность мало отличается от препаратов II поколения. Более того, как было сказано выше, преимущество цефалоспоринов III поколения состоит в их высокой активности в отношении b-лактамазопродуцирующих бактерий, наиболее часто вызывающих серьезные стационарные инфекции. Но поскольку в этом случае больные находятся в стационаре, то уже более обоснованно получают парентеральную терапию. В то же время ввиду сниженной активности в отношении грамположительных бактерий, часто являющихся причиной именно амбулаторной инфекции, назначение препаратов III поколения имеет меньше преимуществ перед препаратами II поколения.
Цель антибактериальной терапии состоит не только в достижении клинического эффекта, но и в полной эрадикации возбудителя, т. е. бактериологической эффективности. Это в основном определяется адекватным дозированием препарата для достижения необходимой концентрации в очаге инфекции. Высокая степень накопления препарата в тканях является необходимым требованием к лекарственному веществу.
ЦА первого поколения хуже проникают в ткани, что уменьшает степень бактериальной эрадикации.
Данные о биодоступности оральных ЦА следует иметь в виду при дифференцированном назначении их больным с сопутствующей патологией кишечника, связанной с нарушением всасывания, а также при одновременном приеме антисекреторных препаратов, антацидов, с учетом влияния пищи на всасывание ЦА.
Знание путей элиминации ЦА наряду с оценкой функционального состояния печени и почек (возраст, сопутствующая патология) также может определять выбор более адекватного для данной ситуации препарата. Выбирая ЦА для лечения тяжелых госпитальных пневмоний, например, у новорожденных и стариков или у больных с патологией почек, при наличии почечной недостаточности предпочтение следует отдать цефоперазону с учетом его преимущественно билиарной экскреции.
При дифференцированном выборе ЦА необходимо учитывать риск развития побочных эффектов. Наиболее типичны реакции гиперчувствительности (лихорадка, кожная сыпь), гематологические синдромы (цитопения, эозинофилия), нарушения со стороны желудочно-кишечного тракта (тошнота, рвота, диарея), печени (повышение активности трансаминаз), почек (повышение уровня креатинина), ЦНС (головная боль), флебиты при внутривенном введении. Поэтому анамнестические и клинико-лабораторные данные о наличии у больных какой-либо патологии должны влиять на выбор соответствующего препарата.
Флебиты часто возникают при введении цефалотина, цефотаксима, цефепима. Цефуроксим, цефоперазон, цефтибутен могут вызывать анемию (чаще гемолитическую), а при назначении цефалотина, цефамандола, цефотаксима, цефтазидима иногда выявляются фиксированные на эритроцитах антитела. Повышение активности печеночных ферментов возможно на фоне лечения цефоперазоном, цефтриаксоном, цефтазидимом, цефуроксимом. Уровень креатинина может повышаться при лечении цефалексином и цефподоксимом. Оральные цефалоспорины чаще всего вызывают нарушения со стороны желудочно-кишечного тракта (тошнота, рвота, диарея). При лечении парентеральными ЦА отмечено увеличение протромбинового времени, за исключением цефтазидима, не влияющего на синтез факторов протромбинового комплекса и показатели свертываемости крови. Возможны реакции гиперчувствительности (кожная сыпь, лихорадка, эозинофилия) на фоне применения почти всех ЦА III поколения.
Таким образом, дифференцированный выбор ЦА для лечения инфекций верхних и нижних дыхательных путей должен базироваться на учете и адекватной оценке многих факторов, включающих как особенности клинической ситуации, так и антимикробную активность и фармакокинетические характеристики назначаемого препарата.
ИНСТРУКЦИЯ
по медицинскому применению лекарственного препарата
Торговое наименование препарата
Международное непатентованное наименование
Лекарственная форма
порошок для приготовления раствора для внутривенного и внутримышечного введения
Состав
Один флакон с порошком для приготовления раствора для внутривенного и внутримышечного введения содержит:
Описание
Фармакотерапевтическая группа
Код АТХ
Фармакодинамика:
Бактерицидная активность цефтриаксона обусловлена подавлением синтеза клеточной стенки.
In vitro цефтриаксон обладает широким спектром действия в отношении грамотрицательных и грамположигельных микроогранизмов. Он высокоустойчив к большинству β-лактамаз (как пенициллиназ так и цефалоспориназ) вырабатываемых грамположительными и грамотрицательными бактериями.
Цефтриаксон обычно активен в отношении следующих микроорганизмов.
Грамположительныеаэробы
Staphylococcus aureus (мстициллиночувствительный) коагулазо-отрицательные стафилококки Streptococcus pyogenes (β-гемолитический группы A) Streptococcus agalactiae (β-гемолитический группы В) β-гемолитические стрептококки (группы ни А ни В) Streptococcus viridans Streptococcus pneumoniae.
Примечание. Метициллиноустойчивые Staphylococcusspp. резистентны к цефалоспоринам в том числе к цефтриаксону. Как правило EnterococcusfaecalisEnterococcusfaecium и Listeriamonocytogenes также устойчивы.
Грамотрицательные аэробы
AcinetobacterIwoffiiAcinetobacteranitratus (главным образом A. baumannii)* AeromonashydrophilaAlcaligenesfaecalisAlcaligenesodorans алкалигеноподобные бактерии BorreliaburgdorferiCapnocytophagaspp. Citrobacterdiversus (в том числе C. amalonaticus) Citrobacterfreundii* EscherichiacoliEnterobacteraerogenes* Enterobactercloacae* Enterobacterspp. (прочие)* HaemophilusducreyiHaemophilusinfluenzaeHaemophilusparainfluenzaeHafniaalveiKlebsiellaoxytocaKlebsiellapneumoniae** Moraxellacatarrhalis(ранее называвшаяся Branhamellacatarrhalis) MoraxellaosloensisMoraxellaspp. (прочие) Morganella morganii Neisseria gonorrhoeae. Neisseria meningitidis Pasteurella multocida Plesiomonas shigelloides Proteus mirabilis Proteus penneri* Proteus vulgaris* Pseudomonas fluorescens* Pseudomonas spp. (прочие) Providencia rettgeri* Providencia spp. (прочие) Salmonella typhi Salmonella spp. (нетифоидные) Serratia marcescens* Serratia spp. (прочие)* Shigella spp. Vibrio spp. Yersinia enterocolitica Yersinia spp. (прочие).
* Некоторые изоляты этих видов устойчивы к цефтриаксону главным образом вследствие образования β-лактамаз кодируемых хромосомами.
Примечание. Многие штаммы вышеуказанных микроорганизмов полирезистентные к другим антибиотикам таким как аминопенициллины и уреидоненициллины цефалоспорины первого и второго поколения и аминогликозиды чувствительны к цефтриаксону. Treponoma pallidum чувствительна к цефтриаксону in vitro и в экспериментах на животных. Клинические испытания показывают что цефтриаксон обладает хорошей эффективностью в отношении первичного и вторичного сифилиса. За очень небольшими исключениями клинические изоляты Р.aeruginosa устойчивы к цефтриаксону.
Анаэробы
Bacteroidesspp. (желчечувствительные)* Clostridiumspp. (кроме С. difficile) Fusobacterium nucleatum Fusobacterium spp. (прочие) Gaffkya anaerobica (ранее называвшаяся Peptococcus) Peptostreptococcus spp.
* Некоторые изоляты этих видов устойчивы к цефтриаксону из-за образования β-лактамаз. Примечание. Многие штаммы β-лактамазообразующих Bacteroidesspp. (в частности В. fragilis) устойчивы. Устойчив и Clostridiumdifficile.
Чувствительность к цефтриаксону можно определять диско-диффузионным методом или методом серийных разведений на агаре или бульоне используя стандартную методику подобную той которую рекомендует Институт клинических и лабораторных стандартов (ИКЛС). ИКЛС установил следующие критерии оценки результатов пробы для цефтриаксона:
Ошибки в антибактериальной терапии инфекций дыхательных путей в амбулаторной практике
Проблема рациональной антибактериальной терапии инфекций дыхательных путей не теряет актуальности и в настоящее время. Наличие большого арсенала антибактериальных препаратов, с одной стороны, расширяет возможности лечения различных инфекций, а с другой
Проблема рациональной антибактериальной терапии инфекций дыхательных путей не теряет актуальности и в настоящее время. Наличие большого арсенала антибактериальных препаратов, с одной стороны, расширяет возможности лечения различных инфекций, а с другой — требует от врача-клинициста осведомленности о многочисленных антибиотиках и их свойствах (спектр действия, фармакокинетика, побочные эффекты и т. д.), умения ориентироваться в вопросах микробиологии, клинической фармакологии и других смежных дисциплинах.
Согласно И. В. Давыдовскому, «врачебные ошибки — род добросовестных заблуждений врача в его суждениях и действиях при исполнении им тех или иных специальных врачебных обязанностей». Ошибки в антибактериальной терапии инфекций дыхательных путей имеют наибольший удельный вес в структуре всех лечебно-тактических ошибок, совершаемых в пульмонологической практике, и оказывают существенное влияние на исход заболевания. Кроме того, неправильное назначение антибактериальной терапии может иметь не только медицинские, но и различные социальные, деонтологические, экономические и другие последствия.
При выборе способа антибактериальной терапии в амбулаторной практике необходимо учитывать и решать как тактические, так и стратегические задачи. К тактическим задачам антибиотикотерапии относится рациональный выбор антибактериального препарата, обладающего наибольшим терапевтическим и наименьшим токсическим воздействием.
Стратегическая задача антибиотикотерапии в амбулаторной практике может быть сформулирована как уменьшение селекции и распространения резистентных штаммов микроорганизмов в популяции.
В соответствии с этими положениями следует выделять тактические и стратегические ошибки при проведении антибактериальной терапии инфекций дыхательных путей в амбулаторной практике (см. таблицу 1).
Тактические ошибки антибактериальной терапии
I. Необоснованное назначение антибактериальных средств
Особую категорию ошибок представляет неоправданное применение антибактериальных препаратов (АП) в тех ситуациях, когда их назначение не показано.
Показанием для назначения антибактериального препарата является диагностированная или предполагаемая бактериальная инфекция.
Наиболее распространенная ошибка в амбулаторной практике — назначение антибактериальных препаратов при острых респираторных вирусных инфекциях (ОРВИ), имеющее место как в терапевтической, так и в педиатрической практике. При этом ошибки могут быть обусловлены как неправильной трактовкой симптоматики (врач принимает ОРВИ за бактериальную бронхолегочную инфекцию в виде пневмонии или бронхита), так и стремлением предотвратить бактериальные осложнения ОРВИ.
При всех трудностях принятия решения в подобных ситуациях необходимо отдавать себе отчет в том, что антибактериальные препараты не оказывают влияния на течение вирусной инфекции и, следовательно, их назначение при ОРВИ не оправдано (см. таблицу 2). В то же время предполагаемая возможность предотвращения бактериальных осложнений вирусных инфекций с помощью назначения антибактериальных препаратов не находит себе подтверждения в клинической практике. Кроме того, очевидно, что широкое неоправданное применение антибактериальных препаратов при ОРВИ чревато формированием лекарственной устойчивости и повышением риска возникновения нежелательных реакций у пациента.
Одной из распространенных ошибок при проведении антибактериальной терапии является назначение одновременно с антибиотиком противогрибковых средств с целью профилактики грибковых осложнений и дисбактериоза. Следует подчеркнуть, что при применении современных антибактериальных средств у иммунокомпетентных пациентов риск развития грибковой суперинфекции минимален, поэтому одновременное назначение антимикотиков в этом случае не оправдано. Комбинация антибиотика с противогрибковым средством целесообразна только у больных, получающих цитостатическую или противоопухолевую терапию или у ВИЧ-инфицированных пациентов. В этих случаях оправдано профилактическое назначение антимикотиков системного действия (кетоконазол, миконазол, флуконазол), но не нистатина. Последний практически не всасывается в желудочно-кишечном тракте и не способен предотвратить грибковую суперинфекцию иной локализации — полости рта, дыхательных или мочевыводящих путей, половых органов. Часто практикующееся назначение нистатина с целью профилактики дисбактериоза кишечника вообще не находит логического объяснения.
Часто врач назначает нистатин или другой антимикотик в случае обнаружения в полости рта или в моче грибов рода Сandida. При этом он ориентируется лишь на данные микробиологического исследования и не учитывает наличие или отсутствие симптомов кандидоза, а также факторов риска развития грибковой инфекции (тяжелый иммунодефицит и др.).
Выделение грибов рода Сandida из полости рта или мочевых путей пациентов в большинстве случаев служит свидетельством бессимптомной колонизации, не требующей коррегирующей противогрибковой терапии.
II. Ошибки в выборе антибактериального препарата
Пожалуй, наибольшее число ошибок, возникающих в амбулаторной практике, связано с выбором антибактериального средства. Выбор антибиотика должен производиться с учетом следующих основных критериев:
Определяющим фактором выбора препарата должен быть спектр природной активности антибиотика: необходимо, чтобы он охватывал основных возбудителей внебольничных инфекций дыхательных путей (см. таблицу 3).
Кроме того, при выборе препарата следует учитывать уровень приобретенной резистентности возбудителей в популяции. Основные тенденции, касающиеся резистентности возбудителей, отмеченной в последние годы, отражены в таблице 4. Наиболее значимые проблемы, связанные с применением основных антибактериальных средств при инфекциях дыхательных путей, могут быть сформулированы следующим образом.
С учетом вышесказанного, оптимальными средствами для лечения внебольничных инфекций дыхательных путей в настоящее время могут быть признаны β-лактамные антибиотики и новые фторхинолоны (см. таблицу 5). Использование макролидов должно быть ограничено — препараты можно назначать при нетяжелой пневмонии у детей или пациентов молодого возраста, особенно при наличии признаков атипичного течения (микоплазменная, хламидийная).
 |
| Таблица 5. Значение антибактериальных средств при инфекциях нижних дыхательных путей в амбулаторной практике. |
Следует подчеркнуть, что назначение некоторых антибактериальных препаратов, применяемое в амбулаторной практике при респираторных инфекциях, нельзя признать рациональным. К таким препаратам прежде всего относятся:
В таблице 6 приведены современные рекомендации по антибактериальной терапии внебольничных респираторных инфекций, с учетом всех требуемых критериев и доказанной эффективности в контролируемых клинических исследованиях.
Представленные рекомендации имеют наиболее общий характер. В то же время с практических позиций выбор оптимального антибактериального препарата также должен осуществляться с учетом особенностей пациента и заболевания. Так, например, у больных пневмонией молодого и среднего возраста без отягощающих факторов терапевтический эффект оказывают амоксициллин, макролиды, защищенные пенициллины и новые фторхинолоны. Однако у больных пожилого возраста в этиологии заболевания большее значение приобретают S. aureus и грамотрицательные бактерии, что объясняет снижение эффективности амоксициллина и макролидов у этой категории больных.
Также распространенной во врачебной практике ошибкой является отказ от назначения антибактериальной терапии при пневмонии беременным женщинам из-за опасения негативного влияния препаратов на плод. Следует отметить, что перечень антибактериальных препаратов, прием которых нежелателен во время беременности из-за риска эмбриотоксического действия, ограничен — тетрациклины, хлорамфеникол, сульфаниламиды, ко-тримоксазол, фторхинолоны, аминогликозиды. Другие антибиотики, в частности β-лактамы, макролиды, могут применяться у беременных женщин.
Другие возможные факторы, влияющие на выбор антибактериального препарата, представлены в таблице 7.
 |
| Таблица 7. Особые клинические ситуации при внебольничных инфекциях нижних дыхательных путей. |
Нередки ошибки при выборе антибактериального препарата в случае неэффективности первоначального. Здесь необходимо также остановиться на ошибках антибактериальной терапии, которые касаются несвоевременной оценки неэффективности первоначального антибиотика. Общепринятым критическим сроком оценки эффективности (или неэффективности) антибактериальной терапии считаются 48—72 ч с момента его назначения. К сожалению, приходится нередко сталкиваться с такими случаями, когда больной продолжает получать назначенный антибиотик в течение недели и более, несмотря на отсутствие очевидного клинического эффекта. Обычно критерием эффективности антибактериальной терапии является снижение или нормализация температуры тела больного, уменьшение признаков интоксикации. В тех случаях (не столь частых), когда лихорадка с самого начала заболевания отсутствует, приходится ориентироваться на другие признаки интоксикации (головная боль, анорексия, общемозговая симптоматика и т. д.), а также на отсутствие прогрессирования заболевания за период проводимого лечения.
Продолжение антибактериальной терапии, невзирая на ее неэффективность, имеет немало негативных последствий. При этом затягивается назначение другого, более адекватного антибиотика, что ведет к прогрессированию воспаления (особенно важно при тяжелых пневмониях, у больных с сопутствующей патологией) и развитию осложнений, а также удлиняет сроки лечения. Кроме того, повышается риск возникновения побочных (токсических) эффектов препаратов, а также развития и усиления антибиотикорезистентности. Продолжение лечения, несмотря на неэффективность проводимой терапии, подрывает доверие больного и его родственников к лечащему врачу. Очевидна и неэкономичность такой ошибочной тактики антибактериальной терапии (напрасный расход неэффективного АП, дополнительные затраты на лечение токсических эффектов и др.).
Кроме того, ошибки встречаются при замене неэффективного антибиотика на другой, т. е. при смене препарата. При этом врач забывает, что принцип выбора антибактериального препарата остается прежним, т. е. ориентироваться следует на клиническую ситуацию с учетом, однако, неэффективности первоначального препарата и ряда других дополнительных признаков. Отсутствие эффекта от первоначально назначенного антибиотика в известной степени должно служить дополнительным ориентиром, позволяющим обосновать выбор второго препарата. Так, например, отсутствие эффекта от применения β-лактамных антибиотиков (пенициллины, цефалоспорины) у больного с внебольничной пневмонией позволяет предполагать атипичную этиологию пневмонии (микоплазменной, хламидийной или легионеллезной) с учетом, разумеется, других клинических признаков.
Клинические признаки атипичной пневмонии, вызванной Mycoplasma pneumoniae или Chlamydia pneumoniae:
Наличие клинических признаков атипичной пневмонии делает обоснованным назначение антибактериальных препаратов из группы макролидов, доксициклина или фторхинолонов (левофлоксацин, моксифлоксацин, офлоксацин).
III. Ошибки в выборе режима дозирования антибактериального препарата
Ошибки в выборе оптимальной дозы антибактериального средства могут заключаться в назначении как недостаточной, так и избыточной дозы препарата. И те и другие ошибки чреваты негативными последствиями.
Если доза антибиотика недостаточна и не создает в крови и тканях дыхательных путей концентрацию, превышающую минимальную дозу для подавления основных возбудителей инфекции, что является условием эрадикации соответствующего возбудителя, то это не только может служить одной из причин неэффективности терапии, но и создает реальные предпосылки для формирования резистентности микроорганизмов. Ошибки в выборе оптимальной дозы могут быть связаны как с назначением недостаточной разовой дозы, так и с неправильным режимом дозирования (недостаточная кратность введения).
В качестве примера неадекватного режима дозирования антибиотиков при внебольничной пневмонии можно привести амоксициллин, который ранее рекомендовался в суточной дозе до 1 г. Однако современные рекомендации предполагают назначение амоксициллина в суточной дозе 1,5 и даже 3 г для преодоления возможной резистентности S. pneumoniae. Примеры неадекватных режимов дозирования антибиотиков в амбулаторной практике при респираторных инфекциях приводятся в таблице 8.
 |
| Таблица 8. Неадекватные режимы дозирования пероральных антибактериальных препаратов в амбулаторной практике при респираторных инфекциях у взрослых. |
Неправильный выбор интервалов между введениями антибактериальных препаратов обычно обусловлен не столько сложностями парентерального введения препаратов в амбулаторных условиях или негативным настроем больных, сколько неосведомленностью практикующих врачей о некоторых фармакодинамических и фармакокинетических особенностях препаратов, которые должны определять режим их дозирования. Типичной ошибкой является назначение в амбулаторной педиатрической практике при пневмонии бензилпенициллина с кратностью введения два раза в сутки, так как более частое его введение неудобно для пациента. Следует отметить, что при нетяжелом течении пневмонии вряд ли оправдано стремление некоторых врачей к обязательному назначению парентеральных антибиотиков. Современные антибактериальные препараты характеризуются хорошей биодоступностью при приеме внутрь, а также одинаковой клинической эффективностью с парентеральными препаратами, поэтому в подавляющем большинстве случаев оправдано лечение пероральными препаратами. Если назначение парентеральных антибиотиков действительно необходимо, следует выбрать препарат с длительным периодом полувыведения (например, цефтриаксон), что позволяет назначать его один раз в сутки.
IV. Ошибки при комбинированном назначении антибиотиков
Одной из ошибок антибактериальной терапии внебольничных респираторных инфекций является необоснованное назначение комбинации антибиотиков. Врачи старших поколений помнят то время (50—70-е гг. прошлого столетия), когда при лечении пневмонии обязательным считалось назначение пенициллина и стрептомицина, о чем свидетельствовали многие учебные пособия и руководства. Это был своеобразный стандарт лечения пневмоний для того времени. Несколько позднее одновременно с антибиотиками рекомендовалось назначение сульфаниламидов, с учетом полученных в свое время З. В. Ермольевой данных о химиотерапевтическом синергизме сульфаниламидов и пенициллина.
В современной ситуации, при наличии большого арсенала высокоэффективных антибактериальных препаратов широкого спектра, показания к комбинированной антибактериальной терапии значительно сужены, и приоритет в лечении респираторных инфекций остается за монотерапией. В многочисленных контролируемых исследованиях показана высокая клиническая и бактериологическая эффективность адекватных антибактериальных средств при лечении респираторных инфекций в режиме монотерапии (амоксициллин, амоксициллин/клавуланат, цефалоспорины II-III поколений, новые фторхинолоны). Комбинированная антибактериальная терапия не имеет реальных преимуществ ни в выраженности эффекта, ни в предотвращении развития резистентных штаммов.
Основными показаниями к комбинированной антибактериальной терапии являются тяжелое течение пневмонии — в этом случае общепринятым стандартом лечения становится комбинированное назначение парентерального цефалоспорина III поколения (цефотаксим или цефтриаксон) и парентерального макролидного антибиотика (эритромицин, или кларитромицин, или спирамицин); последние включаются в комбинацию для воздействия на вероятных атипичных микроорганизмов (легионелла или микоплазма). Следует отметить, что в настоящее время в клинической практике появились новые антибактериальные препараты (левофлоксацин, моксифлоксацин) с высокой активностью в отношении как типичных, так и атипичных возбудителей, что позволяет назначать их в режиме монотерапии даже при тяжелой пневмонии.
Другой клинической ситуацией, оправдывающей комбинированное назначение антибиотиков, является пневмония у иммунокомпрометированных пациентов (лечение цитостатиками, СПИД), при которой имеется высокая вероятность ассоциации возбудителей (см. таблицу 7).
К сожалению, часто в амбулаторной практике приходится сталкиваться с ситуациями, при которых больным с нетяжелым течением пневмонии, при отсутствии осложнений, тяжелой фоновой патологии назначается два антибиотика. Логичного обоснования этой тактики лечения нет, при этом следует учитывать возможный антагонизм препаратов, более высокий риск нежелательных реакций и увеличение стоимости лечения.
Следует отметить, что нерациональные комбинации антибактериальных препаратов имеют и официальные лекарственные формы, которые выпускаются отечественной фармацевтической промышленностью, например ампиокс, олететрин. Разумеется, применение таких препаратов недопустимо.
V. Ошибки, связанные с длительностью антибактериальной терапии и критериями клинической эффективности
В некоторых случаях проводится необоснованно длительная антибактериальная терапия. Такая ошибочная тактика обусловлена, прежде всего, недостаточным пониманием цели самой антибактериальной терапии, которая сводится прежде всего к эрадикации возбудителя или подавлению его дальнейшего роста, т. е. направлена на подавление микробной агрессии.
Собственно воспалительная реакция легочной ткани, которая проявляется различными клинико-рентгенологическими признаками (аускультативная картина, сохраняющаяся рентгенологическая инфильтрация, ускорение СОЭ) регрессирует медленнее и не требует продолжения антибактериальной терапии (см. таблицу 9). В связи с этим следует считать ошибочной тактику, согласно которой у больногос сохраняющимися рентгенологическими признаками легочной инфильтрации, крепитирующими хрипами (crepitacio redux), увеличением СОЭ при нормализации температуры тела и исчезновении (или уменьшении) признаков интоксикации продолжают проводить антибактериальную терапию.
 |
| Таблица 9. Сроки исчезновения симптомов при эффективной антибактериальной терапии внебольничной пневмонии. |
Еще более ошибочна тактика замены одного антибиотика на другой в подобных ситуациях, расцениваемых врачом как неэффективность назначенной антибактериальной терапии. У некоторых больных после исчезновения признаков интоксикации и даже регрессии воспалительных изменений в легких в течение длительного времени может сохраняться слабость, потливость, субфебрильная температура. Последняя расценивается врачом как проявление не полностью купированной бронхолегочной инфекции, что «подтверждается» рентгенологическими данными в виде изменения легочного рисунка или «остаточными явлениями пневмонии» и обычно влечет за собой назначение антибактериального препарата, несмотря на отсутствие изменений со стороны крови. Между тем подобная клиническая ситуация часто обусловлена вегетативной дисфункцией после легочной инфекции (постинфекционная астения) и не требует антибактериальной терапии, хотя, разумеется, в каждом конкретном случае необходимы тщательное обследование больного и расшифровка всей имеющейся симптоматики.
Рекомендованная длительность применения антибактериальных препаратов при бронхолегочных инфекциях приведена в таблице 10.
 |
| Таблица 10. Длительность антибактериальной терапии бактериальных респираторных инфекций в амбулаторной практике. |
Л. И. Дворецкий, доктор медицинских наук, профессор
С. В. Яковлев, доктор медицинских наук, профессор
ММА им. И. М. Сеченова, Москва