залаин или тербинафин что лучше при лишае
Стригущий лишай
Девочка 1,5 года, подхватили на даче лишай,на коже пятнышки маленькие быстро вылечили клотримазолом, на головке никак не вылечимся. Диагноз точный,светили лампой Вуда-яркое зеленое свечение. Нам прописали гризеофульвин и мазь залаин. На мой вопрос о побочных эффектах таблеток доктор ответила,что все хорошо,ничего нет!! Придя домой и прочитав инструкцию к препарату ужаснулась и испугалась. большая нагрузка на печень,аллергические реакции,расстройство жкт,головные боли. и в противопоказаниях детский возраст. Ребенок склонен к аллергии..
Вычитала что есть более щадящие препараты на тербинафине. почему не прописывают их? У нас небольшие очаги в 1см на затылке 3шт.,не ползут,новых нет, кожа в очагах чистая, появляются здоровые волосики, один очаг начал зарастать, но динамика катастрофически мала..болеем уже 1,5 месяца, Обрабатываю йодом,марганцовкой,контролирую уф лампой дома. Чем лечат таких малышей. Неужели только травить гризеофульвином. Также перепробовали ям, лук компрессы (всё образует корочки,под которыми остаетс свече6ие луковиц).
Как насчет ламизила,тербинафина, чем отличаются разные синтетические производные имидазола??что эффективнее? может есть эффективный крем,который может помочь?или только таблетки,какие?
Если таблетки, нужно контролировать анализ крови (если да, то что и когда сдавать)? Может нужна поддерживающая терапия печени,жкт?
Уважаемые посетители сайта СпросиВрача! Вы можете задать свой вопрос и получить 03 онлайн консультацию врача быстро, просто и без регистрации. Мгновенный ответ в режиме онлайн!
Что лучше: Залаин или Тербинафин
Залаин
Тербинафин
Исходя из данных исследований, Тербинафин лучше, чем Залаин. Поэтому мы советуем выбрать его.
Но не забывайте, что у данных препаратов в составе разные активные вещества. Поэтому обязательно проконсультируйтесь с врачом. Возможно, какой-то из них может не подойти для вашей терапии.
Сравнение эффективности Залаина и Тербинафина
У Залаина эффективность больше Тербинафина – это означает, что способность лекарственного вещества оказывать максимально возможное действие разное.
Например, если терапевтический эффект у Залаина более выраженный, то у Тербинафина даже в больших дозах добиться данного эффекта невозможно.
Также скорость терапии – показатель быстроты терапевтического действия у Залаина и Тербинафина тоже разное, как и биодоступность – количество лекарственного вещества, доходящее до места его действия в организме. Чем выше биодоступность, тем меньше его потерь будет при усвоении и использовании организмом.
Сравнение безопасности Залаина и Тербинафина
Безопасность препарата включает множество факторов.
При этом у Залаина она выше, чем у Тербинафина. Важно, где метаболизируется препарат: лекарственные вещества выделяются из организма либо в неизмененном виде, либо в виде продуктов их биохимических превращений. Метаболизм протекает спонтанно, но чаще всего задействует основные органы, такие как печень, почки, лёгкие, кожу, мозг и другие. При оценивании метаболизма у Залаина, также как и у Тербинафина мы смотрим, какой орган является метаболизирующим и наколько критично действие на него.
Соотношение риска к пользе – это когда назначение лекарственного препарата нежелательно, но оправдано при определенных условиях и обстоятельствах, с обязательным соблюдением осторожности применения. При этом у Залаина рисков при применении меньше, чем у Тербинафина.
Также при рассчете безопасности учитывается проявляются ли только аллергические реакции или же возможная дисфункция основных органов. В прочем как и обратимость последствий от использования Залаина и Тербинафина.
Сравнение противопоказаний Залаина и Тербинафина
Исходя из инструкции. Количество противопоказаний у Залаина достаточно схоже с Тербинафином и составляет малое количество. Это и перечень симптомов с синдромами, и заболевания, различные внешних и внутренние условия, при которых применение Залаина и Тербинафина может быть нежелательным или недопустимым.
Сравнение привыкания у Залаина и Тербинафина
Как и безопасность, привыкание тоже включает множество факторов, которые необходимо учитывать при оценивании препарат.
Так совокупность значения таких параметров, как «cиндром отмены» и «развитие резистентности», у Залаина достаточно схоже со аналогичными значения у Тербинафина. Синдром отмены – это патологическое состояние, возникающее после прекращения поступления в организм веществ, вызывающих привыкание или зависимость. А под резистентностью понимают изначальную невосприимчивость к препарату, этим она отличается от привыкания, когда невосприимчивость к препарату развивается в течение определенного периода времени. Наличие резистентности можно констатировать лишь в том случае, если была сделана попытка увеличить дозу препарата до максимально возможной. При этом у Залаина значения «синдрома отмены» и «резистентности» достотачно малое, впрочем также как и у Тербинафина.
Сравнение побочек Залаина и Тербинафина
Побочки или нежелательные явления – это любое неблагоприятное с медицинской точки зрения событие, возникшее у субъекта, после введения препарата.
У Залаина состояния нежелательных явлений почти такое же, как и у Тербинафина. У них у обоих количество побочных эффектов малое. Это подразумевает, что частота их проявления низкая, то есть показатель сколько случаев проявления нежелательного эффекта от лечения возможно и зарегистрировано – низкий. Нежелательное влияние на организм, сила влияния и токсическое действие у Залаина схоже с Тербинафином: как быстро организм восстановиться после приема и восстановиться ли вообще.
Сравнение удобства применения Залаина и Тербинафина
Это и подбор дозы с учетом различных условий, и кратность приемов. При этом важно не забывать и про форму выпуска препарата, ее тоже важно учитывать при составлении оценки.
Удобство применения у Залаина лучше, чем у Тербинафина.
Рейтинг препаратов составлен опытными фармацевтами, изучающий международные исследования. Отчет сгенерирован автоматически.
Дата последнего обновления: 2021-01-27 08:00:39
Отрубевидный лишай
Отрубевидный лишай (син.: разноцветный лишай, pityriasis versicolor, pityriasis furfuracea) — грибковое заболевание кожи, характеризующееся поражением рогового слоя эпидермиса. Возбудителем данного заболевания является гриб Pityrosporum orbiculare или P.
Отрубевидный лишай (син.: разноцветный лишай, pityriasis versicolor, pityriasis furfuracea) — грибковое заболевание кожи, характеризующееся поражением рогового слоя эпидермиса. Возбудителем данного заболевания является гриб Pityrosporum orbiculare или P. ovale. Однако вопрос о том, представляют ли обе эти формы один организм на разных этапах его развития или являются обособленными видами, до конца не решен. В настоящее время принято считать, что обе микроморфологические разновидности P. оrbiculare и P. ovale представляют различные стадии в жизненном цикле гриба. При этом его овальная форма — P. ovale чаще встречается на коже волосистой части головы, а круглая — P. orbiculare — на коже туловища [25]. Правильная таксономическая идентификация липофильных дрожжей, вызывающих данное заболевание, до сих пор является предметом дискуссий. Некоторые ученые предпочитают название Pityrosporum orbiculare, другие же — Malassezia furfur. Благодаря молекулярным технологиям в настоящее время установлено 10 видов рода Malassezia. Ogunbiyi A. O. и George A. O. (2005) выделили наиболее часто встречаемые виды Malassezia: М. furfur, M. symboidalis, M. obtusa, M. globosa, M. restricta, M. slooffiae и M. pachydermatis [12, 15, 17].
В результате проведенного ими анализа установлено, что причиной развития отрубевидного лишая у людей чаще всего является M. globosa. Hort W. и соавт. (2006), обследовав 112 пациентов с диагнозами себорейный дерматит, атопический дерматит, разноцветный лишай и СПИД, установили, что у данных больных присутствовали различные виды грибов Malassezia. По данным авторов, M. globosa являлась наиболее патогенной разновидностью и чаще регистрировалась у ВИЧ-положительных пациентов и больных разноцветным лишаем. В группе больных себорейным дерматитом наряду с M. globosa выделялась M. sympodialis.
Довольно длительно в научной литературе обсуждался вопрос о контагиозности гриба. Раньше считалось, что передача инфекции происходит либо при непосредственном контакте с больным, либо через зараженное белье. Данное наблюдение было основано на высокой распространенности этого заболевания среди лиц одной семьи. Однако в настоящее время доказано, что разноцветный лишай не обладает контагиозностью, и установлена генетическая предрасположенность к развитию кератомикоза: известные случаи семейного заболевания объясняются сходным типом кожи у членов семьи, находящихся в кровном родстве [6, 25, 28].
Являясь дрожжеподобным грибом, Р. orbiculare обладает многими качествами, присущими данной группе грибов. В частности, заболевание развивается при трансформации сапрофитной формы в патогенную при особых, благоприятных обстоятельствах. Развитию заболевания способствуют: повышенная потливость, себорея, уменьшение физиологического шелушения кожи, пониженное питание, патология внутренних органов. Разноцветный лишай — своеобразный маркер сахарного диабета, туберкулеза, ревматизма, СПИДа. При этих заболеваниях его обнаруживают у 52–63% больных. Если отрубевидный лишай развивается на фоне туберкулеза, лимфогрануломатоза и других заболеваний, сопровождающихся потливостью, возрастных ограничений не существует и клинические признаки данного дерматоза могут наблюдаться в любом возрасте [6]. В литературе описывался случай разноцветного лишая, диагностированного у трехмесячного ребенка, больного лейкемией [23].
В последние десятилетия отмечаются гематогенные инфекции, обусловленные M. furfur, они описаны у ослабленных и иммуносупрессированных больных, особенно после трансплантации органов, а также у детей неонатального возраста, получавших липиды через центральный венозный катетер [1, 11, 13, 24].
Наличие у P. orbiculare перекрестно реагирующих антигенов с грибами рода Candida провоцирует развитие аллергических реакций немедленного, иммунокомплексного и замедленного типов. Исследованиями, проведенными различными авторами, доказано, что одним из основных факторов риска формирования осложненных форм атопического дерматита в раннем возрасте у детей является преобладание грибов рода Мalassezia. Присоединение ассоциированной грибковой инфекции изменяет клиническую картину атопического дерматита, которая характеризуется более тяжелым течением, распространенным процессом и резистентностью к традиционной терапии [10, 16, 27]. Согласно наблюдениям Mayser P. и соавт. (2000) у пациентов с колонизацией P. orbiculare на волосистой части головы и на шее чаще регистрировались специфические антитела IgE, чем у пациентов с локализацией на коже туловища. Кроме того, автор установил, что пациенты с Malassezia чаще жаловались на диффузное поредение волос.
Необходимо помнить, что себорейный дерматит, ассоциированный P. orbiculare (ovale), может быть единственным самым ранним проявлением СПИДа. По данным зарубежных авторов, от 30% до 80% пациентов с ВИЧ-инфекцией имеют себорейный дерматит, по сравнению со здоровыми молодыми людьми, у которых данный дерматоз диагностировался лишь в 3–5% случаев. Для СПИД-ассоциированного себорейного дерматита характерны стойкость к проводимой терапии и папулезные высыпания, напоминающие псориаз [1, 8, 9, 13].
Клиническая картина заболевания. Дебют заболевания характеризуется появлением желтоватых точек, приуроченных к устью волосяных фолликул. Первичным морфологическим элементом является пятно розово-желтого цвета, изменяющееся постепенно до коричнево-желтого, на поверхности которого находятся отрубевидные чешуйки. Для элементов характерен периферический рост и, впоследствии, слияние в более крупные очаги с фестончатыми краями. При длительном течении микоза очаги поражения могут занимать обширные участки кожного покрова. Со временем окраска очагов может варьировать от белого цвета до темно-бурого, это послужило основанием для второго названия лишая — разноцветный. Поверхность высыпаний покрыта отрубевидными чешуйками, которые при поверхностном осмотре малозаметны, однако при поскабливании легко возникает шелушение (симптом Бенье). Поскольку излюбленная локализация приурочена к «себорейным зонам», поражаются верхняя половина туловища и волосистая часть головы. Дополнительными критериями диагностики служат, хорошо известные врачам, йодная проба Бальцера и золотисто-желтое или буроватое свечение под лампой Вуда, а также обнаружение возбудителя при микроскопическом и культуральном исследованиях [1, 2, 5, 6, 9].
Особенностью клинической картины отрубевидного лишая является наличие псевдолейкодермы. Мнение ученых о причинах возникновения неравномерной окраски кожи при данном дерматозе разделилось. Некоторые исследователи считают, что P. orbiculare (ovale) в процессе окисления ингибирует активность тирозиназы, что приводит к уменьшению синтеза меланина и клинически проявляется возникновением истинной лейкодермы [6]. По мнению других авторов, разрыхленный роговой слой на очагах поражения препятствует проникновению ультрафиолетовых лучей в глубину эпидермиса. Поэтому пораженные очаги после удаления чешуек во время водных процедур становятся более светлыми, чем окружающая здоровая кожа [2, 9].
Как правило, диагностика не представляет затруднений, однако имеется несколько моментов, на которые необходимо обратить внимание практикующему врачу. Во-первых, у лиц, получавших лечение и прошедших облучение ультрафиолетовыми лучами, проба Бальцера будет отрицательной. Во-вторых, выявление участков поражения на волосистой части головы имеет практическое значение: если врач не обратит внимания на данную локализацию кератомикоза, то возможна большая вероятность рецидива. Для диагностики очагов поражения на волосистой части головы используют лампу Вуда (очаги имеют зеленовато-желтое, желтовато-коричневое или буроватое свечение). В-третьих, розовато-коричневые пятна едва заметны на белой коже, поэтому при осмотре на них часто не обращают внимания, но летом при наличии загара они становятся более заметными. И последний нюанс: у лиц без иммунного дефицита изолированные пятна не превышают, как известно, размеров 1–1,5 см в диаметре, но при выраженном иммунодефиците они могут достигать величины 5 см в диаметре. При этом отмечаются не только диссеминированный характер, но и насыщенная пигментация и инфильтрация элементов разноцветного лишая. У больных СПИДом разноцветный лишай чаще проявляется как себорейный дерматит, реже как атопический дерматит и множественные фолликулиты на участках кожи с явлениями васкулита и некротического компонента.
Атипичное течение разноцветного лишая описывали различные авторы [11, 14]. К редчайшим проявлениям разноцветного лишая относится поражение кожи подошв. В отечественной литературе о такой локализации сообщает Руковишникова В. М. (1999), которая в своей монографии ссылается на наблюдения В. П. Жирковой (1977) 16-летнего мальчика с гипергидрозом, у которого наряду с высыпаниями разноцветного лишая в типичных местах (грудь, спина, шея, лицо) имелись очаги микоза на подошвах. Отмечена выраженная торпидность очагов поражения этой необычной локализации. Даже при прошествии четырех месяцев лечения сохранялись невоспалительные буроватые пятна неправильной формы и очертаний на пятках и в переходной складке от пальцев к подошве.
Дифференциальную диагностику отрубевидного лишая проводят с сифилисом (с сифилитической розеолой и лейкодермой). Диагноз сифилиса подтверждают положительными результатами классических серологических реакций (КСР), реакцией иммобилизации бледных трепонем (РИБТ), реакцией иммунофлюоресценции (РИФ). Кроме того, розеола при вторичном сифилисе имеет розовато-ливидный оттенок, исчезает при диаскопии, не шелушится, не флюоресцирует в свете люминесцентной лампы, проба Бальцера отрицательная.
При сифилитической лейкодерме не бывает сливных гиперпигментированных пятен и микрополициклических краев. Для сифилитической розеолы характерна преимущественная локализация на туловище и верхних конечностях, что определяет некоторую сходность клинической картины, однако при сифилитическом поражении нет склонности к росту и слиянию элементов. Пятно при розеоле имеют сосудистое происхождение, отсутствует шелушение, не сопровождается субъективными ощущениями, проба Бальцера отрицательная.
Разноцветный лишай следует отличать от розового лишая Жибера, при котором эритематозные пятна островоспалительные, округлых или овальных очертаний, со своеобразным шелушением в центре по типу «медальонов», имеется «материнская» бляшка. Высыпания располагаются симметрично по линиям Лангера. Края центральной, шелушащейся, части бляшки окружены воротничком из чешуек. Вокруг материнской бляшки видны многочисленные вторичные высыпания.
Pityrosporum-фолликулит (Мalassezia-фолликулит) — инфекция волосяного фолликула, вызванная дрожжевыми грибами, теми же, что вызывают отрубевидный лишай. Данное заболевание представляет собой отдельно расположенные, иногда зудящие папулосквамозные высыпания, локализующиеся главным образом на верхней половине туловища и плечах. Pityrosporum-фолликулитом болеют чаще лица молодого и среднего возраста и женщины. Первично появляется фолликулярная окклюзия, которая вторично сопровождается усилением роста гриба. Предрасполагающими факторами являются сахарный диабет, а также прием антибиотиков широкого спектра действия или кортикостероидов. Заболевание может проявляться на лбу и имитировать стойкое акне. Клиническая картина представлена бессимптомными или слегка зудящими куполообразными фолликулярными папулами и пустулами диаметром 2–4 мм. Данный дерматоз больше распространен в тропиках, где проявляется фолликулярными папулами, пустулами, узлами и кистами. Отличительной особенностью Pityrosporum-фолликулита является отсутствие комедонов, торпидность к терапии и локализация в области лба. По данным Томас П. Хэбиф (2006) очень часто больных с Pityrosporum-фолликулитом принимают за больных акне. По мнению автора, данное заболевание следует подозревать у пациентов молодого и среднего возраста с фолликулярными очагами, расположенными на туловище, и с жалобами на зуд.
Лечение. Поскольку данное заболевание развивается при трансформации сапрофитной формы гриба в патогенную при особых, благоприятных обстоятельствах, необходимо, в первую очередь, выявить провоцирующие факторы. Разноцветный лишай является маркером сахарного диабета, туберкулеза, ревматизма, СПИДа. Поэтому при обследовании больного нужно провести соответствующие исследования. Особое внимание следует уделять лицам, не попадающим в возрастную категорию от 15 до 45 лет. Часто развитие стойкой клинической картины отрубевидного лишая вызвано химиотерапией у онкологических больных. Как правило, после окончания курса интенсивного лечения у таких пациентов происходит спонтанное самоизлечение.
Как уже упоминалось выше, отрубевидный лишай характеризуется поражением поверхностного слоя эпидермиса — рогового. Следовательно, начинать лечение кератомикоза нужно с наружных средств. Лекарственные препараты для лечения отрубевидного лишая можно разделить на несколько групп:
Терапия разноцветного лишая зависит от распространенности и локализации очагов поражения. Раньше в лечении данного микоза использовались кератолитические средства: 2–5% салициловый спирт или спиртовой раствор резорцина 2 раза в день. Современные методы терапии включают фунгицидные препараты из группы азолов. Установлено, что под воздействием антимикотических лекарств через 24 часа происходит дегидратация и вакуолизация цитоплазмы в клетке гриба, просветление клеточной стенки, от которой через 48 часов остается только тень. Поэтому именно специфическому противогрибковому лечению чаще отдается предпочтение, чем кератолитическим препаратам.
Учитывая поверхностность поражения кожи кератомикозом, предпочтительнее использовать фунгицидные средства в виде растворов (клотримазол, бифоназол, циклопирокс, нафтифин (Экзодерил), тербинафин (Ламизил)) или эконазол в виде порошка, выпускаемого под торговым названием «Ифенек», который наносят на пораженные участки кожи и слегка втирают. Более удобной формой применения лекарственного вещества является спрей (Ламизил, Термикон). Все антимикотические растворы при лечении отрубевидного лишая назначаются 2 раза в сутки в течение 1 недели. Кетоконазол обладает более высокой активностью в отношении P. ovale, подавляя его рост в концентрациях, в 25–30 раз меньших, чем остальные противогрибковые препараты, и в несколько раз меньших, чем любые системные антимикотики. При нанесении местных форм кетоконазола на кожу эффективные концентрации сохраняются внутри и на поверхности эпидермиса в течение 72 часов после отмены препарата, что объясняется сродством препарата к кератинизированным тканям.
Пиритион цинка также оказывает прямое противогрибковое действие. На сегодняшний день механизм терапевтического воздействия пиритиона цинка связывают не только с цитостатическим, но и с противогрибковым, антимикробным действием. Эффективность препаратов, содержащих пиритион цинка, к дрожжеподобным грибам изучена многими авторами [1, 3, 4]. К таким препаратам относятся Псорилом и Скин-кап, выпускаемые в двух формах: спрей и крем. В дальнейшем эти средства могут быть использованы больными в качестве профилактических средств не реже 1 раза в 2 недели. Уступая кетоконазолу, пиритион цинка превосходит по противогрибковой активности другие препараты, в том числе сульфид селена и некоторые имидазолы. В последнее десятилетие шампуни на основе цинка (Head and shoulders, Фридерм цинк) являются широко используемыми препаратами для лечения перхоти. Таким образом, наиболее эффективными лекарственными средствами при лечении отрубевидного лишая являются антимикотические средства и пиритион цинка.
При поражении грибком волосистой части головы применяются лечебные шампуни, содержащие фунгицидные средства (Низорал, Себазол, Дюкре Келюаль DS, Кетоконазол), которые назначаются ежедневно с экспозицией на 2–5 минут в течение 7–10 дней. Лечение шампунями, содержащими деготь (Псорилом), эффективно при наличии себорейного дерматита, для устранения таких проявлений, как инфильтрация, отек, шелушение, эритема.
К комбинированным препаратам можно отнести шампуни: Нодэ DS плюс, который содержит салициловую кислоту, климбазол, пиритион цинка, и Кето плюс на основе кетоконазола и пиритиона цинка.
Системное лечение показано пациентам с распространенной формой заболевания, которые не реагируют на местную терапию или у которых часто наблюдаются рецидивы. Интраконазол назначают в дозе 200 мг 2 раза в день на один день или по 200 мг каждый день в течение 5 дней. Препарат принимают с пищей для улучшения адсорбции. Кетоконазол принимают в дозе 400 мг однократно или по 200 мг ежедневно в течение 5 дней за завтраком, запивая фруктовым соком. Флуконазол назначают в дозе 150 мг (2 капсулы в неделю в течение 4 недель или 2 капсулы в качестве начальной дозы, что повторяют через 2 недели). При медленном разрешении процесса курс системных антимикотиков можно повторить через 2 недели. Пациенту не рекомендуется принимать ванну в течение 12 часов после лечения, т. к. воздержание от водных процедур позволяет лекарству накопиться в коже. Некоторые авторы рекомендуют для предотвращения рецидивов ежедневную смену одежды в течение одного месяца. Больные должны смириться, что остаточная гипопигментация, как следствие псевдолейкодермы, держится довольно длительное время.
В лечении Pityrosporum-фолликулита следует придерживаться тех же принципов, что и в терапии отрубевидного лишая, но предпочтительнее сочетать системный кетоконазол (по 200 мг ежедневно в течение 4 недель) с наружными противогрибковыми средствами.
Современные методы лечения онихомикоза
Онихомикоз является наиболее распространенным заболеванием ногтей. Установлено, что 50 % случаев изменений ногтевых пластинок связано с микотической инфекцией. Эпидемиологические исследования, проведенные в России и зарубежных странах, выявили высокую з
Онихомикоз является наиболее распространенным заболеванием ногтей. Установлено, что 50 % случаев изменений ногтевых пластинок связано с микотической инфекцией. Эпидемиологические исследования, проведенные в России и зарубежных странах, выявили высокую заболеваемость онихомикозом, которая составила в общей популяции населения от 2 до 13 % [1, 2, 3]. Риск развития онихомикоза наиболее высок у больных старшего возраста. Например, у людей старше 70 лет распространенность онихомикоза стоп может составлять 50 % и выше [2, 4, 5]. Считается, что этому способствуют медленный рост ногтевых пластинок, нарушения периферического и магистрального кровообращения у лиц пожилого возраста [6]. Высокую частоту онихомикоза выявляют также у больных с иммунодефицитными состояниями (в том числе у больных СПИДом) и у больных сахарным диабетом [6, 7, 8].
Часто больные и некоторые врачи воспринимают онихомикоз как исключительно эстетическую проблему. Однако это серьезное заболевание, которое протекает хронически и в случаях возникновения иммунодефицитного состояния, декомпенсации эндокринных заболеваний может стать причиной развития распространенного микоза кожи и ее придатков. Нередко онихомикоз сопровождается развитием тяжелых осложнений, например диабетической стопы, хронического рожистого воспаления конечностей, лимфостаза, элефантиаза [9, 10]. У больных, получающих цитостатическую или иммуносупрессивную терапию, болезнь может стать причиной развития инвазивных микозов. Вот почему лечение онихомикоза является необходимым и должно проводиться своевременно [11].
Всего несколько десятилетий назад лечение онихомикоза было трудоемким, длительным и малоперспективным. Лекарственные препараты, применявшиеся для лечения грибковых заболеваний кожи и ее придатков, отличались низкой эффективностью и высокой токсичностью. Для достижения положительного результата требовалось длительное лечение или увеличение дозы препаратов, что нередко сопровождалось тяжелыми осложнениями. Некоторые методы лечения были потенциально опасны для жизни пациентов. Например, рентгенотерапия, применение таллия и ртути приводили к развитию у пациентов онкологических заболеваний кожи, заболеваниям головного мозга и внутренних органов.
Появление высокоэффективных и малотоксичных антимикотических препаратов значительно облегчило лечение грибковых заболеваний кожи и ее придатков. Однако результаты применения новых антимикотиков оказались недостаточно удовлетворительными. Контролируемые клинические испытания показали, что эффективность применения системных антимикотиков после окончания лечения составляет от 40 до 80 %, а через 5 лет — от 14 до 50 % [12]. В то же время эффективность терапии онихомикоза повышается при применении комплексных методов лечения, которые предусматривают использование этиотропных препаратов и средств, влияющих на звенья патогенеза [13]. Также в результате клинических испытаний, проведенных в странах Европы, было установлено, что эффективность лечения онихомикоза можно повысить в среднем на 15 % при сочетанном применении антимикотиков системного действия и антифунгального лака, содержащего аморолфин [14].
Лечение
Аллиламины являются синтетическими антимикотиками. Аллиламины преимущественно действуют на дерматомицеты, при этом они оказывают фунгицидное действие. Механизм их действия заключается в ингибировании фермента скваленэпоксидазы, которая принимает участие в синтезе эргостерола — основного структурного компонента клеточной мембраны дерматомицетов. К аллиламинам относятся тербинафин и нафтифин.
Аллиламины активны в отношении большинства дерматомицетов (Epidermophyton spp., Trichophyton spp., Microsporum spp., Malassezia spp.), возбудителя хромомикоза и некоторых других грибов.
Показаниями для назначения тербинафина внутрь являются онихомикоз, распространенные формы дерматомикозов кожи, микоз волосистой части головы, хромомикоз. Показаниями для наружного применения тербинафина и нафтифина служат ограниченное поражение кожи при микозах, отрубевидный лишай, кандидоз кожи. Тербинафин обладает высокой биодоступностью, хорошо всасывается в ЖКТ независимо от приема пищи. В высоких концентрациях препарат накапливается в роговом слое кожи, ногтевых пластинках, волосах, выделяется с секретами потовых и сальных желез. Абсорбция тербинафина при местном применении составляет менее 5 %, нафтифина — 4–6 %. Концентрация тербинафина и нафтифина в коже и ее придатках значительно превышает МПК для основных возбудителей дерматомикозов. Коррекция режима дозирования тербинафина может потребоваться при сочетанном назначении его с индукторами (рифампицин) или ингибиторами микросомальных ферментов печени (циметидин), так как первые повышают его клиренс, а вторые его понижают.
В результате многочисленных контролируемых многоцентровых сравнительных клинических испытаний было установлено, что тербинафин является наиболее эффективным антимикотиком в терапии онихомикоза [12] (табл. 1).
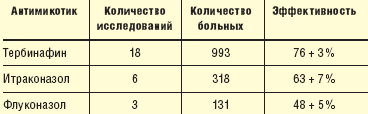 |
| Таблица 1. Сравнительная эффективность антимикотиков в терапии онихомикоза (по результатам метаанализа 27 рандомизированных исследований) |
Тербинафин применяют при распространенном поражении кожи, онихомикозе, хромомикозе, в таких случаях тербинафин назначают перорально. Тербинафин является препаратом выбора в терапии онихомикоза, так как наиболее эффективен по отношению к основных возбудителям онихомикоза — дерматомицетам. Противопоказаниями для назначения аллиламинов являются аллергические реакции на препараты группы аллиламинов, беременность, кормление грудью, возраст до 2 лет, заболевания печени, сопровождающиеся нарушением ее функции (повышением трансаминаз).
Азолы — самая многочисленная группа синтетических антимикотиков. В 1984 г. был внедрен в практику первый системный противогрибковый препарат из группы азолов — кетоконазол, в 1990 г. — флуконазол, в 1992 г. — итраконазол.
Азолы, применяемые в качестве системных препаратов, обладают преимущественно фунгистатической активностью. Важным преимуществом азолов перед другими препаратами является их широкий спектр противогрибковой активности. Итраконазол активен in vitro в отношении большинства возбудителей онихомикоза — дерматомицетов (Epidermophyton spp., Trichophyton spp., Microsporum spp.), Candida spp. (C. albicans, C. parapsilosis, C. tropicalis, C. lusitaniae и др.), Aspergillus spp., Fusarium spp., S. Shenckii и др. Флуконазол активен против дерматомицетов (Epidermophyton spp., Trichophyton spp., Microsporum spp.) и Candida spp. (C. albicans, C. parapsilosis, C. tropicalis, C. lusitaniae и др.), но не действует на Aspergillus spp., Scopulariopsis spp., Scedosporium spp.
Фармакокинетика у разных азолов различна. Флуконазол (90 %) хорошо всасывается в ЖКТ. Для хорошего всасывания итраконазола необходим нормальный уровень кислотности. Если у пациента, принимающего эти препараты, кислотность понижена, то всасываемость их уменьшается и, следовательно, снижается биодоступность. Всасываемость раствора итраконазола выше, чем у капсул с итраконазолом. Итраконазол в капсулах следует принимать с пищей, а в растворе — натощак.
Итраконазол метаболизируется в печени и выводится из организма через ЖКТ. В небольших количествах он также выделяется сальными и потовыми железами. Флуконазол метаболизируется частично и в основном выводится в неизмененном виде почками (80 %).
Итраконазол взаимодействует со многими лекарственными препаратами. Биодоступность кетоконазола и итраконазола уменьшается при приеме антацидов, холиноблокаторов, Н2-блокаторов, ингибиторов протонной помпы, диданозина. Итраконазол является активным ингибитором изоферментов цитохрома Р450 и может изменять метаболизм многих лекарственных препаратов. Флуконазол влияет на метаболизм лекарственных средств в меньшей степени. Недопустим прием азолов с терфенадином, астемизолом, цизапридом, хинидином, так как могут развиться смертельно опасные желудочковые аритмии. Совместный прием азолов и пероральных антидиабетических препаратов требует постоянного контроля за содержанием глюкозы в крови, так как может развиться гипогликемия. Прием непрямых антикоагулянтов группы кумарина и азолов может сопровождаться гипокоагуляцией и кровотечениями — следовательно, необходим контроль гемостаза. Итраконазол может повышать концентрацию в крови циклоспорина и дигоксина, а флуконазол — теофиллина и вызывать развитие токсического эффекта. Требуется корректировка доз и постоянный мониторинг за концентрацией препаратов в крови. Противопоказано совместное применение итраконазола с ловастатином, симвастатином, рифампицином, изониазидом, карбамазепином, циметидином, кларитромицином, эритромицином. Флуконазол не следует применять с изониазидом и терфенадином.
Итраконазол применяют при дерматомикозах (эпидермофитии, трихофитии, микроспории), отрубевидном лишае, кандидозе кожи, ногтей и слизистых оболочек, пищевода, кандидозном вульвовагините, криптококкозе, аспергиллезе, феогифомикозе, споротрихозе, хромомикозе, эндемичных микозах, для профилактики микозов при СПИДе.
Флуконазол применяется для лечения генерализованного кандидоза, всех форм инвазивного кандидоза, в том числе и у иммуноскомпрометированных больных, генитального кандидоза, кандидоза кожи, ее придатков и слизистых. Последнее время благодаря своей безопасности и хорошей переносимости все чаще флуконазол применяется для терапии больных дерматомикозами с поражением как кожи, так и ее придатков (ногтей и волос).
Аморолфин входит в состав лака, применяемого для лечения онихомикоза. Механизм действия аморолфина заключается в нарушении синтеза эргостерола — основного компонента клеточной мембраны гриба. Он оказывает фунгистатическое и фунгицидное действие. Обладает широким спектром действия. Концентрация аморолфина в ногтевой пластинке значительно превышает МПК для основных возбудителей дерматомикозов в течение 7 дней. Поэтому аппликация препарата может осуществляться не чаще 1–2 раз в неделю, что делает его применение экономически выгодным. Противопоказания: аллергические реакции на аморолфин, грудной и детский младший возраст. Лак в качестве монотерапии назначают при поражении не более 1–3 ногтевых пластинок и не более чем на 1/2 по площади с дистального конца. Также аморолфин можно использоваться в сочетании с системными антимикотиками при более распространенном поражении ногтей (табл. 2).
Циклопирокс обладает фунгистатическим действием. Активен в отношении дерматомицетов, дрожжеподобных и мицелиальных грибов, плесеней, а также некоторых грамотрицательных и грамположительных бактерий. Циклопирокс (лак) применяется в качестве монотерапии при поражении не более 1–3 ногтевых пластинок не более чем на 1/2 по площади с дистального конца. Также циклопирокс можно использовать в сочетании с системными антимикотиками при более распространенном поражении ногтей. Противопоказания: аллергические реакции на циклопирокс, грудной и младший детский возраст, беременность и лактация.
Перечень рекомендуемых лабораторных исследований при назначении системных антифунгальных препаратов.
Лечение фоновых заболеваний. Эффективность применения антимикотиков повышается при коррекции патологических состояний, способствовавших развитию онихомикоза. Перед началом антимикотической терапии у больных с соматическими, эндокринными, неврологическими заболеваниями, с нарушениями кровообращения в конечностях необходимо провести обследование для выявления основного симптомокомплекса, способствовавшего развитию дерматомикозов. Так, основными задачами патогенетической терапии являются улучшение микроциркуляции в дистальных отделах конечностей, венозного оттока конечностей, нормализация уровня тиреотропных гормонов у больных с заболеваниями щитовидной железы, углеводного обмена у больных сахарным диабетом и т. д. В результате многолетних исследований, проведенных в Военно-медицинской академии и Санкт-Петербургской медицинской академии последипломного образования, установлено, что одной из основных причин развития дерматомикозов являются нарушения со стороны системы гипофиз–гипоталамус–гонады. Это приводит к расстройству кровообращения в дистальных отделах конечностей, нарушениям микроциркуляции, периферической иннервации. Комплекс мероприятий, направленный на коррекцию этих нарушений, включает иглорефлексотерапию, транскраниальную электростимуляцию подкорковых центров головного мозга, назначение препаратов, корригирующих работу симпатической и парасимпатической вегетативной нервной системы. Все это позволяет добиться более быстрого клинического эффекта при терапии дерматомикозов. Проведение патогенетической терапии у больных дерматомикозами с фоновыми заболеваниями целесообразно назначать до начала этиотропного лечения и продолжать ее во время всего курса приема антифунгальных препаратов.
Симптоматическая терапия дерматомикозов, направленная на уменьшение субъективных жалоб больных и объективных проявлений заболевания, не может заменить этиотропную терапию. Однако ее применение в сочетание с антифунгальными препаратами позволяет быстрее добиться улучшения состояния больных, уменьшить чувство дискомфорта и устранить косметический дефект. При онихомикозах наибольшее беспокойство больным доставляют деформированные, значительно утолщенные (гипертрофированные) ногтевые пластинки — онихогрифоз. Для коррекции этого состояния применяют аппаратный педикюр. С помощью аппарата, напоминающего стоматологическую турбину, за короткий промежуток времени механическим путем удаляются измененные участки ногтей, гиперкератотические, роговые массы с кожи, омозолелости. При этом не происходит травматизации матрикса ногтя, и пациент после процедуры остается работоспособен.
При ограниченном поражение ногтей (не более 3 ногтевых пластинок и не более чем на 1/2 по площади с дистального края) применяются препараты для местного применения. Лечение рекомендуется начинать с подчистки пораженного участка ногтевой пластинки при помощи набора «Микоспор», аппаратного педикюра или кератолитических средств. Далее на пораженную ногтевую пластинку наносятся антифунгальные препараты. Раствор аморолфина, содержащий циклопирокс, наносится на ногтевую пластинку 1–2 раза в неделю. Перед нанесением лака не нужно предварительно очищать ногтевую пластинку от предыдущих слоев препарата. Лак наносится ежедневно до полного отрастания здоровой ногтевой пластинки. На 7-й день ногтевая пластинка очищается с помощью любого косметического средства для снятия лака. В литературе встречаются противоречивые сообщения об эффективности этого метода лечения. Указывается процент излеченности больных от 5–9 до 50 %.
При распространенном поражении ногтевых пластинок на пальцах кистей комплекс лечебных мероприятий должен включать назначение системного антимикотика, подчистку ногтей и наружную терапию антифунгальными препаратами. С целью профилактики повторного заражения необходимо обработать перчатки больного, подвергнуть дезинфекции предметы личной гигиены (мочалки, полотенца, пилочки для ногтей, терки и скребки для обработки кожи и ногтей).
Препаратом выбора при лечении онихомикоза любой локализации является тербинафин. Его назначают взрослым и детям весом более 10 кг по 250 мг в сутки в течение 6 нед. Детям от 2 лет весом менее 20 кг тербинафин назначают из расчета 67,5 мг/кг в сутки, от 20 до 40 кг — 125 мг/кг в сутки в течение 6 нед. Препаратами резерва являются средства, содержащие итраконазол и флуконазол. Итраконазол применяется по двум схемам: по 200 мг ежедневно в течение 3 мес или по 200 мг дважды в день в течение 7 дней на первой и пятой неделях с начала терапии. Для лечения онихомикозов у детей итраконазол не назначается. Флуконазол рекомендуется принимать по 150 мг 1 раз в неделю в течение 3–6 мес.
Проведение комплексной терапии, состоящей из приема системного антимикотика, подчистки ногтей, местного применения антифунгальных препаратов, а также противоэпидемиологические мероприятия, обеспечивают высокую эффективность излечения онихомикоза стоп. Тербинафин назначают взрослым и детям весом более 10 кг по 250 мг в сутки в течение 12 и более недель. Детям от 2 лет весом менее 20 кг препарат назначают из расчета 67,5 мг/кг в сутки, от 20 до 40 кг — 125 мг/кг в сутки в течение 12 нед. Флуконазол рекомендуется применять по 150–300 мг 1 раз в неделю в течение 6–12 мес. Итраконазол применяется по двум схемам: по 200 мг ежедневно в течение 3 мес или по 200 мг дважды в день в течение 7 дней на первой, пятой и девятой неделях. При поражении больших пальцев стоп рекомендуется проводить 4-й курс пульс-терапии на тринадцатой неделе от начала терапии. Для лечения онихомикозов у детей итраконазол не применяется.
Критериями микологической излеченности онихомикоза являются отрицательные результаты микроскопического и культурального исследования ногтевой пластинки. После окончания лечения итраконазолом и тербинафином здоровые ногтевые пластинки отрастают не полностью, поэтому полное клиническое выздоровление можно наблюдать только спустя 2–4 мес после окончания приема антифунгальных препаратов.
Литература
Л. П. Котрехова, кандидат медицинских наук, доцент
К. И. Разнатовский, доктор медицинских наук, профессор
Н. Н. Климко, доктор медицинских наук, профессор
СПбМАПО, Санкт-Петербург



