запоры при химиотерапии что делать
Лечение после химиотерапии
Химиотерапия – один из безоперационных способов борьбы с раком. Лечение основано на введении в организм больного препаратов, которые содержат токсины и яды, сдерживающие или полностью прекращающие рост злокачественной опухоли. Химиотерапия наносит громадный урон человеческому организму. В результате воздействия ядов и токсинов повреждаются и гибнут не только атипичные клетки, но и здоровые, поражается печень, почки и другие системы. Поэтому после химиотерапии человеку необходимо лечение – комплексное, профессиональное, которое поможет справиться с побочными эффектами, пойти на поправку и полностью восстановиться.
Когда показана химиотерапия?
Решение о медикаментозном лечении онкологии принимает лечащий врач, основываясь на результатах анализов и аппаратных исследований. Как правило, к химиотерапии прибегают в следующих случаях:
Чаще всего медикаментозная терапия онкологии назначается для профилактики метастазирования ранее удалённых опухолей, а также лечения рака крови (лейкоз, гемобластоз) и других редких видов злокачественных новообразований (хориокарцинома, рабдомиосаркома). Также химиотерапия применяется для подготовки опухоли к операции – чтобы хирург мог её полностью удалить, не оставив ни единой раковой клетки.
Какие препараты химиотерапии для каких опухолей применяются
Это 2 группы средств консервативного лечения рака – цитостатики и цитотоксины. Первые проникают в атипичную клетку, нарушают её ДНК, запуская процесс самоуничтожения. Чаще всего для лечения используются следующие цитостатики: Гидроксимочевина, Фторурацил, Циклофосфан, препараты платины.
Цитотоксины уничтожают клетки – и раковые, и здоровые, вызывая тяжёлые побочные эффекты в организме у больных раком. Среди таких препаратов выделяют несколько групп:
Больше всего побочных эффектов у цитостатиков и цитотоксинов. Поэтому лечение после химиотерапии – неотъемлемая часть процесса избавления от рака. Оно позволяет ускорить восстановление клеток организма, облегчить состояние больного и улучшить качество его жизни.
Побочные эффекты химиотерапии
Рак – тяжёлое заболевание, которое требует от пациента немалых физических и эмоциональных сил для лечения. Побочные эффекты, среди которых не только физиологические, но и психологические страдания, многих выбивают из колеи, заставляя замкнуться, отгородиться от внешнего мира. Это часто приводит к ухудшению общего состояния больных раком.
Наиболее частые побочные эффекты при лечении химиотерапией:
Это лишь небольшая часть побочных эффектов при лечении рака химиопрепаратами. Реакция организма зависит не только от его индивидуальности, но и от применяемых средств. Если больному раком назначают для лечения лекарства таргетной терапии, то проблем с ЖКТ скорее всего не будет. У таких пациентов почти не бывает тошноты, рвоты, изжоги, поносов и запоров. Также большую роль играет предподготовка к лечению, которая позволяет провести реабилитацию большинства хронических заболеваний. Это помогает избежать их обострения после химиотерапии и быстрее восстановиться.
Лечение онкобольных после медикаментозной терапии рака
Применение лекарств для купирования злокачественного процесса имеет множество положительных моментов, за исключением одного – побочных эффектов. Однако с ними можно справиться, если своевременно начать лечение после химиотерапии рака.
Его назначает лечащий врач, опираясь на результаты последних анализов, аппаратных исследований и жалобы пациента. Лечение включает в себя:
Диета в пост лечении рака
Одна из распространённых реакций организма на терапию препаратами, содержащими яды и токсины – тошнота и потеря аппетита. Отказываться от еды нельзя, потому что она даёт силы для восстановления, однако рацион пересмотреть придётся.
Основные рекомендации по питанию больных раком, которые восстанавливаются после лечения химиотерапией:
Рекомендации по самому рациону касаются не только продуктов, но и приготовления различных блюд:
В день больному раком, который проходит лечение после воздействия химиопрепаратами, нужно выпивать около полутора литров жидкости. По этому вопросу рекомендуется проконсультироваться с врачом. Если наблюдается скопление жидкости в брюшине, лёгких или плевральной полости, её количество ограничивают.
Иммуномодуляторы в пост лечении рака
Химиотерапия для организма человека представляет сильнейший стресс. Больше всего повреждается костный мозг, отвечающий за кровь. После лечения её показатели значительно ухудшаются, показывая нехватку основных компонентов – лейкоцитов, эритроцитов и тромбоцитов, из-за чего возникают лейкопения, эритропения, тромбоцитопения.
Нехватка белых кровяных телец в организме сказывается на иммунитете – он становится настолько слабым, что больной может подхватить любую инфекцию или вирус, к которым ранее был невосприимчив. Для коррекции состояния больных раком лечение после химиотерапии всегда включает препараты-иммуномодуляторы, которые стимулируют гемопоэз (процесс кроветворения в костном мозге):
Иммуномодулирующие препараты применяются для улучшения качества жизни пациентов, больных раком. Их эффективность доказана более чем 30-летней практикой применения у онкологических больных во время химиотерапии и в период восстановления.
Симптоматическое лечение
Лечение расстройств ЖКТ
Первое, что делает врач – устанавливает причину состояния. Тошнота и рвота возникают не только от отравления организма больного раком при лечении токсическими противоопухолевыми препаратами. Часто это происходит в результате кишечной непроходимости – механической или динамической (отёк головного мозга, гиперкальциемия). Если ничего серьёзного не обнаружено, больному раком для лечения прописывают Церукал или Дексаметазон, если они действуют слабо, могут назначаться Зофран, Навобан, Осетрон.
Запор – один из побочных эффектов химиотерапии у особо тяжёлых больных. Здесь рекомендации врача исключительно индивидуальны. Если не стоит вопрос об оперативном лечении запора, проводят поэтапную терапию:
Диарея возникает либо как функциональное нарушение, либо как психоневрологическое осложнение после химиотерапии рака. Лечение включает в себя:
Если анализы выявляют инфекционную природу диареи, для лечения состояния назначаются антибиотики.
Печень и почки
Оба органа участвуют в фильтрации, а потому сильнее остальных поражаются при лечении от рака. Для восстановления печени сначала нужно её очистить от скопившихся в ней вредных веществ. Для этой цели применяется Легалон – препарат на основе семян расторопши. После очищения основная задача – восстановить повреждённые химиотерапией клетки печени, чтобы орган снова заработал корректно и начал выполнять свою прямую функцию – очищать кровь от вредных веществ. Для лечения используют БАДы – Эссенциале Форте, Карсил, Флор Эссенс.
С почками несколько сложнее. Агрессивное воздействие токсических/ядовитых препаратов может вызвать мочекислую нефропатию, почечную недостаточность. Для восстановления правильной работы почек применяют:
Если диагностируются воспалительные заболевания почек и мочевыводящих путей, для лечения назначаются антибактериальные препараты – Нитроксолин, Фурадонин.
Кровь
При лечении рака сильнодействующими токсичными препаратами в крови наблюдается сильная нехватка компонентов. Чтобы повысить уровень лейкоцитов, назначаются витаминные комплексы, содержащие витамины группы B, в частности B9 и 12.
Аскорбиновая и фолиевая (витамин B9) кислоты, кальций + витамин D3, магний и цинк ускорят выработку тромбоцитов. Эритроциты восстанавливаются самостоятельно. Повысить гемоглобин можно с помощью витаминов B12, B9, препаратов железа.
Психологическая помощь
Для пациентов, больных раком, свойственны стрессы и депрессия, которые загоняют человека в состояние безысходности и апатии. Это прямым образом сказывается на процессе лечения и выздоровления. Помощь психотерапевта в такой ситуации необходима. Важно найти своего врача, которому можно доверять и рассказывать о своих страхах и фобиях. Это поможет больному раком вернуться к полноценной жизни в социуме.
После каждого курса химиотерапии пациент нуждается в комплексном лечении. Выполняя все рекомендации лечащего врача, больной быстрее восстанавливается, что позволяет ему не выпадать надолго из нормальной жизни.
Что вам необходимо сделать
2. Нашим пациентам мы предлагаем курсы реабилитации:
3. Если вам понравилась статья оставьте комментарии ниже.
Практические рекомендации по лечению запора
Запор – третий по частоте симптом в паллиативной помощи после боли и анорексии. Предлагаем специалистам ознакомиться с памяткой по лечению запора у паллиативных больных, подготовленной фондом «Вера». Скачать памятку в формате pdf можно в конце статьи.
Определение
Запор – это нерегулярный и затрудненный пассаж твердых каловых масс по кишечнику или редкое отхождение малого количества твердого стула (менее 3 раз в неделю), ощущение неполного опорожнения кишечника или отхождение стула реже, чем было в норме у данного пациента до болезни.
Факт наличия запора определяется самим пациентом. Отхождение стула не должно быть обязательно ежедневным. Если стул мягкий и отходит без затруднений один раз в 2–3 дня, это можно считать нормой. Запор – третий по частоте симптом в паллиативной помощи после боли и анорексии. Частота возникновения запоров у онкологических больных колеблется от 32% до 87%, в случае приема опиоидов – 90%.
Цель всех мероприятий – профилактика запоров, а в случае их возникновения – правильное лечение.
Причины возникновения запоров
Органические факторы
● Опиоиды:
В случае высокой вероятности выраженного запора (соответствующий анамнез) предпочтительно выбирать опиоиды с меньшим влиянием на кишечник (например, Таргин).
● Другие медикаментозные средства: антациды, противорвотные (5-НТ3 антагонисты), диуретики, препараты железа, кальция.
● Метаболические нарушения: дегидратация (лихорадка, рвота, полиурия, недостаточное питье), гиперкальциемия, гипокалиемия, уремия, гипотиреоидоз, диабет.
● Неврологические нарушения: опухоли головного мозга, поражения на уровне спинального тракта, инфильтрация крестцовых нервов, вегетативные нарушения (первичные, такие как болезнь Паркинсона, множественный склероз, болезнь двигательных нейронов, или вторичные, связанные с онкологическим заболеванием).
● Структурные нарушения: опухолевые массы в малом тазу, пострадиационный фиброз, геморрой, анальные трещины, перианальный абсцесс.
Функциональные факторы
Последствия запора
Оценка/Анамнез
При сборе анамнеза, поскольку разговор затрагивает очень интимную сферу, необходимо предварительно расположить пациента к беседе. Следует обратить внимание на факторы, представленные в таблице 1.
Клинический осмотр
Обследование живота:
Пальцевое исследование прямой кишки:
Дополнительные методы обследования (в случае достаточно стабильного состояния и долгосрочного прогноза жизни):
Профилактика
Личное пространство
Для лежачих пациентов ‒ приподнимать изголовье кровати, положение на левом боку с прижатыми к животу коленями может облегчить отхождение стула.
В последние дни жизни нужно взвешивать необходимость и нагрузку для пациента при попытках получить регулярно стул. Решение принимается индивидуально, освобождение кишечника может утратить приоритетность по сравнению с купированием других симптомов.
Медикаментозное лечение запора
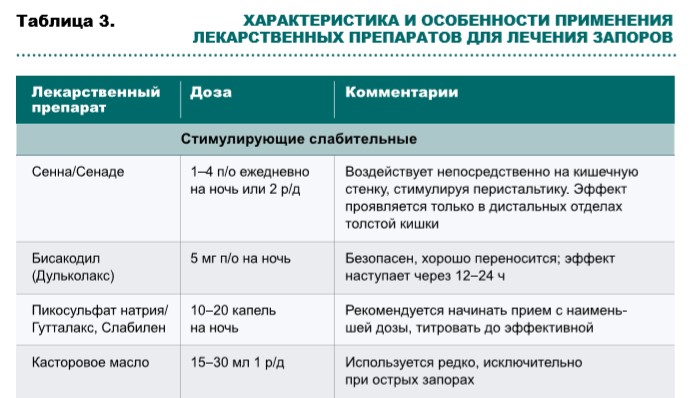
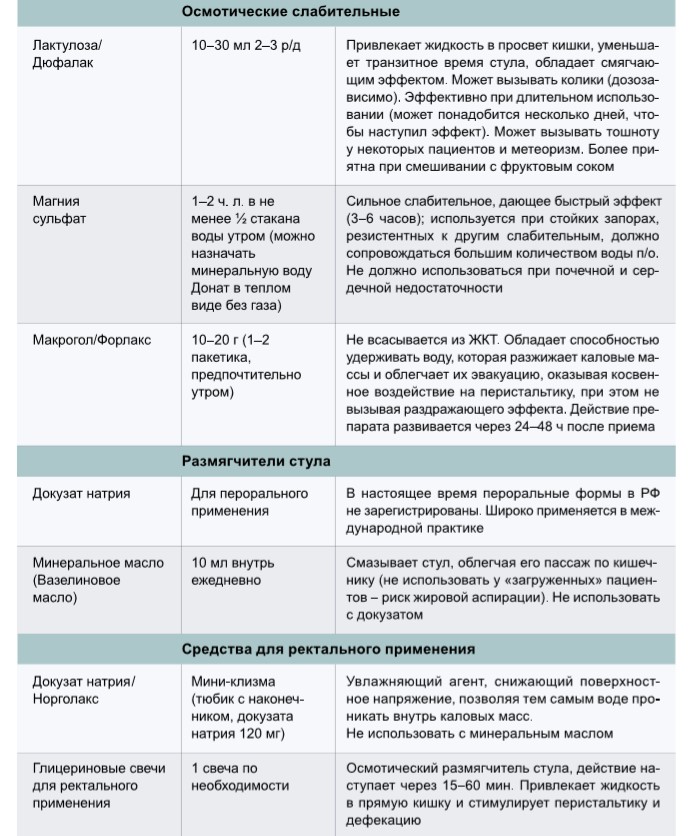
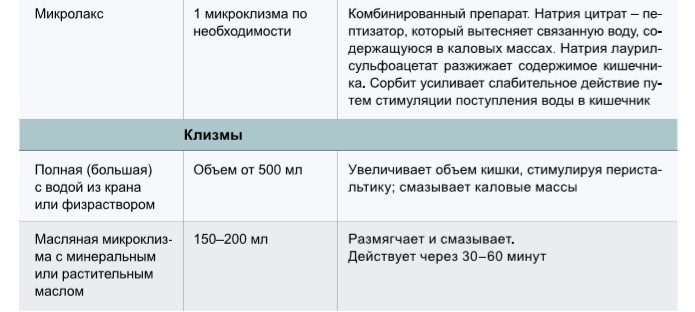
Рекомендуемые мероприятия для лечения запоров при различных клинических проявлениях данного состояния представлены в таблице 2, характеристики и особенности применения лекарственных препаратов для лечения запоров – в таблице 3.
Многие слабительные, принимаемые внутрь, ректальные свечи и клизмы имеют одинаковые побочные эффекты – спазмы, колики, метеоризм, тошнота и диарея, – степень выраженности которых можно уменьшить, титруя дозу.
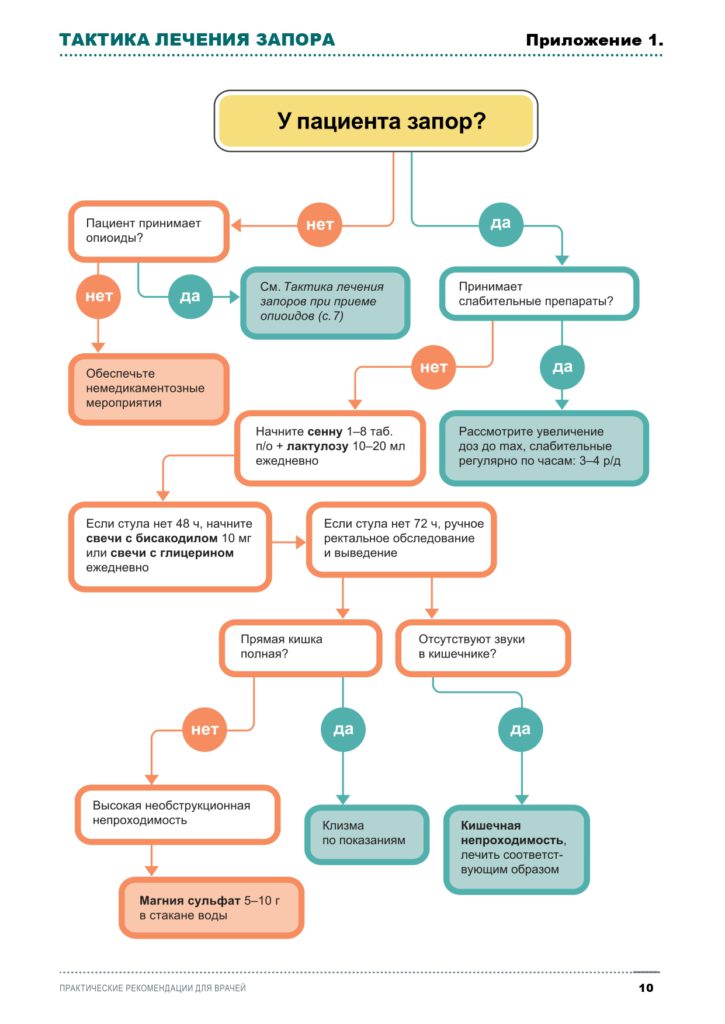
Тактика лечения запоров (см.Приложение 1)
При приеме опиоидов:
При запоре в отсутствии приема опиоидов:
При запоре, сопровождающемся признаками кишечной непроходимости:
При колостоме:
При параплегии:
Благодарим за помощь в подготовке материалов Артыкову О.В. (руководителя филиала «Хоспис «Зеленоград» ГБУЗ ЦПП ДЗМ), Крюкова А. В. (клинического фармаколога ГБУЗ ЦПП ДЗМ).
Список источников
1. Хронический болевой синдром (ХБС) у взрослых пациентов, нуждающихся в паллиативной медицинской помощи, 2016, МКБ 10: R52.1/ R52.2.
2. Introducing Palliative Care Fifth Edition. Editors Twycross R., Wilcock A., 2016.
3. Hospice and Palliative Care Training for Physicians. Unipac Self-Study Program, 2008.
4. Lanarkshire Palliative Care Guidelines, 2012.
5. ProCare HospiceCare. Hospice Medication Utilization Guidelines. Eds. S. Shah, M. Madison. www.ProCareHospiceCare.com.
6. Larkin P.J. The management of constipation in palliative care: clinical practice recommendations. Palliative Medicine, 2008; 22: 796–807.
7. Constipation Symptoms in Adults with Cancer. Cancer Care. Ontario, 2012.
Скачать памятку «Запор в паллиативной помощи» в формате pdf можно здесь:
Особенности питания пациентов с целью профилактики и лечения энтероколита, ассоциированного с противоопухолевой лучевой и химиотерапией
Войцицкий В.Е., д.м.н., профессор, заведующий кафедрой онкологии ФГБОУ ВО НГМУ Минздрава РФ. Лебедева В.А., к.м.н., доцент кафедры онкологии ФГБОУ ВО НГМУ Минздрава РФ
Энтероколит на фоне лечения онкологических заболеваний
Нарушение работы пищеварительной системы является самым частым нежелательным явлением, связанным с лучевой и химиотерапией.
Симптомами поражения кишечника после химиотерапии являются: возникновение болей в животе спазматического характера, появление урчания и вздутия живота, запоров или поносов, а также неустойчивого стула – чередования запоров с диареей. При этом позывы к опорожнению кишечника часто бывают болезненными. Иногда в каловых массах наблюдается слизь или примесь крови. В этом состоянии больной испытывает чувство вялости и слабости, иногда наблюдается повышение общей температуры тела.
Понос после химиотерапии возникает вследствие дисбактериоза в кишечнике, вызванного действием цитостатических препаратов. Также причиной поноса является поражение периферической нервной системы, которое проявляется вегетативной полинейропатией. Диарея нередко является побочным явлением и антиэметогенных препаратов сопроводительной терапии.
Диарея способствует нутритивной недостаточности и ведет к нарушениям трофологического статуса организма. Нутритивная недостаточность рассматривается как фактор повышенного риска синдрома полиорганной недостаточности в период лечения онкологических больных и приводит к росту медикаментозной нагрузки, увеличению длительности пребывания больных в стационаре и, как следствие, прямых и непрямых затрат на лечение. Известно, что коррекция статуса питания способствует улучшению прогноза выживаемости, снижению риска послеоперационных осложнений и токсичности химиотерапии, повышению качества и продолжительности жизни.
Клинические проявления энтероколита вносят свой вклад в формирование хронического болевого синдрома, который существенно снижает качество жизни больных, требует дополнительной фармакотерапии, нередко является причиной нарушения режима химиотерапии.
Изменения кишечной микрофлоры на общем фоне проблем нередко обделено врачебным вниманием. Однако, развивающийся дисбактериоз снижает эффективность пищеварения, создает условия для дополнительной нагрузки на детоксикационные системы печени, способствует развитию вздутия живота и процессов гниения в кишечнике.
Клиническая эффективность некоторых продуктов питания позволяет рассматривать их как средства, корригирующие нежелательные побочные действия фармакотерапии, или средства, повышающие эффективность лечебного воздействия фармпрепаратов. К таким продуктам питания относятся биологически активные добавки, которые сочетают в себе активные формы фармакопейных штаммов бифидобактерий, факторы роста и продукты метаболизма бифидобактерий, имеют небольшую кислотность, соответствующую кисломолочным продуктам.
Выраженные симптомы энтероколита, ректита, ректосигмоидита могут стать причиной прерывания курса химио- или лучевой терапии, что влечет за собой снижение эффективности лечения. При умеренном проявлении симптомы поражения кишечника существенно ухудшают аппетит, снижают физическую толерантность к легким физическим нагрузкам, что ограничивает возможности пациента выполнить такие рекомендации врача, как «для лучшей переносимости лечения хорошо питайтесь и чаще бывайте на свежем воздухе».
В итоге, нарушение работы кишечника может стать причиной низкой эффективности противоопухолевого лечения.
Защитная роль микрофлоры в профилактике развития энтероколита на фоне противоопухолевого лечения
Серьезным недостатком химиотерапевтических средств, применяемых при онкологических заболеваниях, является низкая селективность и связанная с этим высокая общая токсичность. Осложнения, возникающие при химиотерапии, включают как гемо- и иммунодепрессию, так и структурные поражения внутренних органов. Одним из серьезных осложнений является некротическая энтеропатия, связанная с поражением слизистой оболочки кишечника, и гепатобилиарные расстройства. С химиотерапией связано развитие дисбиоза кишечника, а именно избыточный рост и активизация Clostridiumdifficile и реже Klebsiellaoxytoca, что является одной из причин упорного течения диареи на фоне ПХТ и на долгое время после окончания ПХТ.
В здоровом кишечнике основная масса нормальных кишечных бактерий фиксирована к специфическим рецепторам энтероцитов и колоноцитов слизистой оболочки кишечника, образуя микроколонии, которые в виде биопленок покрывают поверхность слизистой оболочки. Лишь небольшая часть нормальной кишечной микрофлоры находится в просвете кишки в свободном состоянии.
Осуществляемые кишечной микробиотой метаболические процессы чрезвычайно важны для нормальной функции всех систем организма человека, и, в первую очередь, для гомеостаза и обеспечения физиологических процессов в кишечнике. Так, кишечная микрофлора поддерживает энергетический гомеостаз слизистой оболочки кишечника, синтезирует витамины, метаболизирует желчные кислоты, деградирует ксенобиотики, обеспечивает энтероциты дополнительным источником энергии за счет образования короткоцепочечных жирных кислот. Короткоцепочечные жирные кислоты обладают также иммуномодулирующим действием, супрессируют продукцию провоспалительных цитокинов, повышают толерантность слизистой оболочки кишечника к антигенной нагрузке.
Энтероциты и колоноциты относятся к клеткам с высокой скоростью обменных процессов. Покровный эпителий слизистой оболочки кишечника отличается высокой митотической активностью росткового слоя. Скорость полного обновления клеток кишечного эпителия в двенадцатиперстной и тощей кишке составляет около трех суток, в подвздошной и в толстой кишке 4-5 суток. Высокий темп пролиферации эпителиальных клеток кишечника и интенсивное обновление клеток сопровождаются процессом быстрого продвижения клеток из крипт, где они образуются, на ворсинки — место интенсивного функционирования и слущивание отработавших клеток в просвет кишки. Кишечные симбионты также являются клетками с высокой митотической активностью, что обеспечивает обновление адгезированных к слизистой оболочке микроколоний, адекватное смене эпителиальных пластов. Таким образом, кишечная микробиота и слизистая оболочка кишечника человека представляют собой взаимовыгодный симбиоз, где микрофлора защищает и питает слизистую оболочку кишечника человека, а кишечник предоставляет анатомический субстрат для фиксации и осуществления жизненных функций бактерий. Разрушение этой связи влечет за собой снижение структурной устойчивости энтероцитов и колоноцитов к воздействию агрессивных факторов, к которым несомненно относится ПХТ.
Предсказать степень сохранности кишечной микробиоты у пациентов невозможно, поскольку она достаточно чувствительна к характеру питания и образу жизни, любой длительной фармакотерапии и воздействию стрессовых факторов. Однако по этим же причинам становится ясно, что у онкологического пациента имеются в большом количестве факторы, неблагоприятно действующие на симбиоз кишечной микробиоты и кишечника человека. Патогенное влияние ПХТ на кишечник проявляется диареей. Клинически степень тяжести существенно отличается: от диареи без энтероколита до геморрагического эрозивного энтероколита. Одной из ведущих причин формирования тяжести морфологических изменений слизистой оболочки кишечника является нарушение естественной микробиоты и избыточный рост Klebsiellaoxytica. Сохраняющийся после ПХТ дисбиоз кишечника лежит в основе длительного рецидивирующего течения диареи.
Повышенное содержание просветной микрофлоры из бифидобактерий обеспечивает создание благоприятной среды для кишечных пристеночных симбионтов за счет увеличения содержания в кишечнике короткоцепочечных жирных кислот, высокого уровня колицинов, подавления роста гнилостной микрофлоры, усиления ферментативной обработки содержимого кишки. В таких условиях агрессивное действие цитостатических и гормональных препаратов на слизистую оболочку кишечника существенно менее травматично как для ворсинок кишечника, так и для микроколоний симбионтов. В свою очередь более сохранная морфологически слизистая оболочка за счет процессов обновления эпителиальных пластов скорее восстанавливает свою функциональную структуру. В конечном итоге, это приводит к отсутствию или меньшей степени тяжести клинических проявлений нарушения работы кишечника.
Пробиотические продукты питания и препараты
Совершенствование схем противоопухолевой химиотерапии путем включения в нее препаратов-корректоров побочных эффектов традиционных цитостатиков, является одной из приоритетных задач современной онкологии. Улучшение качества жизни, повышение переносимости пациентом агрессивной фармакотерапии во многом зависит от нутритивного статуса его организма и продуктов, используемых в качестве лечебного питания. По этой причине питание онкологического пациента должно быть направлено не только на обеспечение энергетических потребностей, но и обладать лечебно-профилактическими свойствами. С целью профилактики развития энтероколита перспективными представляются пробиотик-содержащие продукты питания и биологически активные добавки к пище. Пробиотические продукты питания и биологически активные добавки способствуют улучшению пищеварения и регенерации слизистой оболочки кишечника, создают в кишечнике временный микробиоценоз.
По этой причине наиболее привлекательно выглядят именно пробиотические продукты питания и биологически активные добавки, которые выпускаются в жидкой форме и небольшие по объему. При такой форме выпуска бифидобактерии выступают в роли закваски, наполняя питательную среду своими метаболитами, бактериоцинами и витаминами. В отличие от лекарственных средств в продуктах питания большое значение придается вкусовым качествам продукта. Для людей со сниженным аппетитом или анорексией органолептические свойства продукта могут стать ключевым фактором в принятии решения – пить или не пить полезный продукт. Органолептические свойства жидких лекарственных форм пробиотиков оставляют желать лучшего. По компонентному составу принято выделять: пребиотики, пробиотики, симбиотики.
Пробиотики (определение ВОЗ) – это непатогенные для человека микроорганизмы, которые способны восстанавливать нормальную микрофлору органов, а также губительно воздействовать на патогенные и условно-патогенные бактерии. Иными словами, пробиотиками называют микробы, которые в норме составляют микрофлору различных органов человека. В настоящее время к пробиотикам относятся следующие микроорганизмы: Лактобактерии (L. acidophilus, L. plantarum, L. casei, L. bulgaricus, L. lactis, L. reuteri, L. rhamnosus, L. fermentum, L. jonsonii, L. gassed); Бифидобактерии (B. bifidum, B. infantis, B. longum, B. breve, B. adolescents); Непатогенные разновидности Escherichia Coli; Непатогенные разновидности Bacillus (В. subtilis); Непатогенные разновидности Enterococcus (Enterococci faecium, Е. salivarius); Молочнокислый стрептококк (Str. thermophylus); Дрожжевые грибки Saccharomyces boulardii.
Симбиотики – препараты, содержащие в своем составе пребиотики и пробиотики.
Особенности питания при развитии энтероколита, ассоциированного с противоопухолевой лучевой или химиотерапией
Чтобы облегчить состояние больного при диарее после химиотерапии, нужно придерживаться следующих рекомендаций:
Пищу больной должен принимать в отварном, протёртом или приготовленном на пару виде. Исключаются специи, жир и грубая клетчатка растительного происхождения.
Пища принимается часто и малыми порциями, через каждые три часа. В результате получается в сутки не менее пяти – шести приёмов еды.
В рацион питания вводятся продукты закрепляющего действия – варёный рис; сухари из белого хлеба или чёрствый белый хлеб; бананы; печёные яблоки; супы на некрепком бульоне из мяса, рыбы или овощей с разваренными крупами; нежирные виды мяса и рыбы в виде паровых котлет; варёные яйца и паровые омлеты; каши в протёртом виде, напоминающие «размазню», приготовленные на воде.
Из напитков рекомендуется крепкий чай, минеральная вода, отвары из трав с дубильными веществами, соки и кисели с вяжущими свойствами, несладкие компоты из сухофруктов малой концентрации.
Чтобы возместить потерю жидкости и элеткролитов, рекомендуется принимать регидратирующие растворы Регидрон и Гастролит.
При запорах после химиотерапии рекомендуется придерживаться следующих правил:
Необходимо включить в рацион продукты, богатые клетчаткой. К ним относятся овощи, фрукты, зелень, ягоды, цельнозерновой хлеб, неочищенные крупы, семечки и орехи. Хорошо помогают справиться с запорами абрикосы, сливы, свекла, а также курага и чернослив.
Нужно каждый день пить много жидкости, не менее двух литров. К полезным напиткам относятся чистая вода, свежеприготовленные соки из фруктов и овощей, морсы и компоты, зелёный чай без сахара. Особенно полезными являются компоты из сухофруктов.
Необходимо каждодневное движение, к которому относятся прогулки пешком в течение не менее получаса. Хорошо помогает справиться с запорами езда на велосипеде и утренняя гимнастика.
Клинические исследования
Исследование влияния лечебно-профилактического и лечебного введения продукта кисломолочного обезжиренного «Биовестин-А» на токсические эффекты противоопухолевой химиотерапии (ПХТ) в тканях печени и кишечника у мышей с карциномой легких Льюис
Исполнитель: лаборатория фармацевтических исследований СО РАН ФГБУН Новосибирский институт органической химии им. Н.Н. Ворожцова – заведующая лабораторией д.б.н.. профессор Толстикова Т.Г.
Исследования проведены на 60 самках мышей линии С57Bl/6 (22-25 г, 1,5 мес.), из которых сформированы группы
В работе использовали модель экспериментальной противоопухолевой (ПХТ), имитирующей стандартную схему СНОР. При воспроизведении ПХТ мышам на 10 день после перевивки карциномы легких Льюис вводили парентерально однократно комплекс цитостатиков: доксорубицин в дозе 4 мг/кг внутривенно; циклофосфан, винкристин и преднизолон внутрибрюшинно в дозах 50 мг/кг, 0,4 мг/кг и 5 мг/кг соответственно. Продукт кисломолочный обезжиренный «Биовестин-А» вводили в двух режимах: в лечебно-профилактическом (ежедневно в течение 17-ти дней после перевивки опухоли + в течение ПХТ) и лечебном (только на фоне ПХТ с 11-го по 17-ый день после перевивки опухоли). Перевивочный материал брали из банка опухолей Института цитологии и генетики СО РАН. Данная опухоль является солидной, перевивается внутримышечно, диссеминирует гематогенно в легкие.
На 18 день после перевивки (период роста метастазов) животных выводили из опыта декапитацией. После вскрытия у животных определялась масса печени и селезенки, на гистологическое исследование брали образцы тканей печени и кишечника (тонкого и толстого).
Результаты исследования:
При лечебно-профилактическом введении продукта кисломолочного обезжиренного «Биовестина-А» на фоне опухоли без ПХТ (IV группа) у животных наблюдается уменьшение степени деструктивных процессов, по сравнению с контрольной группой. В гепатоцитах выявляется очаговая мелковезикулярная липидная инфильтрация, и лишь у одного животного наблюдалась гидропическая дистрофия в центролобулярных зонах (рис. 1).
Рис. 1. Печень животного IV группы. (ПХТ после профилактического и лечебного введения продукта кисломолочного обезжиренного Биовестина-А). Мелковезикулярная липидная инфильтрация гепатоцитов. В просвете синусоидов увеличенные купферовские клетки и клетки с липидными включениями. Окраска гематоксилином и эозином. Ув. 400.
Популяция гепатоцитов без явных признаков гетерогенности, отмечалось увеличение двухъядерных гепатоцитов по сравнению с контролем. Некрозы отдельных гепатоцитов локализовались перипортально вокруг метастазов, постнекротические мелкоочаговые гранулемы не выявлялись. В синусоидах наблюдалось большое количество клеток с липидными гранулами в цитоплазме. По сравнению с контролем незначительно увеличилось и количество купферовских клеток. В просветах синусоидов выявлялись отложения фибрина в виде гомогенных эозинофильных масс.
При лечебном введении продукта кисломолочного обезжиренного «Биовестина-А» (V группа) на фоне опухоли и ПХТ в печени существенной положительной динамики по сравнению с группой животных, получавших только ПХТ, не выявлено. У всех животных отмечалось умеренное венозное полнокровие. На фоне очагового метастазирования в гепатоцитах центролобулярных зон наблюдалась преимущественно гидропическая дистрофия. У 2 особей отмечалась дискомплесация печеночных балок и выявлялась тотальная гидропическая дистрофия в сочетании с мелковезикулярной липидной инфильтрацией гепатоцитов. Гепатоциты резко увеличены в размерах, что сопровождалось компрессией перифокально расположенных с ними гепатоцитов, которые находились в состоянии ацидофильной дегенерации. На этом фоне отмечалась и редукция синусоидального русла (рис. 2).

Морфологическое исследование влияния продукта кисломолочного обезжиренного «Биовестин-А» на цитотоксический эффект ПХТ по схеме СНОР в кишечнике мышей с перевиваемой опухолью
У всех контрольных животных (I группа) в тонком и толстом кишечнике отмечалось умеренно выраженное полнокровие подслизистой оболочки с незначительной лимфоцитарной инфильтрацией. Тонкая кишка имеет типичное строение и состоит из слизистой оболочки, подслизистой основы, мышечной и серозной оболочек. Кишечные ворсинки высокие, содержат центральное хилоносное пространство, выстланное эндотелиоцитами. Снаружи ворсины покрыты высоким однослойным призматическим эпителием с незначительным содержанием бокаловидных клеток (рис. 3). Кишечные крипты открываются в межворсинчатое пространство. В них отмечаются клетки с повышенной митотической активностью и единичные клетки Панета с эозинофильными гранулами в цитоплазме. В тонком кишечнике наблюдался незначительный отек ворсин и подслизистой оболочки. Кишечные ворсинки толстого кишечника покрыты однослойным каемчатым эпителием составляющей частью, которого, является наличие многочисленных бокаловидных клеток (рис. 4). Признаков межуточного воспаления и некротических изменений не выявлено.
При введении животным с перевитой опухолью комплекса цитостатиков (II группа) в тонком кишечнике наблюдались выраженный отек и уменьшение высоты кишечных ворсин, диапедез эритроцитов, слущивание поверхностных слоев с мелкоочаговыми некрозами эпителия и резко уменьшенное количество бокаловидных клеток. Энтероциты увеличены в размерах, с конденсацией хроматина по периферии ядер.

Рис. 3. Тонкая кишка контрольного животного. Незначительный отек кишечных ворсин. Окраска гематоксилином и эозином. Ув. 200.
.
Рис. 4. Толстая кишка контрольного животного. Незначительный отек каемчатого эпителия. Окраска гематоксилином и эозином. Ув. 100
В кишечных криптах отмечается увеличение секреторной активности в клетках Панета. Хилоносные пространства большей частью сужены, заполнены гомогенными эозинофильными массами. Также отмечалась инфильтрация подслизистой оболочки полиморфноядерными лейкоцитами (рис. 5).
Рис. 5. Тонкая кишка животного после однократного введения ПХТ. Отек ворсин, некроз и десквамация эпителия. Окраска гематоксилином и эозином. Ув. 400.
Рис. 6. Толстая кишка животного после однократного введения ПХТ. Отек ворсин и десквамация эпителия. Окраска гематоксилином и эозином. Ув. 400.
В толстом кишечнике наблюдались сходные альтеративные изменения (рис. 6). Лимфоидные фолликулы (пейеровские бляшки) в подслизистом слое не выявлялись.
При лечебно-профилактическом введении продукта кисломолочного обезжиренного «Биовестина-А» (III группа) в сочетании с ПХТотмечаются положительные сдвиги альтеративных процессов в кишечнике. У всех животных наблюдается уменьшение отека кишечных ворсин с сохранностью их высоты в тонком и толстом кишечнике (рис. 7).
Рис. 7. Тонкая кишка животного после профилактического введения продукта кисломолочного обезжиренного «Биовестина-А» и ПХТ. Уменьшение отека кишечных ворсин и сохранение их высоты. Окраска гематоксилином и эозином. Ув. 200.
В тонком кишечнике по сравнению с группой животных, получавших только ПХТ, отмечается выраженное уменьшение секреторной активности в клетках Панета с восстановлением популяции бокаловидных клеток. В области кишечных крипт выявляются активно пролиферирующие эпителиоциты. В подслизистом слое тонкого кишечника выявляется отек, незначительная лимфоцитарная инфильтрация и диапедезные кровоизлияния. В толстом кишечнике наблюдаются многочисленные пейеровские бляшки (лимфоидные фолликулы), что является свидетельством сохранения иммунной системы (рис. 8 а, б).
Рис. 8 а. Толстая кишка животного после профилактического введения продукта кисломолочного обезжиренного «Биовестина-А» и ПХТ. Незначительный отек каемчатого эпителия с инфильтрацией подслизистого слоя лимфоцитами. Окраска гематоксилином и эозином. Ув. 200.
Рис. 8 б. Толстая кишка животного после профилактического введения продукта кисломолочного обезжиренного «Биовестина-А» и ПХТ. Лимфоидный фолликул в подслизистом слое. Окраска гематоксилином и эозином. Ув. 200.
При лечебно-профилактическом введении продукта кисломолочного обезжиренного «Биовестина-А» на фоне опухоли без ПХТ (IV группа) в тонком и толстом кишечнике признаков деструктивно-некротических изменений не выявлено. В толстом кишечнике наблюдались многочисленные лимфоидные образования в подслизистом слое (Пейеровы бляшки). В тонком кишечнике отмечалась умеренная лимфоцитарная инфильтрация слизистой оболочки (рис. 9, 10).
Рис. 9. Тонкая кишка животного после профилактического введения продукта кисломолочного обезжиренного Биовестина-А. Незначительная лимфоцитарная инфильтрация кишечных ворсин. Окраска гематоксилином и эозином. Ув. 200.
Рис. 10. Толстая кишка животного после профилактического введения продукта кисломолочного обезжиренного Биовестина-А. Незначительная лимфоцитарная инфильтрация подслизистого слоя. Окраска гематоксилином и эозином. Ув. 200.
Лечебное введение продукта «Биовестин-А» привело к незначительному уменьшению выраженности экссудативно-пролиферативных процессов в тонком и толстом кишечнике (уменьшение отека кишечных ворсин и сохранение их высоты) только у двух животных. У 8 животных сохранялись выраженные признаки токсического поражения в тонком кишечнике в виде уменьшения высоты кишечных ворсин, отека и некрозов каемчатого эпителия, отсутствия бокаловидных клеток. В области кишечных крипт выявлялись активно пролиферирующие эпителиоциты. По сравнению с группой животных, получавших только ПХТ, в толстом кишечнике наблюдался лишь поверхностный отек каемчатого эпителия и выявлялись единичные лимфоидные образования в подслизистом слое.
Заключение:
Внутрижелудочное введение продукта кисломолочного обезжиренного «Биовестин-А» ежедневно профилактически в течение 10 дней до ПХТ и дополнение ПХТ ежедневным внутрижелудочным введением «Биовестин-А» предотвращает развитие энтеропатии, сохраняет лимфоидную ткань тонкого и толстого кишечника.
Влияние биологически активной добавки к пище «Биовестин» на функциональное состояние желудочно-кишечного тракта у пациентов, получающих адьювантную химиотерапию по схемам PF, TPF и FOLFOX
Лебедева В.А., Войцицкий В.Е., Чаукина В.А., Соколов А.В., Понебратец О.Ю.
Цель исследования. Установить влияние на функцию пищеварительного тракта симбиотического продукта «Биовестин» (биологически активная добавка к пище) при включении его в диету пациентов на фоне адьювантной химиотерапии по поводу колоноректального рака.
Материалы и методы.Продукт ввели в рацион 26 больных со злокачественными опухолями головы и шеи, желудка, толстой кишки, принятых на адьювантную химиотерапиюпо схемам PF, TPF и FOLFOX, включающим 2-5 суточную постоянную инфузию фторурацила. Контрольная группа из 26 больных со злокачественными опухолями аналогичной локализации получала адьювантную химиотерапиюпо схемам PF, TPF и FOLFOX без пробиотических продуктов в диете. Средний возраст пациентов группы исследования 57,2±3,41лет; средний возраст пациентов группы контроля 61,1±5,19 лет.
Проведен анализ гастро-интестинальной токсичности первого курса химиотерапии по критериям CTCAE, версия 4.03, 2010год. Шкала отражает 0-4 степени токсичности по следующим параметрам: анорексия, ухудшение аппетита, неопухолевый асцит, диарея, эзофагит, сухость рта, изжога, фистула кишки, ЖКТ-кровотечение, тошнота, рвота, тонкокишечная непроходимость, боль в животе, стоматит, гастрит, проктит, нарушение вкуса.
Показатели оценены ежедневно в первые семь дней каждого курса ПХТ.
В ходе наблюдения были выявлены следующие показатели гастро-интестинальной токсичности: анорексия, ухудшение аппетита, диарея, боль в животе, стоматит. Максимальная степень токсичности и количество случаев выявления каждого состояния представлены в таблице 1.
Таблица 1. Выявленные признаки гастро-интестинальной токсичности во время первого курса химиотерапии