гипертрофия правого желудочка у новорожденного что это
Гипертрофия правого желудочка у новорожденного что это

Поиск
Гипертрофическая кардиомиопатия у детей
На основании собственного опыта и данных литературы даётся описание генетической природы гипертрофической кардиомиопатии, её клинической картины, результатов инструментальных исследований. Обсуждается лечение. Даны критерии неблагоприятного прогноза.
Hypertrophic cardiomyopathy in children
Based on our experience and the literature describes the genetic nature of hypertrophic cardiomyopathy, its clinical presentation, results of instrumental studies. It is discuss the treatment. Some criteria of poor prognosis were held.
Гипертрофическая кардиомиопатия (ГКМП) – структурное и функциональное поражение миокарда с увеличением его толщины (массы) с известным или предполагаемым генетическим дефектом белка саркомера кардиомиоцитов, наследуемое аутосомно-доминантно с различными пенетрантностью и экспрессивностью при отсутствии системной гипертензии, болезней накопления, гипотиреоза, атеросклеротического коронаросклероза, пороков клапанов, врождённых пороков сердца и других состояний, которые бы могли объяснить увеличение массы миокарда. Современные возможности лечения ГКМП с длительной поддержкой достаточно высокого качества жизни актуализировали проблемы ранней диагностики и адекватного выбора тактики ведения пациента [1, 2].
Этиология.ГКМП наследуется по законам Менделя по аутосомно-доминантному типу. Форма заболевания у пробандов и их ближайших родственников совпадают в 60% случаев. Гены, ответственные за заболевание, локализуются на 6 хромосоме (15 генов) и на длинном плече 14 хромосомы [3]. Изменения генов представлены более чем 400 миссенс-мутациями, ответственными за регуляторные, структурные или функциональные характеристики тонких или толстых нитей кардиальных саркомеров (тяжёлая цепь β-миозина, актин, титин, миозин-связывающий протеин С, тропомиозин Т и др.). Само по себе число мутаций и определяет клиническую вариативность ГКМП. Более половины всех генетически идентифицированных случаев ГКМП определяются мутациями 3 генов, определяющих дефекты тяжёлой цепи β-миозина, миозин-связывающего протеина С, кардиального тропонина Т. Другие 13 генов ответственны за нечастые случаи дефектов титина, α-тропомиозина, α-актина, кордиального тропонина I, лёгкой цепи миозина. Но среди людей с клинически и инструментально диагностированной ГКМП и подвергшихся молекулярно-генетическому тестированию, аномалии генов выявлены только в 50-80% случаев [4, 5]. Это значит, что в 20-50% мы имеем дело с ещё не идентифицированными мутациями. Вполне вероятно, что для разных популяций будут характерны свои мутации. Так, высказывается мнение, что для российской популяции может быть характерна миссенс-мутация в гене β-MHC.
Полиморфизм клинической картины объясняется недостаточно изученным взаимодействием различных генов (мутация MYH7 – выраженная гипертрофия, раннее начало и тяжёлое течение; мутация TNNT2 – умеренная гипертрофия; мутация MYBPC3 – неполная пенетрантность и относительно поздний дебют), пола, внешних факторов.
Патофизиология. Дефект гена приводит к дискоординации деятельности миофибрилл и с последующим фиброзом и гипертрофией миокарда. Хаотичность клеточной структуры возникает уже в областях без признаков гипертрофии и являющихся аритмогенным субстратом желудочковых тахикардий и фибрилляций. Одновременно утолщается интима интрамуральных коронарных артерий, нарушается транспорт кислорода в утолщенный миокард, возникают ишемия, гибель клеток, склероз. Стенки желудочков утолщаются, но внутренний размер остаётся неизменным или даже уменьшается. Систолическая функция длительное время не изменяется, ригидность миокарда резко повышается, возрастает конечно-диастолическое давление, тормозится возврат крови. Гипертрофированный миокард может сужать выносной тракт ЛЖ. Степень обструкции варьирует в зависимости от толщины межжелудочковой перегородки, расположения митрального кольца, переднесистолического движения створок митрального клапана, интенсивности сокращения миокарда (поэтому противопоказаны препараты дигиталиса). Степень обструкции не коррелирует с риском внезапной смерти. Прогрессия болезни приводит к дилятации желудочков.
В эксперименте на животных с положительным ГКМП-генотипом, но отрицательным фенотипом показано, что назначение блокаторов кальциевых каналов до развития гипертрофии способно предотвратить заболевание [6]. Такая экспериментальная терапия проводится и у людей, пресимптомных носителей генотипа ГКМП.
Распространённость ГКМП у детей составляет 3-5: 1 млн, медиана возраста – 7 лет, 1/3 всех случаев диагностируется в возрасте до 1 года. У 25-58% родственников 1 степени выявляются эхографические признаки ГКМП. Частота ГКМП приблизительно одинакова в различных популяциях, хотя в Азии чаще встречаются атипичные варианты ГКМП. Среди детей гендерных различий в частоте ГКМП, но во взрослом состоянии, заболевание чаще выявляется у мужчин. Различия объясняют гормональными факторами, влиянием внешней среды, более яркой симптоматикой или большей степенью обструкции выносного тракта ЛЖ у мужчин. Всё это и обуславливает более частые исследования, приводящие к диагностике ГКМП.
Клиническая картина. Жалобы могут отсутствовать, и в этих случаях диагностика ГКМП является результатом случайных эхокардиографических исследований. По результатам собственных исследований (84 больных), чаще встречаются указания на обмороки, одышку, чувство перебоев в сердце и др. По результатам суточного мониторирования артериального давления, регистрируется склонность к брадикардии, видимо, за счёт снижения выброса из ЛЖ.
Одышка – один из самых ранних симптомов и встречается у 90% больных. Одышка обусловлена высокой ригидностью утолщенного миокарда, повышением конечно диастолического давления и переносом давления на малый круг кровообращения.
Обмороки и предобморочные состояния типичны для ГКМП, особенно для детей и подростков с малым диаметром ЛЖ и желудочковой тахикардией или синдромом слабости синусового узла или дисфункцией синусового узла при суточном мониторинге. В нашей группе пациентов они встречались у 27%, чаще при обструктивной форме ГКМП. Наличие обмороков – показатель высокой вероятности внезапной смерти. Предобморочные состояния, возникающие при резком переходе в вертикальное положение, могут быть обусловлены преходящими предсердной или желудочковой тахиаритмией и рассматриваются как предиктор внезапной смерти.
Головокружения часто беспокоят детей с ГКМП с высоким градиентом в выносном тракте ЛЖ и усиливаются при физической нагрузке или при гиповолемии (обильное отделение пота при жаре), быстром переходе в вертикальное положение или реакцией Вальсальвы при дефекации. Головокружение может быть при нарушениях ритма со снижением перфузии мозга. Кратковременные эпизоды нарушения ритма проявляются пресинкопами и головокружением, в то время как устойчивые нарушения ритма приводят к обморокам и внезапной смерти.
Ангинозные боли типичны для детей с ГКМП. При этом нет атеросклеротического коронаросклероза. Симптоматика ишемии миокарда объясняется повышенной потребностью утолщенного миокарда в кислороде, что при нарушении диастолы приводит к субэндокардиальной гипоксии, особенно при физических нагрузках. Чувство перебоев в сердце объясняется преждевременными предсердными или желудочковыми сокращениями, интермиттирующим атрио-вентрикулярным блоком, суправентрикулярной или желудочковой тахикардией. Недиагностированная желудочковая тахикардия – показатель высокого риска внезапной смерти.
Ортопноэ и пароксизмальная ночная одышка – признаки сердечной недостаточности при тяжёлых вариантах ГКМП с венозным застоем в лёгких. Застойная сердечная недостаточность у детей встречается всего в 10% случаев (значительно реже, чем у взрослых) и в основном в возрасте до 1 года. Она свойственна пациентам с наиболее выраженным утолщением миокарда. Застойная сердечная недостаточность является результатом двух повреждающих факторов: высокой ригидности миокарда и субэндокардиальной ишемии.
Верхушечный толчок разлитой, приподнимающий, смещён влево. Типичен двойной толчок, верхняя часть которого образована усиленным сокращением левого предсердия. Самым типичным для ГКМП является тройной верхушечный толчок, последняя часть которого вызвана изометрическим сокращением желудочка. Но этот вариант встречается крайне редко.
Венозный югуллярный пульс – выраженная волна «а» на флебограмме: резкое повышение конечно диастолического давления в ЛЖ с повышением давления в малом круге кровообращения и утолщение межжелудочковой перегородки с уменьшением полости правого желудочка, в итоге, с торможением притока к нему.
Кародитный пульс высокий, быстрый и короткий, что объясняется высокой скоростью потока крови через суженный выносной тракт ЛЖ. В ряде случаев каротидный пульс предстаёт как последовательная двойная пульсация сонной артерии: 1 пик – как описано ранее, 2-ой – невысокий подъём артерии в поздней систоле после падения градиента.
Аускультативно I тон не изменён, II — обычно расщеплён, при очень высоком градиенте – парадоксально. Нередко выслушивается ритм галопа или III тон, но при ГКМП он не имеет такого прогностического значения как при клапанном стенозе аорты. Часто определяется IV тон за счёт форсированной систолы предсердия, преодолевающего сопротивление притоку крови в ЛЖ. Систолический шум выброса ромбовидный (кресчендо-декресчендо) наилучшим образом выслушивается в точке между верхушкой и левым краем грудины, ирраидиирует надгрудинно, но не передаётся на сонные артерии. Интенсивность шума определяется субаортальным градиентом в выносном тракте ЛЖ. Так как степень градиента давления варьирует в зависимости от обструкции, объёма притекающей крови, интенсивность шума непостоянна. Шум уменьшается при увеличении преднагрузки: проба Вальсальвы, проба Мюллера (после форсированного выдоха движение вдоха совершается при закрытых рте и носе (возникает субатмосферное давление в грудной клетке и лёгких = инвертированная проба Вальсальвы), положение на корточках. Градиент увеличивается и шум становится громче при снижении преднагрузки (нитраты, диуретики, в положении стоя) или снижении после нагрузки (вазодилятаторы). Голосистолический шум возникает при переднесистолическом движении митрального клапана и очень высоком градиенте в выносном тракте ЛЖ. У 10% детей с ГКМП выслушивается диастолический шум декресчендо регургитации на аортальном клапане, но при доплерографии минимальная и умеренная аортальная регургитация определяется у 33%.
Дополнительные исследования. Электрокардиографически чаще всего выявляются признаки гипертрофии ЛЖ, отклонение электрической оси сердца, нарушения проводимости, синусовая брадикардия (33%) с эктопическим предсердным ритмом и расширением предсердия. При мутации аденозинмонофосфат активированном PRKAG2 ГКМП сочетается с врождённым синдромом Вольф-Паркинсон-Уайта и нарушениями проводимости.
Сравнительно часто встречаются глубокие зубцы Q в прекардиальных отведениях (40%), фибрилляция предсердий (плохой прогностический признак) и аномалии волны Р. Величина зубца Q прямо коррелирует с толщиной миокарда задней стенки ЛЖ (рис. 1).
Рисунок 1. Электрокардиограмма больного Н. 5 лет с обструктивной формой ГКМП. Отмечается патологически глубокий зубецQ в отведениях I, AVL, V5-V6. Снижен вольтаж зубцаR в отведениях II, III, AVF, V6. Толщина межжелудочковой перегородки по данным ЭХОКГ составляет 1,5 см, задней стенки левого желудочка — 0,7 см.
ЗубецQ в отведениях II, III, aVFрегистрировался преимущественно у больных с умеренной изолированной гипертрофией миокарда. При тяжёлом прогрессирующем течении ГКМП помимо отведений II, III, aVF зубец Q регистрировался в отведениях V4-V6, при комбинированой гипертрофии миокарда ЛЖ и правого желудочка – в отведениях I, II, aVL, V4-V6. Можно предположить, что патологический зубец Q является не только изолированным признаком гипертрофии межжелудочковой перегородки, но и косвенным признаком особенностей гипертрофии ЛЖ. Типичны изменения процесса реполяризации: снижение амплитуды волны Т (21% обследованных), его выраженная инверсия (61%) вплоть до гигантских отрицательных Т в отведениях V1-V6. Для больных с обструктивной формой ГКМП характерны атриовентрикулярные блокады.
При холтеровском мониторировании нарушения ритма и проводимости регистрируются значительно чаще, чем при одномоментной записи ЭКГ.
Существуют большие и малые ЭКГ-критерии ГКМП. Большие критерии включают в себя: 1) изменение волны Q (>40 мсек или 1/3R) по меньшей мере в 2х отведениях и 2) инверсия волны Т (≥3 мм) по меньшей мере в 2х отведениях. Малые: 1) увеличение левого предсердия (Pv1), 2) PR
Закономерности изменений показателей ультразвукового исследования при врожденных пороках сердца у плода в зависимости от особенностей внутрисердечной гемодинамики антенатального периода
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Врожденные пороки сердца редко влияют на развитие плода. Впервые это было отмечено в исследованиях B. Mac Mahon и соавт. [1]. Однако есть пороки, не совместимые с жизнью, и после рождения ребенок тотчас погибает. Некоторые врожденные пороки сердца, даже несложные формы, в раннем неонатальном периоде протекают злокачественно, обусловливая развитие декомпенсации кровообращения и дыхательную недостаточность. Главной причиной этого является несовершенство компенсаторных механизмов.
Антенатальный период характеризуется особенностями кровообращения, такими как высокое давление в правом желудочке, незначительный объем кровотока в легочной артерии, параллельность работы желудочков сердца, функционирующие артериальный проток и овальное окно, нагнетающие кровь как обходные анастомозы в большой круг кровообращения за счет усиленной работы правого желудочка. Эти особенности внутрисердечной гемодинамики плода, безусловно, должны корректировать характер гемодинамических изменений ультразвуковых показателей сердца в норме и при пороках сердца у плода.
Известно, что у пациентов с врожденными пороками сердца нарушения гемодинамики в результате анатомических изменений в значительной степени влияют на данные ультразвукового сканирования сердца, такие как размеры полостей сердца, степень гипертрофии миокарда, функция клапанного аппарата, сократительная способность миокарда, направленность движения межжелудочковой перегородки.
Метод оценки внутрисердечной гемодинамики базируется на широко известных понятиях о систолической, объемной и смешанной перегрузках сердца, предложенных в 1952 г. E. Cabrera и J. Monroy [2].
В основе разделения использован следующий принцип.
Нагрузка сопротивлением возникает при ситуации, когда выброс крови из желудочков сердца в магистральные сосуды затруднен на уровне полулунных клапанов (стеноз аорты и легочной артерии), подклапанного пространства (идиопатический гипертрофический субаортальный стеноз, подклапанный стеноз аорты или легочной артерии), на протяжении сосудистого русла (коарктация аорты) либо при значительном увеличении выходного сопротивления (синдром Эйзенменгера). В результате затруднения выброса крови резко возрастает напряжение миокарда соответствующего желудочка при относительно стабильном объеме крови, что служит проявлением систолической перегрузки сердца. При систолической перегрузке желудочков сердца независимо от нозологической формы порока полость желудочка, несущего основную нагрузку сопротивлением, умеренно увеличивается в размерах. В ответ на нагрузку сопротивлением на эхокардиограмме выявляется гипертрофия миокарда соответствующего желудочка, и чем больше сопротивление выбросу, тем резче выражена степень гипертрофии миокарда соответствующего желудочка и межжелудочковой перегородки (рис. 1) [3].
Нагрузка объемом возникает при дополнительном притоке крови в желудочки и в результате шунтирования крови через септальные перегородки или артериальный проток (дефекты межпредсердной и межжелудочковой перегородок, открытый артериальный проток), а также в результате обратного тока крови через атриовентрикулярные клапаны (клапанная недостаточность).
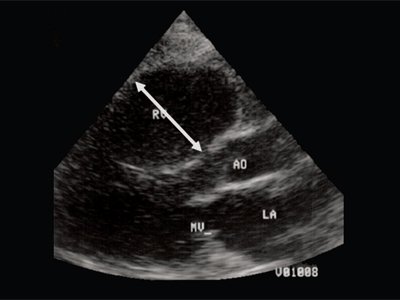
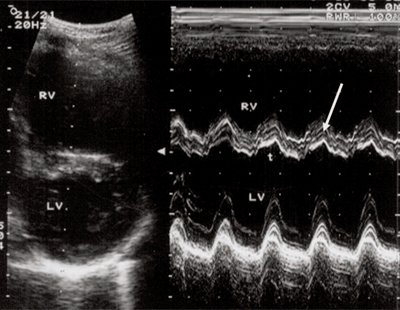
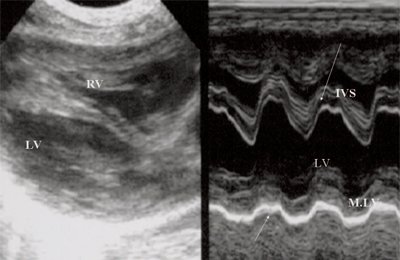
Характерными особенностями выраженной объемной перегрузки правого желудочка являются дилатация желудочка, при которой толщина миокарда не превышает верхней границы нормы, увеличение правого предсердия, парадоксальный характер движения межжелудочковой перегородки и увеличение амплитуды движения трикуспидального клапана (рис. 2, 3).
Рис. 2. Длинная ось сердца. Объемная перегрузка правого желудочка при дефекте межпредсердной перегородки. Объем сброса крови превышает 200% МОС. Отмечается выраженная дилатация правого желудочка.
Рис. 3. Объемная перегрузка правого желудочка при дефекте межпредсердной перегородки. В- и М-сканирование. Стрелкой показан парадоксальный характер движения межжелудочковой перегородки.
Для левого желудочка признаком объемной перегрузки являются увеличение полости левого предсердия и желудочка, а также экскурсии межжелудочковой перегородки и миокарда задней стенки левого желудочка (рис. 4).
Рис. 4. Объемная перегрузка левых отделов сердца. В- и М-сканирование. Отмечается усиление экскурсии межжелудочковой перегородки и миокарда задней стенки левого желудочка.
При сочетании нагрузки сопротивлением и объемом возникает смешанная перегрузка (например, при дефекте межжелудочковой перегородки и повышении давления в легочной артерии для правого желудочка систолическая перегрузка сочетается с нагрузкой объемом, для левого желудочка в результате артериальновенозного сброса крови через дефект).
За многолетний период (с 1980 г. по настоящее время) наблюдений в ФГУ Научный центр акушерства, гинекологии и перинатологии им. В.И. Кулакова Минздравсоцразвития России было замечено, что в антенатальном периоде не всегда работают принципы гемодинамических эхокардиографических проявлений врожденного порока сердца, которые ранее были разработаны и представлены в современной литературе 6.
Анализ более 2000 наблюдений врожденных пороков сердца у плода показал, что в ряде наблюдений имеются лишь анатомические изменения, характерные для определенной нозологической формы порока. При других врожденных пороках сердца изменения на эхокардиограмме связаны с характером гемодинамической нагрузки на сердце и аналогичны тому, что наблюдается после рождения. Наконец, в ряде наблюдений врожденных пороков сердца у плода вторичные изменения на эхокардиограмме, вызванные гемодинамическими нарушениями, отличаются от гемодинамических проявлений ультразвуковых показателей у детей и взрослых. Это позволило разделить все врожденные пороки сердца плода на три группы в зависимости от изменений на эхокардиограмме, обусловленных особенностями антенатальной внутрисердечной гемодинамики.
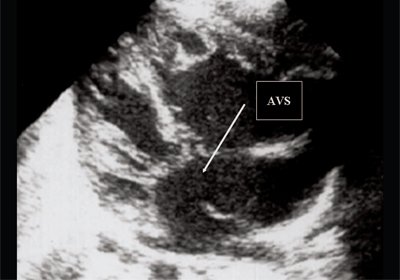
Рис. 5. Четырехкамерное сечение сердца плода. Стрелкой указан первичный дефект межпредсердной перегородки (АVS).
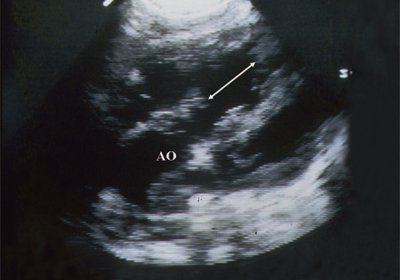
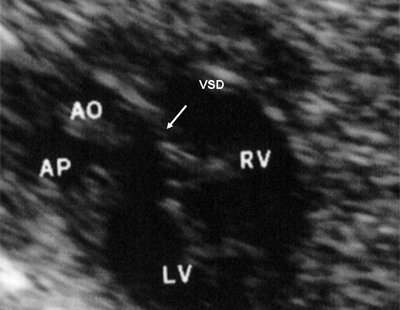
Рис. 6. Дефект межжелудочковой перегородки. Длинная ось сердца. Стрелками показан дефект межжелудочковой перегородки.
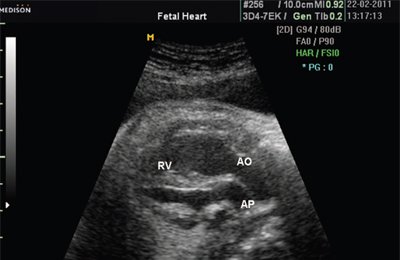
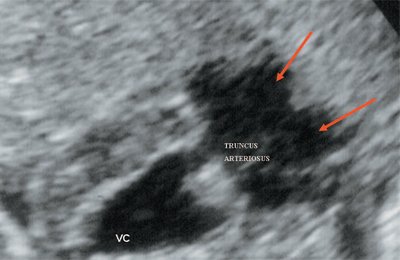
Рис. 7. Транспозиция магистральных сосудов.
Рис. 8. Транспозиция магистральных сосудов, стрелками показаны ветви легочной артерии.
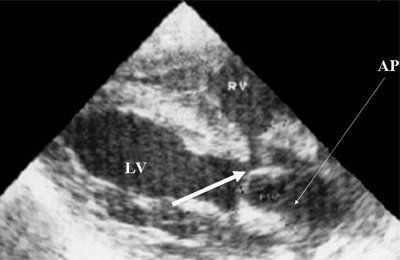
Рис. 11. Двойное отхождение магистральных сосудов от левого желудочка. Длинная ось сердца. Магистральные сосуды инвертированы и отходят от левого желудочка. Аорта расположена «верхом» над дефектом межжелудочковой перегородки (стрелка).
Таким образом, диагностика перечисленных выше врожденных пороков сердца основывается на знании анатомических изменений, характерных для определенной нозологической формы патологии.
Вторая группа врожденных пороков сердца. При ультразвуковом исследовании регистрируются анатомические и гемодинамические изменения, характерные для определенной нозологической формы порока. В эту группу были отнесены: стеноз аорты, стеноз легочной артерии, врожденный митральный стеноз, транспозиция магистральных сосудов с сужением легочной артерии, обструкция опухолью выходного тракта одного из желудочков, аномалия Эбштейна, синдром гипоплазии правого и левого желудочков сердца, фиброэластоз, преждевременное закрытие овального окна.
Как пример можно разобрать изменения эхокардиографических показателей при клапанном стенозе легочной артерии. Нарушение гемодинамики при изолированном стенозе легочной артерии обусловлено препятствием на пути выброса крови в легочную артерию. Тяжесть стеноза определяется разницей систолического давления в правом желудочке и легочной артерии, т.е. градиентом давления.
При двухмерной эхокардиографии выявляется утолщение створок клапана легочной артерии, экскурсия их уменьшена, а в систолу они образуют купол. Это анатомические проявления порока. К ним добавляются гемодинамические проявления: выраженная гипертрофия миокарда передней стенки правого желудочка и межжелудочковой перегородки, значительно превышающие нормативы. Степень выраженности гипертрофии миокарда правого желудочка зависит от степени стенозирования легочной артерии и соответственно от величины градиента давления. Эти данные получены при сопоставлении результатов ультразвукового сканирования и данных катетеризации полостей сердца у детей [6]. Следует особо отметить, что при выраженной гипертрофии миокарда полость правого желудочка увеличивается незначительно. Отмечается также увеличение размера правого предсердия.
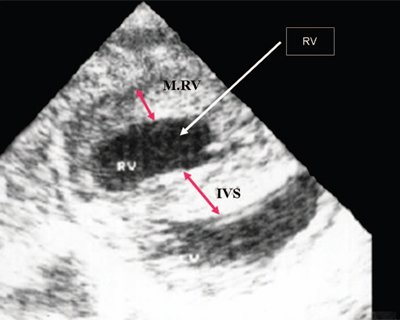
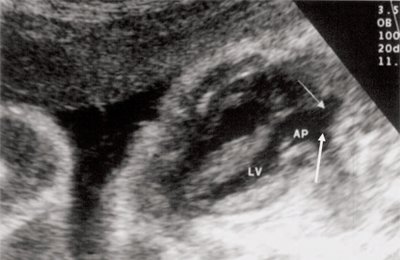
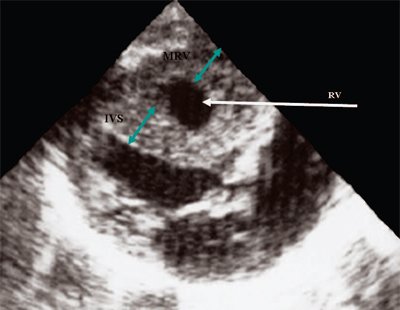
У плода получены аналогичные изменения, зависящие также от степени стенозирования легочной артерии. Полость правого желудочка, как видно на рис. 12, не увеличена. В то же время имеется значительная гипертрофия стенок правого желудочка. Как и в постнатальном периоде отмечено увеличение полости правого предсердия (рис. 13). После рождения при катетеризации полостей сердца в данном наблюдении был выявлен градиент давления на выходе из правого желудочка, равный 200 мм рт.ст.
Рис. 12. Стеноз легочной артерии. Гипертрофия миокарда правого желудочка.
Гипертрофия сердца у детей
Гипертрофия сердца представляет собой увеличение сердца в размерах. Это состояние сердца, которое может привести к серьезным нарушениям в структуре и работе сердца. Сердце увеличивается за счет того, что клетки, кардиомиоциты, разрастаются. Они составляют около 25 % всех клеток этого органа.
Известно, что сердце представляет собой полый орган из четырех камер: левого предсердия и желудочка, правого предсердия и желудочка. В этих камерах циркулирует кровь. В предсердия кровь поступает, а из желудочков выталкивается. При нормальном процессе картина будет такой: давление в левой стороне сердца всегда в норме выше, чем в правых камерах. Это происходит потому, что камеры левой части сердца участвуют в большом круге кровообращения (системном круге), а правые – в малом круге кровообращения.
При патологиях сердца эта закономерность может в той или иной степени изменяться. Врачи отмечают гипертрофию разных отделов сердечных камер, хотя частота встречаемости у детей гипертрофии того или иного отдела сердца неодинакова.
Ученые генетики изучают тему наследственных причин развития гипертрофии у детей и взрослых. Раньше считалось, что это заболевание пациентов разного возраста связано с разными генетическими предпосылками. На данном этапе установлено, что мутации могут быть причиной гипертрофии как у детей, так у более взрослых пациентов.
К формам гипертрофии сердца у детей относятся:
Гипертрофия правого желудочка
Данная патология встречается у детей чаще, чем у взрослых и связана с увеличением и удлинением мышечных волокон в результате усиленного функционирования. Нередко патология носит физиологический характер и связана с тем, что в первые месяцы жизни увеличивается нагрузка на отделы желудка. Однако чаще прослеживается взаимосвязь гипертрофии с врожденными пороками сердца, которые приводят к тому, что правый желудочек получает большее количество крови, чем он в состоянии обработать (при пороке ток крови может нарушаться). Это приводит к перегрузке в работе правого желудочка.
Увеличенный миокард теряет свои физиологические свойства. Нарушается электропроводимость, вызывающая, в свою очередь, аритмию, изменения в сократительной способности и другие нарушения.
Следует отметить, что при возникновении гипертрофии правого желудочка подвергаются негативному воздействию и сосуды с ним связанные, что, в конечном счете, может привести к их склеротизации и нарушению функционирования малого круга кровообращения.
Основными методами диагностики заболевания являются электрокардиография и эхокардиография (УЗИ). Первый метод может указывать на нарушение электропроводимости сердца и считается косвенным методом. Второй метод более информативен. Он указывает на точные размеры сердца, наличие стеноза, расположение дефектов, позволяет оценить давление в камерах и т.д. Два эти метода дополняют друг друга, потому что не всегда диагноз гипертрофии правого желудочка может подтверждаться ультразвуковым исследованием.
Гипертрофия левого желудочка
При этой патологии стенка желудочка утолщается. Бывает, что утолщается перегородка между правой и левой желудочной камерой. Утолщение может быть неравномерным, от чего зависит течение заболевания.
Это достаточно часто встречающееся состояние среди детских болезней сердца при таких патологиях:
Характерные признаки гипертрофии левого желудочка неоднородны. Больной может не знать о наличии у него данного заболевания. Генетики отмечают большую вероятность передачи заболевания по наследству, поэтому грамотный врач изучает картину семейного анамнеза.
Диагностика гипертрофии левого желудочка у новорожденных достаточно сложна, потому что у них наблюдается преобладание массы правого желудочка. В современной педиатрии и кардиологии диагностика гипертрофии левого желудочка выделена в отдельную область изучения. Наиболее информативными являются как электрокардиография (ЭКГ), так и эхокардиография.
Лечение данного заболевания может быть как хирургическим, так и медикаментозным. Во время операции перегородка приводиться к нормальному физиологическому состоянию.
Гипертрофия предсердий
Относительно часто встречающаяся патология у детей. Она наблюдается в случае одновременного нарушения митрального клапана и трикуспидального клапана, при других пороках сердца, которые носят врожденный характер, а также при дефекте перегородки предсердий. Также гипертрофия обоих предсердий возникает как сопутствующее нарушение при кардитах.
Врачи отмечают, что диагностика биатриального увеличения (гипертрофии предсердий) более сложна, чем при изолированных дефектах предсердий. Также как и при других видах гипертрофии, основными методами диагностики являются ЭКГ И УЗИ сердца.
Гипертрофия миокарда желудочков
Основой нормального движения крови является работающий без нарушений миокард обеих желудочков и синхронная сократительная способность обеих камер. Но при нарушении физиологически нормальной работы сердечной системы, создающего препятствия или изменения в направлении тока крови приводят к интенсивной его работе. В результате большей нагрузки развивается гипертрофия сердца, которая сочетается с одновременным изменением в самом миокарде. Ухудшается проводимость, метаболизм.
Заболевание достаточно распространено у детей раннего возраста. Но диагностика его, особенно в раннем детстве, достаточно сложна. По сравнению с диагностикой гипертрофии предсердий, выявление нарушения миокарда желудочков считается более сложной задачей, так как труднее уловить асинхронность в работе правого и левого отделов.
Гипертрофия предсердий
Гипертрофия левого предсердия встречается у детей при следующих заболеваниях:
Гипертрофия правого предсердия, по сравнению с патологией левого предсердия, встречается значительно реже у пациентов детского возраста. Процессу увеличения правого предсердия дают начало такие заболевания, например, как:
В заключении следует отметить, что в зависимости от степени патологии и ее видов врач назначает либо консервативное лечение, либо настаивает на необходимости проведения хирургической операции.