гомозиготная форма семейной гиперхолестеринемии
Семейная гиперхолестеринемия (СГХС) – наследственная патология, характеризующаяся выраженным повышением количества липопротеинов низкой плотности (ЛПНП) в кровотоке и высоким риском раннего развития ишемической болезни сердца. В большинстве случаев протекает бессимптомно. Иногда отмечается боль в груди, волдыри на руках, коленях и вокруг глаз, сухожильные и подкожные отложения холестерина. Основные методы диагностики – сбор наследственного анамнеза, анализ крови на общий холестерин и ЛПНП. Для лечения используется гиполипидемическая диета, регулярные физические нагрузки, медикаментозная коррекция липидоснижающими препаратами, аферез атерогенных липопротеидов.
МКБ-10
Общие сведения
Синонимы семейной гиперхолестеринемии – первичная, наследственная гиперхолестеринемия. Является не самостоятельным заболеванием, а состоянием предрасположенности к сердечно-сосудистым болезням – атеросклерозу сосудов, ИБС, острому инфаркту миокарда. Данные о распространенности СГХС имеют большой разброс, поскольку во многих случаях патология остается недиагностированной. Частота гетерозиготной формы, при которой у пациента имеется один дефектный ген из пары, составляет 1 случай на 108-300 человек. Гомозиготная форма, характеризующаяся наличием двух мутационных генов в аллели, протекает тяжелее и встречается гораздо реже – у 1 человека из 1 миллиона. Среди всех вариантов гиперхолестеринемии на долю семейной ГХС приходится 10% случаев.
Причины
СГХС является наследственной аутосомно-доминантной патологией, которая вызывается мутацией генов, ответственных за метаболизм ЛПНП и активность их рецепторов. При наличии одного дефектного гена в паре возникает гетерозиготная гиперхолестеринемия – легкое и умеренное нарушение метаболизма липидов. В редких случаях у пациентов присутствует два парных измененных гена (от матери и от отца), развивается гомозиготная гиперхолестеринемия – тяжелое расстройство липидного обмена со злокачественным течением. Причиной семейной гиперхолестеринемии является мутация в одном из следующих генов:
Патогенез
В основе семейной гиперхолестеринемии лежит генетически обусловленное повышение уровня ЛПНП. Чаще всего оно вызывается снижением активности специфического рецептора, ответственного за выведение липопротеинов. ЛПНП – наиболее атерогенные частицы. Атеросклеротические бляшки формируются при их накоплении в субэндотелиальном пространстве. Чем выше уровень липопротеинов с низкой плотностью в крови, тем интенсивнее протекает процесс.
Хуже всего ЛПНП выводятся у людей с гомозиготной первичной гиперхолестеринемией: оба парных гена имеют мутацию, функциональность рецептора снижена на более чем на 50%, концентрация ЛПНП высокая, плохо поддается коррекции при помощи медикаментов и диеты. Атеросклероз и его осложнения развиваются в детском и подростковом возрасте. При гиперхолестеринемии гетерозиготного типа только один ген дефектный, половина или более рецепторов остаются функциональными, количество ЛПНП повышается, но долгое время не проявляется клинически. Зачастую первым признаком СГХС становится атеросклероз, ишемическая болезнь сердца или инфаркт миокарда.
Симптомы
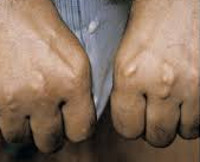
СГСХ развивается с рождения, но часто не имеет выраженных клинических признаков. Диагноз устанавливается с опозданием при манифестации сердечно-сосудистых заболеваний, таких как ИБС, инфаркт сердечной мышцы, атеросклероз. Симптомы гиперхолестеринемии наблюдаются менее чем у половины больных. Примерно у трети пациентов формируются сухожильные ксантомы – уплотнения из жироподобного вещества (холестерина), прощупываемые над сухожилиями. Узелки особенно легко определяются на кистях. Холестерин откладывается под кожей век, возле глаз в виде ксантелазм – желтоватых или не имеющих специфического цвета плоских узелков.
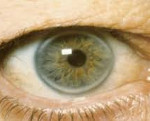
Патогномоничный признак СГСХ – липоидная дуга роговицы. Она представляет собой скопления холестерина по краю роговицы, которые обнаруживаются при офтальмологическом осмотре и выглядят как белый или серо-белый ободок. В отдельных случаях больные отмечают боль и дискомфорт в области груди, водянистые высыпания на коже рук, локтей и коленей. На стадии развития атеросклероза выявляются мозаичные симптомы поражения внутренних органов.
Осложнения
При отсутствии лечения гомозиготная первичная гиперхолестеринемия способствует развитию атеросклероза до 20-летнего возраста, продолжительность жизни больных не превышает 30 лет. Нелеченые пациенты с гетерозиготной формой патологии имеют высокий риск развития ИБС, к 60 годам диагноз подтверждается у 85,5% мужчин и у 53% женщин. Средние показатели продолжительности жизни для мужчин составляют 53 года, для женщин – 62 года. ИБС становится причиной смерти половины мужчин с наследственной гетерозиготной гиперхолестеринемией. Около 20% случаев инфаркта миокарда до 45 лет связаны с наличием СГХС.
Диагностика
Обследованием пациентов занимаются терапевт, кардиолог, врач-генетик. Важным этапом диагностики является сбор личного и семейного анамнеза. Учитывается возраст больного и время начала симптомов, потому что для наследственной патологии характерен ранний дебют. В пользу диагноза семейной гиперхолестеринемии рассматривается наличие двух и более близких родственников (особенно детей) с повышенным холестерином крови, ксантомами и/или липоидными дугами роговиц. Основная задача дифференциальной диагностики – исключение вторичной гиперхолестеринемии. Обследование больных проводится следующими методами:
Лечение семейной гиперхолестеринемии
Терапия включает комплекс мероприятий, нацеленных на снижение количества ЛПНП. Тактика определяется формой гиперхолестеринемии, величиной отклонения показателей липидограммы от нормы, выраженностью симптомов и возрастом пациента. Значительная часть лечебных процедур проводится амбулаторно при регулярном контроле эффективности лечащим врачом. Пациентам назначается:
Прогноз и профилактика
Благоприятное течение семейной гиперхолестеринемии наиболее вероятно при гетерозиготном типе, раннем начале лечения и периодическом контроле уровня холестерина на протяжении всей жизни. Из-за наследственного характера патологии предупредить ее развитие невозможно. Профилактические меры нацелены на раннюю диагностику гиперхолестеринемии, что позволяет сократить вероятность атеросклероза, ИБС, инфаркта мышцы сердца. Для этого проводится каскадный скрининг – исследование уровня липидов крови у всех ближайших родственников пациента.
Гомозиготная форма семейной гиперхолестеринемии
Этиология и встречаемость семейной гиперхолестеринемии. Семейная гиперхолестеринемия (MIM №143890) — аутосомно-доминантное заболевание метаболизма холестерина и липидов, вызываемое мутациями в гене LDLR. Семейная гиперхолестеринемия встречается во всех расах и имеет распространение 1 на 500 в большинстве европеоидных популяций. Это составляет чуть меньше 5% всех пациентов с гиперхолестеринемией.
Патогенез семейной гиперхолестеринемии
Рецептор ЛПНП, трансмембранный гликопротеид, преимущественно экспрессирующийся в печени и коре надпочечников, играет ключевую роль в гомеостазе холестерина. Он связывает аполипопротеин В-100, единственный белок ЛПНП, и АроЕ, белок ЛПОНП, липопротеинов средней плотности, остатков хиломикронов и некоторых ЛПВП. Рецепторы ЛПНП печени захватывают из кровотока приблизительно 50% липопротеинов промежуточной плотности и 66-80% низкой плотности за счет эндоцитоза; остаток захватывается недостаточно изученным путем, не зависящим от рецептора ЛПНП.
Мутации, связываемые с семейной гиперхолестеринемией, наблюдают в гене LDLR; от 2 до 10% таких мутаций — большие инсерции, делеции или перестройки, вызванные рекомбинацией между повторами Alu в пределах гена LDLR. Некоторые мутации — доминантные. Большинство мутаций достаточно редкие, хотя некоторые популяции — например, ливанцы, французские канадцы, южноафриканские индийцы, южноафриканские евреи ашкенази и африканеры (жители ЮАР голландского происхождения) имеют общие мутации и высокое распространение болезни из-за эффекта родоначальника.
Гомозиготные или гетерозиготные мутации в гене LDLR уменьшают эффективность эндоцитоза ЛПНП и липопротеинов средней плотности и вызывают накопление ЛПНП плазмы за счет увеличения их синтеза из липопротеинов средней плотности и уменьшения печеночного захвата. Высокий уровень ЛПНП в плазме вызывает атеросклероз, увеличивая захват ЛПНП через рецептор-независимые пути, например эндоцитоз окисленных ЛПНП макрофагами и гистиоцитами.
Моноциты, проникающие через интиму артерий и захватывающие ЛПНП, образуют пенистые клетки и выбрасывают цитокины, вызывающие пролиферацию гладкомышечных клеток артериальной стенки. Первоначально гладкомышечные клетки производят достаточно коллагена и матричного белка, чтобы сформировать над пенистыми клетками волокнистый колпачок; но, поскольку пенистые клетки продолжают эндоцитоз окисленных ЛПНП, в конечном счете, они прорываются через колпачок в просвет артерии и инициируют образование тромба. Такое образование тромба — основная причина инсультов и инфарктов миокарда.
Окружающая среда, пол и генетический фон модифицируют эффект мутаций рецептора ЛПНП на их уровень в плазме, и тем самым частоту возникновения атеросклероза. Основной средовой модификатор уровня ЛПНП в плазме — диета; в Тунисе большинство гетерозигот по семейной гиперхолестеринемии имеют уровень ЛПНП в диапазоне «нормы» для жителей США и редко страдают сердечно-сосудистыми болезнями и ксантомами.
Аналогично китайские гетерозиготы по семейной гиперхолестеринемии, проживая в Китае, редко имеют ксантомы и сердечно-сосудистую патологию, тогда как китайцы, гетерозиготы по семейной гиперхолестеринемии, проживающие в западных странах, имеют клинические проявления, сходные с гетерозиготами по семейной гиперхолестеринемии европейского происхождения. Пищевой холестерин подавляет синтез рецепторов ЛПНП и тем самым поднимает уровень ЛПНП в плазме; этот эффект усиливается насыщенными жирными кислотами, например пальмитиновой (из молочных продуктов), и ослабляется ненасыщенными жирными кислотой, например олеиновой и линолевой.
Поскольку аналогичная диета неодинаково поднимает уровень ЛПНП среди разных пациентов, на метаболизм ЛПНП также должны влиять и другие средовые и генетические факторы. Некоторые семьи с семейной гиперхолестеринемией передают другой доминантный локус, уменьшающий уровень ЛПНП в плазме, что подтверждает наличие генетического модификатора.
Фенотип и развитие семейной гиперхолестеринемии
Гиперхолестеринемия, самый ранний симптом при семейной гиперхолестеринемии, обычно появляется уже при рождении и остается единственным клиническим симптомом в первом десятилетии жизни у гетерозиготных пациентов; во всех возрастных периодах концентрация холестерина в плазме выше 95-го процентиля у более чем 95% пациентов. «Старческая» дуга роговицы и ксантомы сухожилий начинают появляться к концу второго десятилетия жизни, к моменту смерти уже 80% гетерозигот по семейной гиперхолестеринемии имеют ксантомы. Почти 40% взрослых пациентов имеют рецидивирующие непрогрессирующие полиартриты и тендосиновиты.
Подсчитано, что развитие ИБС среди гетерозигот по семейной гиперхолестеринемии зависит от возраста и пола. Чаще всего при отсутствии лечения концентрация холестерина превышает 300 мг/дл.
Гомозиготная форма семейной гиперхолестеринемии проявляется ксантомами сухожилий и дугой роговицы уже на первом десятилетии жизни. Без энергичного лечения гомозиготная семейная гиперхолестеринемия обычно летальна к возрасту 30 лет. Концентрация холестерина без лечения колеблется между 600 и 1000 мг/дл.
Особенности проявлений семейной гиперхолестеринемии:
• Возраст начала: для гетерозигот — молодость или средний возраст; для гомозигот — детство
• Гиперхолестеринемия
• Атеросклероз
• Ксантомы
• Старческая дуга
Лечение семейной гиперхолестеринемии
Повышение холестерина ЛПНП плазмы крови и наличие в семейном анамнезе гиперхолестеринемии, ксантом или ранней ИБС заставляет предположить диагноз семейной гиперхолестеринемии. Тем не менее подтвердить диагноз трудно, поскольку для этого нужно определить функции рецептора ЛПНП в фибробластах кожи или мутации в гене LDLR. В большинстве популяций большое количество мутаций в гене LDLR затрудняет прямой анализ ДНК, если не подозревается конкретная мутация.
Тем не менее отсутствие ДНК-подтверждения не создает помех для оказания помощи пациентам с семейной гиперхолестеринемией, поскольку окончательный молекулярный диагноз не дает прогностической или терапевтической информации, в основном зависящей от семейного анамнеза и уровня холестерина в плазме.
Независимо от того, семейная это гиперхолестеринемия или нет, все пациенты с повышенным уровнем холестерина ЛПНП требуют энергичных мер по нормализации концентрации для уменьшения риска ИБС. Тщательная нормализация уровня холестерина может предохранить и обратить развитие атеросклероза. Гетерозиготам по семейной гиперхолестеринемии необходимо строжайшее соблюдение высокоуглеводной диеты с резким уменьшением потребления жиров, обычно приводящей к 10-20% снижению уровня холестерина ЛПНП.
Поскольку такого уменьшения обычно недостаточно, пациентам также назначают лечение одним из трех классов лекAPCтвенных средств (или их комбинацией): секвестрантами желчных кислот, статинами (ингибиторы 3-гидрокси-3-метилглутарил КоА редуктазы) и никотиновой кислотой. Текущие рекомендации — начало лекарственной терапии в 10-летнем возрасте у пациентов с концентрацией холестерина ЛПНП выше 190 мг/дл и отрицательным семейным анамнезом по ранней ИБС, и для пациентов с уровнем холестерина ЛПНП выше 160 мг/ дл с положительным семейным анамнезом.
У гомозигот по семейной гиперхолестеринемии уровень холестерина плазмы можно уменьшить до 70% с помощью плазмафереза. Терапевтическая эффективность плазмафереза повышается, если его проводить на фоне энергичной терапии статинами и никотиновой кислотой. В редких случаях проводят пересадку печени.
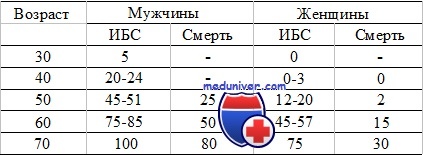
Показатели зависимости ИБС и смерти от возраста и пола (в %) у гетерозигот по семейной гиперхолестеринемии
Риски наследования семейной гиперхолестеринемии
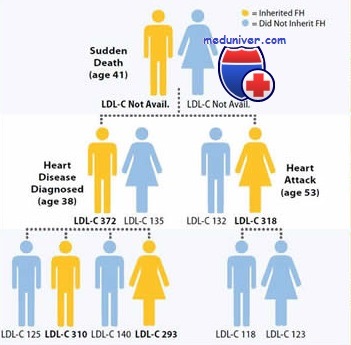
Поскольку семейная гиперхолестеринемия — аутосомно-доминантное заболевание, каждый ребенок больного родителя имеет 50% шанс унаследовать мутантный аллель гена LDLR. Без лечения гетерозиготы по семейной гиперхолестеринемии имеют 100% риск развития ИБС к 70 годам для мужчин и 75% риска для женщин. Постоянное лечение заметно уменьшает этот риск, нормализуя концентрацию холестерина в плазме.
Пример семейной гиперхолестеринемии. У Л.Л., ранее здорового 45-летнего французского канадца, произошел инфаркт миокарда. У него была небольшая ксантома в ахилловом сухожилии справа. У его брата также была ИБС; его мать, бабушка по матери и два дяди по матери умерли от осложнений ИБС. Кроме семейного анамнеза и пола, факторы риска по ИБС и атеросклерозу для Л.Л. включали повышенный уровень ЛПНП, небольшое ожирение, малую физическую активность и курение. На основе семейного анамнеза заподозрена аутосомно-доминантная форма гиперхолестеринемии.
В подтверждение этого подозрения при молекулярном анализе обнаружено, что он гетерозиготен по делеции 5′-конца гена рецептора ЛПНП (LDLR), эту мутацию обнаруживают у 59% французских канадцев с семейной гиперхолестеринемией. Обследование детей Л.Л. показало, что у двоих из трех детей уровень ЛПНП повышен.
Кардиолог сказал Л.Л., что дополнительно к лекарственной терапии эффективное лечение его ИБС требует изменения диеты и образа жизни, т.е. снижения в рационе питания насыщенных жиров и холестерина, повышения физической активности, снижения массы тела и прекращения курения. Больной не последовал этим рекомендациям и умер годом позже от повторного инфаркта.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Дислипопротеидемии
Липидный обмен является одним из сложнейших обменов организма человека. Значение липидов в организме велико: они составляют основу центральной нервной системы, образуют липидную матрицу клеточных мембран и органелл клеток, играют большую роль в энергетич
Липидный обмен является одним из сложнейших обменов организма человека. Значение липидов в организме велико: они составляют основу центральной нервной системы, образуют липидную матрицу клеточных мембран и органелл клеток, играют большую роль в энергетическом обмене. Некоторые липиды представляют собой сложные ферментные комплексы, принимающие участие в иммунологических реакциях, процессах пищеварения, свертывании крови.
Еще совсем недавно считалось, что нарушения обмена липидов являются редкостью, теперь же мы знаем, что в индустриальных странах с избыточным питанием это наиболее распространенный фактор заболеваний обмена веществ.
Классификация гиперлипопротеидемий, составленная ВОЗ на основе классификации Фредриксона, описывает весь спектр липопротеидов при наиболее распространенных гиперлипидемиях, однако она не разделяет причины нарушений на генетически предопределенные и вторичные — в ответ на факторы окружающей среды или основное заболевание (табл. 1).
Таблица 1. Классификация гиперлипопротеидемий
Гепатомегалия
Липемическая ретинопатия
Ксантомы
Ранний атеросклероз
Ксантелазмы
Ранний атеросклероз
Распространенный атеросклероз
Ксантомы
Атеросклероз сосудов
Панкреонекрозы
Ожирение
Ксантомы
I тип гиперлипопротеидемии — гиперхиломикронемия (экзогенная гиперлипемия; эссенциальная, индуцированная жирами гипертриглицеридемия; болезнь Бюргера-Грюцше) — выражается в гипертриглицеридемии при избытке хиломикронов и развивается при недостаточности липопротеинлипазы, обусловленной наследственным дефицитом липопротеинлипазы, дефицитом апопротеина С II. Ферментная недостаточность приводит к неполному расщеплению хиломикронов и их накоплению в кровотоке.
Заболевание встречается очень редко, проявляется уже в детстве. Ведущими клиническими симптомами являются спленомегалия и рецидивирующие боли в животе, напоминающие острый панкреатит, эруптивные ксантомы, липемия в сосудах сетчатки. Уровень триглицеридов в плазме повышается до 50-100 ммоль/л. После ограничения пищевых жиров в течение 10-14 дней происходит прогрессирующая нормализация лабораторных параметров и состояния. Диагноз обоснован, если активность липопротеидлипазы составляет менее 10% его нормального содержания. Дифференциальный диагноз проводится с гиперлипидемией V типа. Прогноз в общем благоприятный, если не считать предрасположения к панкреатиту. Основное направление лечения — снижение образования хиломикронов за счет ограничения потребления жиров.
II тип гиперлипопротеидемии — семейная гиперхолестеринемия (множественная бугорчатая ксантома) — подразделяется на два подтипа: IIа, IIб. При IIа типе повышается уровень ХС ЛПНП, а при IIб типе картина дополняется умеренной формой гипертриглицеридемии за счет возрастания ЛПОНП. Наиболее тяжелой формой является гомозиготная гиперхолестеринемия (частота составляет 1:1 000 000), при этом уровень холестерина плазмы достигает 12-25 ммоль/л. При гетерозиготной форме, частота которой 1:500, уровень холестерина колеблется в пределах 6-13 ммоль/л. При гомозиготной форме отсутствуют, а при гетерозиготной снижено число рецепторов для ЛПНП. В норме ЛПНП связываются с рецепторами, поглощаются клетками, включаются в лизосомы, где белки разрушаются, а высвободившийся холестерин подавляет активность основного фермента синтеза холестерина (ГМГ-КоА-редуктазы). При дефиците рецепторов активность этого фермента не подавляется, что ведет к повышенному синтезу холестерина.
| Гиперлипидемии представляют собой заболевания, при которых в результате нарушения синтеза, транспорта и расщепления липопротеидов повышается уровень холестерина и/или триглицеридов в плазме крови. Поскольку липиды крови вследствие их нерастворимости в воде транспортируются только в виде комплексов с белками, то правильнее употреблять термин «гиперлипопротеидемия» |
Клинические признаки заболевания проявляются на втором — третьем — четвертом десятилетии жизни и зависят от уровня холестерина в плазме. Наиболее типичными клиническими проявлениями являются кожные ксантомы, которые обычно расположены на коже разгибательных поверхностей суставов, в области ягодиц, шеи, подбородка. Часто встречаются сухожильные ксантомы. Преимущественная локализация их на ахилловом сухожилии, сухожилиях разгибателей ладоней и стоп. Офтальмологические изменения характеризуются роговичными липемическими дугами, периорбитальными ксантелазмами.
Изменения со стороны сердечно-сосудистой системы определяются развитием коронарного атеросклероза: появляются боли стенокардитического характера. По данным ЭхоКГ обнаруживается стеноз аорты, утолщение створок аортальных клапанов. Ангиография выявляет неравномерное сужение и воронкообразную деформацию проксимальной части венечных артерий. Прогрессирование атеросклеротического процесса способствует развитию инфаркта миокарда. Прогноз при данной форме гиперлипидемии зависит от степени поражения сосудистого русла атеросклеротическим процессом. Лечение, как правило, включает комбинированную лекарственную терапию на фоне диеты.
При III типе гиперлипопротеидемии накопление ремнантов хиломикронов и ЛППП приводит к увеличению содержания холестерина и триглицеридов. Нарушения липидного обмена при этом типе гиперлипидемии обусловлены наследственным дефектом апопротеина Е, который обычно сочетается с ожирением, сахарным диабетом, гипотиреозом. Частота встречаемости III типа гиперлипопротеидемии 1:5000. Клинические проявления замечены после 20 лет. Отличительной особенностью является высокая степень поражения атеросклеротическим процессом всего сосудистого русла. Наряду с симптоматикой ишемической болезни сердца имеются признаки поражения периферических сосудов, нередко с явлениями перемежающейся хромоты, напоминающие симптомы облитерирующего эндартериита. Характерно наличие кожных ксантом желтого или оранжевого цвета с локализацией на ладонях, в области локтей, коленей, ягодиц и реже на сухожилиях. Часто у больных встречается нарушение толерантности к углеводам: нагрузка углеводами приводит к резкому возрастанию уровня триглицеридов в плазме. Лечение сводится к устранению любых причин, отягощающих заболевание (гипотиреоз, диабет, ожирение), назначению гиполипемических препаратов.
Повышение содержания триглицеридов в сыворотке крови, взятой у пациентов с IV типом гиперлипидемии, обусловлено накоплением ЛПОНП, часто сопровождающимся умеренной гиперхолестеринемией при нормальной ХС ЛПНП. Частота встречаемости этого заболевания в популяции 0,2 — 0,3%. Клинические проявления комбинированной семейной гипертриглицеридемии обычно наблюдаются у взрослых и характеризуются атеросклеротическим поражением коронарных и периферических сосудов. Возможно развитие панкреатита, проявляющегося приступами абдоминальных болей и диспептическими явлениями. Для больных гипертриглицеридемией типична особенность жировой прослойки лица и области шеи — так называемое «лицо Луи-Филиппа». Кожные проявления — ксантомы — встречаются нечасто. У большинства пациентов имеется нарушение толерантности к глюкозе. Основные направления лечения сводятся к соблюдению модифицированной жировой диеты, направленной на нормализацию веса тела, ограничению сахара и избытка алкоголя, поощрению физической активности. При неэффективности может потребоваться лекарственная терапия.
Причиной выраженной триглицеридемии при V типе гиперлипопротеидемии является избыток и хиломикронов, и ЛПОНП. В отличие от гиперлипопротеидемии I типа данное нарушение редко проявляется в детстве. Клинические проявления семейной гипертриглицеридемии мало отличаются от клиники гиперлипопротеидемий IV типа. Также заболевание проявляется на втором — третьем десятилетии жизни ожирением, появлением эруптивных ксантом. На переднем плане стоит более выраженный абдоминальный синдром, сопровождающий тяжелое течение панкреатита, вплоть до развития панкреонекроза. При этом типе гиперлипопротеидемии снижена толерантность как к жирам, так и к углеводам.
Гиперлипопротеидемия V типа является вторичным фактором риска развития атеросклероза за счет накопления ЛПОНП.
Каждый из фенотипов гиперлипопротеидемий может быть как первичным, так и вторичным. Среди вторичных причин гиперлипопротеидемии чаще всего встречаются диабет, гипотиреоз, воспалительные заболевания почек, ожирение (табл. 2).
Таблица 2. Этиология фенотипов гиперлипоротеидемий
Упомянутые пять типов гиперлипопротеидемий не исчерпывают всего разнообразия нарушений липидного обмена. Прежде всего это касается такой довольно частой формы нарушений, для которой характерно снижение ХС ЛПВП. При этом гиперлипопротеидемия как таковая отсутствует, может даже наблюдаться снижение уровня общего холестерина, однако в липидном составе крови может определяться атерогенный сдвиг. Для характеристики атерогенной направленности липидного спектра рассчитывают индекс атерогенности, который равен отношению содержания ХС в ЛПНП и ЛПОНП к его содержанию в ЛПВП. В норме он не должен превышать 4,0 (у детей — 2,0). Таким образом, термин гиперлипопротеидемия не является всеохватывающим для характеристики сдвигов в липидном составе, поэтому более правильно пользоваться термином дислипидемия (дислипопротеидемия).
Многообразие типов дислипопротеидемий и их клинических проявлений указывает на то, что нарушение липидного гомеостаза может происходить на любом уровне, следовательно, не может быть стандартного подхода к лечению этой категории больных. Необходимо индивидуализировать коррекцию дислипопротеидемии в зависимости от типа нарушения липидного обмена, клинического варианта течения. Цель лечения — свести к минимуму риск развития атеросклероза сосудов, ишемической болезни сердца и панкреатита.
Лечение гиперлипидемий всегда начинается с диеты. Основными принципами гиполипидемической диеты являются: снижение веса при его избытке; общая калорийность диеты обеспечивается на 55% углеводами, 10-15% белками и до 30% жирами, включая по 10% насыщенных, мононенасыщенных и полиненасыщенных жирных кислот, холестерина менее 300 мг/день и 35 мг/день клетчатки, получаемой в основном в виде бобовых, а также других овощей и фруктов. Если стандартная диета неэффективна, то потребление жира следует снижать до 20-25%, а холестерина до 150 мг/день и меньше.
Некоторые пациенты с гиперлипидемией не реагируют должным образом на диету и коррекцию других причинных факторов. В таких случаях требуется медикаментозное лечение, но с обязательным продолжением соблюдения диеты. Фармакотерапия дислипопротеидемии достаточно сложна и многообразна. По принципу действия все гиполипидемические препараты могут быть разделены на следующие основные группы.
При неэффективности консервативной терапии пациентам с высокой гиперхолестеринемией показаны хирургические методы коррекции дислипопротеидемии, в частности ЛПНП-аферез через колонки с моно- и поликлональными антителами к ЛПНП и каскадную плазмофильтрацию через колонки с гепарином. В рекомендациях ВОЗ по лечению дислипопротеидемии выделяются пять групп наблюдения.
Группа А включает лиц с умеренной гиперхолестеринемией: содержание холестерина в сыворотке крови 200 — 250 мг/дл (5,2 — 6,5 ммоль/л), триглицеридов менее 200 мг/дл ( 7,8 ммоль/л), и/или триглицеридов выше 500 мг/дл (>5,6 ммоль/л). Пациенты с уровнем холестерина более 300 мг/дл (>7,8 ммоль/л) и с нормальным содержанием триглицеридов обычно имеют семейную гиперхолестеринемию и особенно высокий риск ИБС. Терапия обычно включает диету и одно или два гиполипидемических лекарства: секвестранты желчных кислот в сочетании с одним из фибратов (или ингибиторов синтеза холестерина) либо с никотиновой кислотой. Для хиломикронемии не существует подходящей медикаментозной терапии, она лечится диетой с низким содержанием жиров. Ремнантная гиперлипидемия (тип III) обычно проявляется в виде значительного повышения как холестерина, так и триглицеридов. Она очень часто связана с коронарным и периферическим атеросклерозом, в большинстве случаев требуется лечение диетой и лекарствами, обычно фибратами. Семейная гипертриглицеридемия, подобно хиломикронемии, может привести к острому панкреатиту. Она часто сопровождается диабетом. В лечении необходимы: контроль массы тела, диета, в тяжелых случаях — фибраты или никотиновая кислота.
Одним из важнейших аспектов медицины является профилактика. Правильнее начинать ее в с раннем возрасте, когда еще нет никаких признаков дислипопротеидемии. Такая профилактика получила название первичной, в отличие от вторичной, при которой превентивные мероприятия проводятся при уже имеющихся признаках атеросклероза. Цель первичной профилактики — не допустить развития заболевания, вторичная направлена на стабилизацию состояния и предотвращение серьезных осложнений. Основу профилактических мероприятий составляет работа по формированию здорового образа жизни, отказу от курения, неумеренного потребления алкоголя, внедрению принципов рациональной диеты. Немаловажное значение имеет борьба с избыточным весом, сидячим образом жизни. Решающую роль отводят мерам по нормализации артериального давления, уровню сахара и содержанию липидных фракций крови. Первичная профилактика гиперлипопротеидемий и связанных с ними заболеваний проводится среди детей, родители которых имеют нарушения липидного обмена, ранние признаки коронарного атеросклероза. Массовые профилактические мероприятия должны и могут принести большую пользу в тех случаях, когда осуществляются в детском и юношеском возрасте.
Как определить фенотип гиперлипопротеидемии?
Для определения фенотипа гиперлипопротеидемии необходимо знать концентрации триглицеридов, общего холестерина и холестерина липопротеидов низкой плотности (ЛПНП). Кроме того, необходимо оценить присутствие хиломикрон или липопротеидов очень низкой плотности (ЛПОНП). Так как уровни липидов в плазме имеют значительные биологические вариации в разные дни, диагностика повышенного уровня липидов должна основываться на двух анализах, взятых с интервалом две — три недели. Для измерения уровня общего холестерина и холестерина липопротеидов высокой плотности (ЛПВП) нет необходимости в предварительном голодании. Триглицериды, как правило, измеряются в образцах плазмы или сыворотки через 12 часов после последнего приема пищи, обычно утром; разрешается прием воды или других жидкостей, не содержащих жиры. Исследования должны проводиться не ранее чем через три — четыре недели после серьезной операции, перенесенного инфаркта миокарда. В большинстве лабораторий уровень холестерина, входящий в состав ЛПНП, рассчитывается исходя из уровня общего холестерина, триглицеридов и ХС ЛПВП. Этот расчет обычно проводится по формуле Фридвальда:
ХС ЛПНП (мг/дл) = ОХ — триглицериды/5 — ХС ЛПВП
ХС ЛПНП (ммоль/л) = ОХ — триглицериды/2,2 — ХСЛПВП
Эта формула справедлива при значениях триглицеридов 7,8 ммоль/л ( >300 мг/дл) — выраженной гиперхолестеринемией. Уровень триглицеридов выше 2,0 ммоль/л для мужчин и 1,5 ммоль/л для женщин требует проведения коррекции. Риск развития атеросклероза сосудов увеличивается при показателе ХС ЛПНП >4,2 ммоль/л (164 мг/дл), ХС ЛПВП