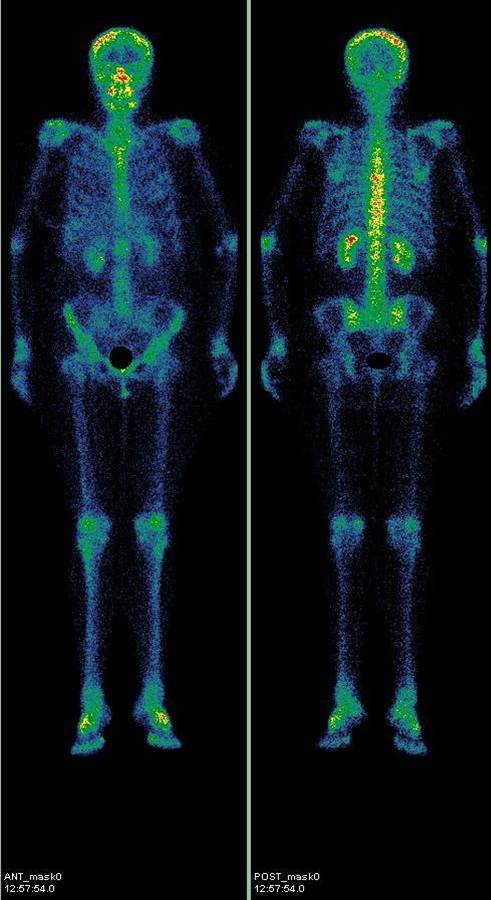
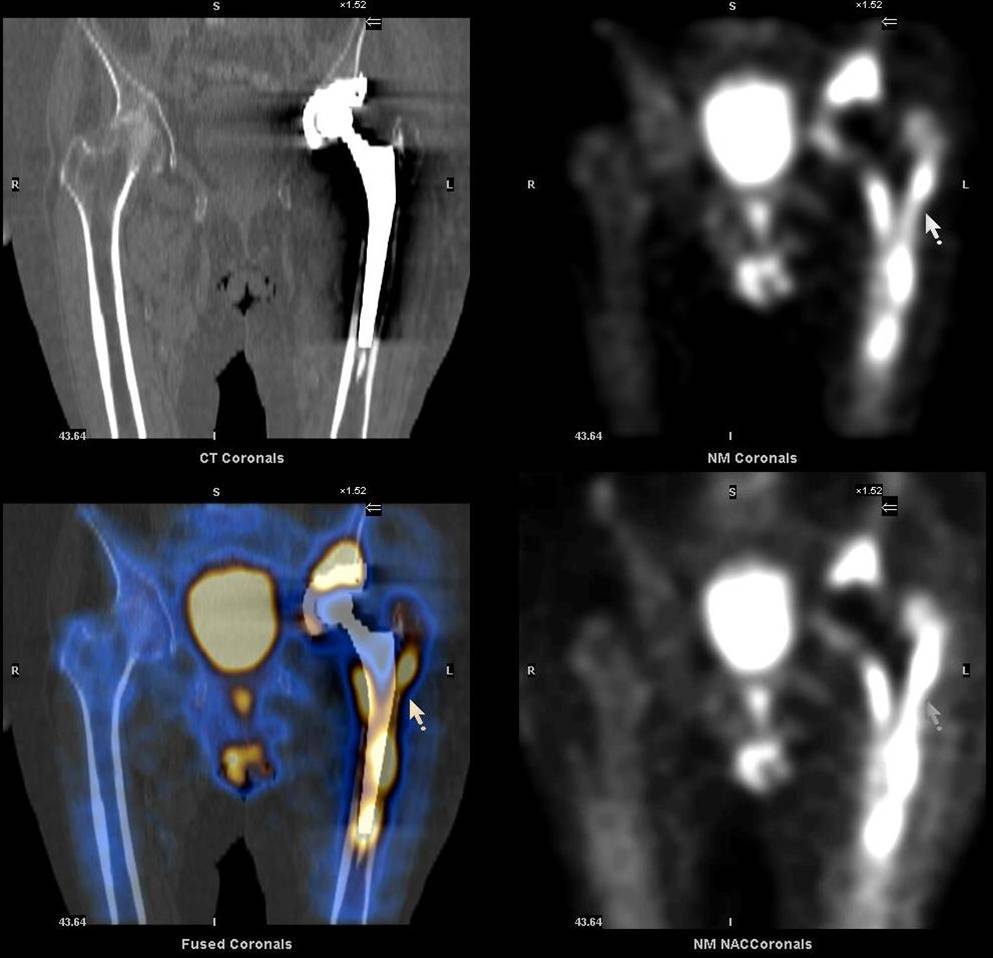
Суперскан при сцинтиграфии что это
Радионуклидная диагностика состояния скелета
Виды исследований: Остеосцинтиграфия планарная, ОФЭКТ-КТ скелета.
Цель: Визуализация патологических изменений в склете (очагов патологического метаболизма костной ткани).
Показания:
РФП: Меченные Tc99m фосфатные комплексы. Меченные Tc99m бисфосфонаты. Механизм визуализации метастатических очагов связан с включением РФП в минеральный обмен костной ткани и активным накоплением в участках повышенного костеобразования (минерализации), сопровождающих костную деструкцию.
Методика: После внутривенного введения РФП через 2-3 часа проводят сканирование скелета в режиме «все-тело».
Подготовка: Специальная подготовка не требуется. После инъекции РФП пациент должен выпить около 1 литра жидкости. Исследование выполняют после опорожнения мочевого пузыря.
Особенности: Остеосцинтиграфия является высокочувствительным, но низкоспецифичным методом диагностики. В некоторых случаях остеохондроз, артроз и травматические изменения в скелете могут приводить к ошибочным заключениям. В этой ситуации рекомендовано проведение исследования в режиме ОФЭКТ-КТ. Применение меченных Tc99m бисфосфонатов повышает чувствительность метода.
ОФЭКТ-КТ скелета способствует более точному определению состояния скелета при неясных результатах остеосцинтиграфии. Позволяет выявить метастазы размерами 5-10мм. Является надежным способом оценки эффективности лечения метастазов химиопрепаратами и бисфосфонтами. Рекомендовано выполнять ОФЭКТ-КТ у больных первичным раком предстательной и молочной желез, раком почки и мочевого пузыря, раком легкого (при отсутствии ПЭТ-КТ), меланомой, гистиоцитозом, злокачественными новообразованиями органов ЖКТ и репродуктивной системы, эмбриональными опухолями, остеосаркомой.
Радиоизотопные методы
Изотопные методы в диагностике рака предстательной железы.
I. Введение.
Рак простаты (РП) остается одним из самых распространенных новообразований у мужчин после 50 лет.
Надо заметить, что в большинстве случаев РП — медленно растущие опухоли, которые находят только на аутопсии, и которые никак себя не проявляли клинически при жизни, и не являлись непосредственной причиной смерти. С другой стороны, в некоторых случаях РП может вести себя весьма агрессивно, быстро прогрессировать, метастазируя в мягкие ткани и кости. Чаще всего РП метастазирует в тазовые лимфоузлы, окружающие предстательную железу мягкие ткани и органы (парапростатическая клетчатка, семенные пузырьки, мочевой пузырь) и кости скелета (кости таза, позвоночник, ребра). РП находится на втором месте по причинам смерти от онкологических заболеваний у мужчин, уступая только раку легких.
В настоящее время принят скрининг РП (ранняя диагностика у практически здоровых мужчин) с помощью простатоспецифического антигена ПСА и пальцевого ректального исследования. Цель скрининга — обнаружения РП на ранней, излечимой стадии. Современные методики многоточечной биопсии простаты позволяют обнаружить очень маленькие и даже фактические не опасные для здоровья (клинически не значимые) опухоли. Однако, к сожалению, по прежнему нет достаточно четких критериев, позволяющих определить будущее поведение обнаруженной опухоли, ее прогноз с точки зрения влияния на продолжительность жизни больного. Хотя различные системы критериев предлагаются и используются, ни одна из них не совершенна.
II. Обнаружение метастазов рака предстательной железы в костях скелета и радиоизотопное сканирование.
У пациентов с диагностированным раком простаты, имеющим низкий ПСА ( ng / mL ) и низкий балл по шкале Gleason редко обнаруживаются костные метастазы.
Сцинтиграфия или радиоизотопное сканирование скелета на 50㫨% чувствительнее рентгенографии для поиска костных метастазов. Это объясняется тем, что для того чтобы метастатический очаг был виден на рентгенограмме, кость в этом очаге должна потерять около 50% неорганического состава. Однако специфичность сцинтиграфии лимитирована. Костные переломы, дегенеративные изменения и многие другие доброкачественные изменения костной структуры могут давать при сцинтиграфии ложноположительные результаты. Тем не менее, возможность исследования всего скелета в течение одной процедуры делает сканирование процедурой первого выбора при поиске костных метастазов у пациентов с РП.
Как же интерпретируются радиоизотопные исследования костного скелета?
В интерпретации сцинтиграфии большое значение имеет распределение и локализация очагов. При наличии метастатического поражения скелета, очаги накопления как правило множественные (примерно в 90% случаев). Около 80% всех метастатических повреждений расположено в аксиальном скелете (кости черепа, позвоночник, ребра, кости таза). У пациентов с диагностированным онкологическим заболеванием очаги, обнаруженные в центральном скелете (позвоночник, ребра, кости таза) в 60㫞% являются метастатическими. В то время как очаги, обнаруженные в аппендикулярном скелете (кости рук и ног) или черепе будут метастазами только в 40㫊% случаев. Одиночное повреждение ребра оказывается метастазом в 10% случаев. При оценке очагов в позвоночнике большое значение имеет расположение повреждений. Очаги, выходящие за пределы позвонка, как правило, представляют собой остеофиты. Захват метки на поверхности сустава практически всегда представляет собой доброкачественные изменения. Захват метки в теле позвонка и отростках позвонков обычно представляет собой метастатическое повреждение.
Важно отличать так называемый » Flare phenomenon» — увеличение интенсивности захвата радиометки и числа очагов после лечения, отражающее желаемый результат лечения — заживление метастатичеких повреждений. Пациенты при этом, как правило, не имеют симптомов, и в области захвата на рентгенограмме определяются склеротические очаги. » Flare phenomenon» обычно определяется от 2-х недель до 3-х месяцев после терапии, и практически никогда после 6 месяцев. Увеличение числа и интенсивности очагов захвата на сцинтиграмме после 6 месяцев, прошедших от момента последнего курса лечения, как правило, говорит о прогрессировании болезни. Поэтому имеет смысл делать контрольную сцинтиграфию не ранее 3 месяцев после завершения лечения.
Сцинтиграфия скелета является одним из исследований выбора при рецидиве рака простаты после радикальных методов лечения (радикальная простатэктомия, лучевая терапия), определяемым повышением ПСА.
III. Обнаружение метастатических очагов РП в мягких тканях.
Данная диагностическая задача у пациентов с рецидивом РП часто бывает достаточно сложна.Компьютерная томография и МРТ имеют достаточно лимитированную чувствительность для поиска метастазов в лимфатических узлах.
Позитронно-эмиссионная сцинтиграфия (ПЭТ),возможно, сможет играть роль в поиске метастатических очагов у таких пациентов. ПЭТ — радиоизотопное исследование, проводимое с помощью короткоживущих изотопов, при радиоактивном распаде которых выделяются позитроны. Позитрон проходит в ткани весьма небольшое расстояние (около 2мм) и затем подвергается аннигиляции с излучением двух гамма лучей с одинаковой энергией (511 keV ) направленных под углом 180 градусов. Действие ПЭТ камеры основано на определении этих противоположно направленных гамма-лучей. Одной из наиболее часто используемых радиометок в ПЭТ исследованиях является ФДГ (Ф18 флюородеоксиглюкоза), которая, как и обычная глюкоза, накапливается в тканях с повышенной метаболической активностью. Однако, по имеющимся на настоящее время данным, чувствительность ФДГ ПЭТ для определения метастазов РП невелика и составляет по разным источникам от 18 до 65%. Более высокую метаболическую активность и соответственно выявляемость на ФДГ ПЭТ исследовании имеют опухоли с высоким баллом по шкале злокачественности Gleason и высоким уровнем ПСА. Возможно, ФДГ ПЭТ можно использовать при оценке эффективности лечения, сравнивая метаболическую активность и размер метаболически активного очага до и после лечения. ФДГ ПЭТ не показан для первичной диагностики РП из-за его, как правило, низкой метаболической активности, неспецифичности теста для дифференциальной диагностики доброкачественных заболеваний простаты. Чувствительность ФДГ ПЭТ для диагностики костных метастазов составляет около 50%. В отличие от сцинтиграфии скелета, ПЭТ обладает большей чувствительностью в обнаружении остеолитических метастазов, и менее чувствителен в отношении склеротических.
C 11- acetate and C 11- choline изучаются как альтернативные ПЭТ метки для обследования пациентов с РП. Но данных за широкое внедрение таких обследований пока недостаточно. Кроме того, короткое время полураспада требует наличие циклотрона в том же учреждении, где проводится обследование. В то время как ФДГ для ПЭТ может транспортироваться от места продукции метки к месту обследования пациента.
IV. Диагностика рецидивов РП после радикальных методов лечения ранних стадий заболевания.
Показания для Prostascint сцинтиграфии:
Выявление метастазов у таких пациентов будет противопоказанием к радикальному лечению и показанием к паллиативному лечению. Иссечение лимфатических узлов таза, хотя и является наиболее точным методом выявления метастазов у этих пациентов все же дает ложнонегативные результаты в 12% случаев. Кроме того, пациенты могут иметь метастазы в лимфатических узлах брюшной полости при отсутствии метастазов в лимфатических узлах таза (» skip » metastases ). КТ и МРТ, к сожалению, имеют очень низкую чувствительность в обнаружении метастатичских очагов у этих пациентов (4 — 45%). Чувствительность сканирования с ProstaScint в группе среднего и высокого риска составляет 62%, специфичность — 72%.
2)Рецидив опухоли простаты у пациентов после простатэктомии/радиационной терапии, подозреваемый на основании повышения ПСА. Выявление рецидива позволяет своевременно и правильно спланировать наиболее эффективное лечение.
В последние годы радиоизотопные методы исследования заняли достойное место в диагностике и определении стадии РП. Их применение позволяет осуществлять лечение в строгом соответствии с распространенностью опухолевого процесса (стадией заболевания), что дает наилучший результат при минимальных побочных эффектах и осложнениях.
Клинико-морфологические и лабораторные предикторы сцинтиграфического феномена «superscan» при раке предстательной железы
Полный текст:
Аннотация
Введение. Диагностика метастатического поражения скелета при различных видах злокачественных новообразований имеет важнейшее значение в выборе тактики лечения и оценке прогноза заболевания. В статье рассматривается сцинтиграфический феномен «superscan» при диагностике вторичного опухолевого поражения скелета у больных раком предстательной железы (РПЖ). При анализе литературных источников нами найдено лишь одно крупное проспективное исследование и немногочисленные описания клинических случаев диагностики «superscan» при генерализованном поражении скелета.
Материал и методы. В исследование включены 48 пациентов с феноменом «superscan», выявленным при радионуклидном обследовании 2 474 больных РПЖ. В качестве клинико-лабораторных и морфологических параметров у больных РПЖ, включенных в исследование, оценивались: возраст, стадия заболевания по TNM (7-е издание, 2010), гистологический тип опухоли, индекс Глисона, уровень простатического специфического антигена (ПСА), болевой синдром (по 5-балльной вербальной шкале оценок боли, 1982), наличие кастрационно-резистентного рака предстательной железы, уровень гемоглобина и скорость оседания эритроцитов (СОЭ).
Заключение. Наиболее значимыми факторами, ассоциированными со сцинтиграфическим феноменом «superscan» у больных РПЖ, явились распространенность первичной опухоли, высокий уровень ПСА и низкая степень дифференцировки опухоли. Получены новые данные о сопряженности феномена с уровнем гемоглобина и СОЭ, требуют дальнейшего изучения взаимосвязь с болевым синдромом и развитием кастрационной резистентности.
Ключевые слова
Об авторах
660133, Красноярск, ул. 1-ая Смоленская; 660022, Красноярск, ул. Партизана Железняка, 12
660022, Красноярск, ул. Партизана Железняка, 12
660022, Красноярск, ул. Партизана Железняка, 12; 660022 Красноярск, ул. Партизана Железняка, 3А
660133, Красноярск, ул. 1-ая Смоленская
660133, Красноярск, ул. 1-ая Смоленская, 16/113
660133, Красноярск, ул. 1-ая Смоленская; 660022, Красноярск, ул. Партизана Железняка, 12
Список литературы
1. Каприн А.Д., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2017 году (заболеваемость и смертность). М., 2018. 250 с.
2. ГлушковЕ.А., Кисличенко А.Г., РамазановаМ.С. Эффективность ОФЭКТ/КТ в обнаружении костных метастазов при раке молочной железы и простаты. Сибирский онкологический журнал. 2015; (6): 19-25.
3. Лишманов Ю.В., Чернов В.И. Национальное руководство по радионуклидной диагностике. Томск, STT. 2010. 418 с. [Lishmanov Y.B., Chernov VI. National guide on radionuclide diagnostics. Tomsk, STT. 2010. 418 p. (in Russian)]
4. Manohar P.R., Rather T.A., Khan S.H., MalikD. Skeletal Metastases Presenting as Superscan on Technetium 99m Methylene Diphosphonate Whole Body Bone Scintigraphy in Different Type of Cancers: A 5-Year Retro-prospective Study. World J Nucl Med. 2017; 16 (1): 39-44. doi: 10.4103/1450-1147.181153.
5. Bailly M., Besse H., KerdraonR., Metrard G., Gauvain S. 18F-FDG PET/CT superscan in prostate cancer. Clin Nucl Med. 2014 Oct; 39 (10): 912-4. doi: 10.1097/RLU.0000000000000376.
6. Lawal I., Vorster M., Boshomane T., Ololade K., Ebenhan T., Sathekge M. Metastatic Prostate Carcinoma Presenting as a Superscan on 68Ga-PSMA PET/CT. Clin Nucl Med. 2015 Sep; 40 (9): 755-6. doi: 10.1097/RLU.0000000000000870.
7. Liu Y. Super-superscan on a bone scintigraphy. Clin Nucl Med. 2011 Mar; 36 (3): 227-8. doi:10.1097/RLU.0b013e318208f503.
8. Alam M.S., Fu L., Ren Y.Y., Wu H.B., Wang Q.S., Han Y.J., Zhou W.L., LiH.S., Wang Z. 18F-FDG super bone marrow uptake: a highly potent indicator for the malignant infiltration. Medicine (Baltimore) 2016 Dec; 95 (52): e5579. doi: 10.1097/MD.0000000000005579.
9. Shikino K., Ikusaka M., Hirota Y., Sato E. Super bone scan: bone metastases of prostate cancer. BMJ Case Rep. 2014 Sep 16; 2014. pii: bcr2014206886. doi: 10.1136/bcr-2014-206886.
10. PounceyA.L., Fox T.P., Bryant C.A. Unilateral proptosis: an unusual case presentation of prostatic carcinoma. BMJ Case Rep. 2013 May 27; 2013. pii: bcr2013009904. doi: 10.1136/bcr-2013-009904.
11. Rajkumar D., Singh J.C., Devasia A. Superscan in carcinoma prostate. Indian J Surg. 2008 Feb; 70 (1): 44-45. doi: 10.1007/s12262-008-0012-1.
12. GrossmanM., Zajac J.D. Hematological changes during androgen deprivation therapy. Asian J Androl. 2012 Mar; 14 (2): 187-192. doi: 10.1038/aja.2011.102.
13. Betsch D.M., Gray S., Zed S.E. A case of metastatic prostate cancer and immune thrombocytopenia. Curr Oncol. 2017 Oct; 24 (5): e434e436. doi: 10.3747/co.24.3592.
14. Drudge-CoatesL., Oh W.K., TombalB., Delacruz A., TomlinsonB., Ripley A. V, Mastris K., O’Sullivan JM., Shore N.D. Recognizing Symptom Burden in Advanced Prostate Cancer: A Global Patient and Caregiver Survey. Clin Genitourin Cancer. 2018 Apr; 16 (2): e411e419. doi: 10.1016/j.clgc.2017.09.015.
15. KucukzeybekB. B., Calli A.O., Kucukzeybek Y., Bener S., Dere Y., Dirican A., Payzin K. B., Ozdemirkiran F., Tarhan M. O. The prognostic significance of bone marrow metastases: evaluation of 58 cases. Indian J Pathol Microbiol. 2014 Jul-Sep; 57 (3): 396-9. doi: 10.4130/0377-4929.138728.
16. Nieder C., Haukland E., Pawinski A., Dalhaug A. Anaemia and thrombocytopenia in patients with prostate cancer and bone metastases. BMC Cancer. 2010 Jun 13; 10: 284. doi: 10.1186/1471-2407-10-284.
17. MangaonkarA. A., GuptaH. R., BeraB. M., Barmare S. Bone marrow fibrosis and metastatic prostate adenocarcinoma. BMJ Case Rep. 2013 May 27; 2013. pii: bcr2013009904. doi: 10.1136/bcr-2013-009904.
18. МарковаА.С., МатвеевВ.Б., НазрановБМ. Последовательная терапия метастатического кастрационно-резистентного рака предстательной железы: новые возможности. Онкоурология. 2018; 14(3): 120-127. doi: 10.17650/1726-9776-2018-14-3-120-127.
19. Алексеев Б.Я., Каприн А.Д., Колонтарев К.Б., Матвеев В.Б., Пушкарь Д.Ю., РаснерП.И., Харчилава Р.Р. Клинические рекомендации: рак предстательной железы. Москва, 2018. 71 с.
20. Гафанов РА., Дзидзария А.Г., Кравцов И.Б., Фастовец С.В. Метастатический гормоночувствительный рак предстательной железы: практические рекомендации и оптимизация выбора терапии. Онкоурология 2018; 14(4): 139-149. doi: 10.17650/1726-9776-2018-14-4-139-149.
21. NCCN. Clinical Practice Guidelines in Oncology (NCCN Guidelines). Prostate Cancer [Internet]. URL: https://www.nccn.org/profession-als/physician_gls/pdf/prostate.pdf (cited 30.04.2019).
Для цитирования:
Шумилина Н.Ю., Вязьмин В.В., Евдокимова Е.Ю., Дашанов Д.О., Чанчикова Н.Г., Зуков Р.А. Клинико-морфологические и лабораторные предикторы сцинтиграфического феномена «superscan» при раке предстательной железы. Сибирский онкологический журнал. 2020;19(2):17-24. https://doi.org/10.21294/1814-4861-2020-19-2-17-24
For citation:
Shumilina N.Yu., Vyazmin V.V., Evdokimova E.Yu., Dashanov D.O., Chanchikova N.G., Zukov R.A. Clinical-morphological and laboratory predictors of «superscan» scintigraphy phenomenon in prostate cancer. Siberian journal of oncology. 2020;19(2):17-24. (In Russ.) https://doi.org/10.21294/1814-4861-2020-19-2-17-24
Сцинтиграфия костей скелета (остеосцинтиграфия)
Наши специалисты свяжутся с вами в ближайшее время
Сцинтиграфия костей скелета (остеосцинтиграфия) – это исследование метаболизма (обмена веществ) костной ткани с помощью радиофармацевтических препаратов (РФП), которые накапливаются в костях скелета. Радиофармпрепарат вводится внутривенно и накапливается в костной ткани, затем излучение от накопившегося препарата улавливается детекторами регистрирующего прибора (гамма-камеры).
Что показывает?
С помощью сцинтиграфического обследования, в основе которого лежит лучевая диагностика, врачи выявляют различные патологии, недоступные другим диагностическим методам, в том числе на ранних стадиях развития:
Если речь идет сцинтиграфии при онкологии, важно понимать, что данный метод позволяет выявлять динамику лечения, а значит, подтверждает его эффективность или свидетельствует о необходимости смены назначений.
Подготовка к сцинтиграфии костей скелета: не требуется.
В течение часа после введения РФП Вас попросят выпить 1 литра питьевой воды, так как это необходимо для улучшения накопления препарата в костях скелета и снижения лучевой нагрузки. Непосредственно перед исследованием необходимо опорожнить мочевой пузырь.
Показания к проведению сцинтиграфии костей скелета:
Противопоказания:
беременность. Грудное вскармливание необходимо прервать на 48 часов от момента введения РФП.
Особенности проведения сцинтиграфии костей скелета:
Исследование проводится через 3 часа после введения РФП. Занимает от 10 до 30 минут. Заключение выдается в день исследования.
Пациентам, приходя на исследование, необходимо с собой иметь выписки из историй болезни или амбулаторную карту, заключения (если имеются) по результатам рентгенологических исследований, КТ, МРТ, а также результаты предыдущих сцинтиграфических исследований.
Используемые радиофармацевтические препараты (РФП): диагностику заболеваний костей скелета проводят с меченными фосфатными комплексами, которые прочно связываются с кристаллами гидроксиапатита и незрелым коллагеном. В качестве метки используется 99мТс, который имеет короткий период полураспада – всего 6 ч. Гамма-кванты покидают организм и регистрируются детекторами прибора, в результате после компьютерной обработки получается изображение.
Нормальная сцинтиграмма костей скелета в передней и задней проекции:
Метастазы различных опухолей в кости
Многие опухоли метастазируют в кости. В первую очередь подозрение на метастатическое поражение скелета возникает при раке молочной и предстательной желез, раке легкого, почек и некоторых других. Особую настороженность следует проявлять при увеличении уровня онкомаркеров, например: ПСА (простатспецифический антиген), СА 15-3 и некоторых других. После консервативного лечения или хирургического удаления опухоли рекомендуется динамическое наблюдение за состоянием костной ткани. Сцинтиграфию следует проводить первые 2 раза с промежутком 6-8 месяцев, затем, при нормальном результате исследования, через 1–2 года. Уточнять необходимость проведения повторных исследований нужно у специалиста-радиолога или Вашего лечащего врача.
К достоинствам радионуклидной диагностики следует отнести возможность выявления патологии костной ткани до развития клинических и рентгенологических признаков поражения костей.
Воспалительные и травматические изменений костной ткани
Одним из показаний к проведению радионуклидных исследований костной системы (сцинтиграфии костей) являются воспалительные изменения костной ткани. Метод позволяет определить распространенность процесса, выявив очаги воспаления в костях и суставах во всем скелете, даже на ранних стадиях заболевания. На рентгенограммах при остеомиелитах, как правило, определяется меньшая распространенность процесса, чем на самом деле. Сцинтиграфия же показывает истинные размеры воспалительного очага.
Кроме того, с помощью этого метода можно выявлять переломы и оценивать, насколько хорошо происходит их заживление. Часто переломы костей являются случайной находкой, например переломы ребер у пациентов с распространенным остеопорозом. В ряде случаев удается выявить нарушение целостности костей на ранних стадиях, когда рентгенологическое исследование не позволяет этого сделать, например переломы ладьевидной кости, ребер.
Остеосцинтиграфия в ортопедии и вертебрологии
При протезировании суставов или установке металлоконструкций в позвоночник сцинтиграфия костей скелета позволяет выявить механическую нестабильность компонентов протеза (расшатывание) либо воспалительный процесс вокруг протеза или металлоконструкции. В отличие от других методов исследования (рентген, КТ, МРТ) сцинтиграфия костей скелета позволяет определить интенсивность протекания воспалительного процесса в различных участках кости.
Дополнительное проведение ОФЭКТ/КТ с возможностью посрезового анализа изображения, позволяет более точно локализовать область повреждения, что дает возможность своевременно провести необходимое лечение. Преимущества ОФЭКТ/КТ по сравнению с планарной сцинтиграфией: отсутствие суммации (посрезовый анализ накопления радиофармпрепарата), и точная локализация благодаря совмещению радионуклидного и КТ-изображений.
Как проходит восстановление после процедуры?
Обследование проводится в гамма-камере, которая радиоактивными лучами просвечивает организм человека, выявляя радиофармпрепарат в костях и суставах. Несмотря на кажущуюся сложность, процедура не дает никаких вредных последствий и сразу после диагностики пациент может вернуться к привычному образу жизни. Из рекомендаций на реабилитационный период можно выделить контроль достаточного употребления жидкости в первые сутки (чем больше – тем лучше), а также соблюдение мер качественной личной гигиены – тщательное купание, стирка всех вещей.
Где сделать сканирование скелета?
Выбирая место, где сделать сцинтиграфию, важно доверить процедуру опытным профессионалам, которые максимально корректно проведут дорогостоящее обследование и гарантируют информативность результатов. Еще одним фактором в пользу выбора ЦКБ РАН в Москве является наличие современного оборудования, которое воздействует на пациентов минимально возможной для информативного обследования дозой облучения.
Вредна ли сцинтиграфия костей скелета?
Во время обследования пациент получает минимальную дозу облучения, говоря о том, как часто можно делать сцинтиграфию, большинство специалистов сходятся во мнении – хоть каждый месяц. Абсолютным противопоказанием является беременность пациентки, если же она кормит ребенка грудью, а обследование не терпит отлагательств, после сцинтиграфии рекомендуется в течение суток сцеживать молоко, и лишь потом возвращаться к обычному кормлению.