Тамоксифен или анастрозол что лучше при рмж
Гормонотерапия рака молочной железы
Гормонозависимый рак
Гормонотерапия при раке
Гормоночувствительность
Подробнее о принципах лечения рака молочной железы смотрите ЗДЕСЬ (для специалистов)
Гормонотерапия при раке
Oncotype DX
Endopredict (Эндопредикт)
Эстрогеновые рецепторы
Эстрогеновые рецепторы обозначаются ER.
Рецепторы прогестерона
Прогестиновые рецепторы обозначаются PR. Они тоже находятся на оболочках клеток. С ними взаимодействует прогестерон, стимулируя клетки к делению.
Гормональная терапия
Гозерелин
Удаление яичников
Лучевая кастрация тоже представляет собой исторический интерес.
Когда начинать гормонотерапию
Где купить препараты для гормонотерапии смотрите ЗДЕСЬ
Никто не собирается гормонотерапией делать из женщины мужчину. Борода и усы у Вас не вырастут, голос не изменится.
Как переносится гормонотерапия
Гормонотерапия по сравнению с химиотерапией переносится совершенно иначе. Неприятные ощущения могут возникать в период адаптации в начале лечения (1 мес), но совсем не обязательно. При гормонотерапии нет проявлений токсичности (тошнота, рвота, кишечные расстройства). Она не требует контроля анализов крови.
Тамоксифен
Тамоксифен противопоказан при глаукоме. Обязательно скажите своему врачу, если она у Вас есть.
При сопутствующей сердечной патологии частота и степень её усугубления на фоне приёма Тамоксифена была ниже, чем на фоне приёма ингибиторов ароматазы.
Анализ на Циклин Д1 можно сдать в лаборатории, тел.8 (812) 439-95-28.
Торемифен
Ингибиторы ароматазы
При Her2/neu позитивных (Her2/neu3+) и гормонопозитивных (ER+ и PR+) опухолях Тамоксифен не показал должной эффективности, по сравнению с ингибиторами ароматазы.
Анастрозол иногда провоцирует обострения ревматоидного артрита. Смена его на Фемару (Летрозол) нивелирует этот побочный эффект. Анастрозол и Фемара провоцируют остеопороз и требуют параллельного назначения препаратов кальция и витамина Д (например, КальцийД3 компании Никомед), равно как и ежегодной контрольной остеосцинтиграфии.
Прогнозы при раке молочной железы СМОТРИТЕ ЗДЕСЬ
Гормонотерапия рака молочной железы
Гормонотерапия рака груди
Для проведения гормонотерапии есть оригинальные препараты и дженерики. Стоимость оригинальных препаратов не всегда неподъёмна. Информация об аптеках, легально продающих препараты для гормонотерапии находится ЗДЕСЬ.
| Мы стараемся обеспечить всем нашим пациентам консультацию грамотного химиотерапевта, мотивированного при назначении гормонотерапии только потребностями пациента, а не другими причинами. |
Дополнительно о гормонотерапии Вы можете прочитать ЗДЕСЬ.
Специалисты Университетского Маммологического Центра регулярно повышают свой профессиональный уровень, посещают отечественные и зарубежные конференции, чтобы быть в курсе всех современных тенденций в онкологии и пластической хирургии.
Автор: Чиж Игорь Александрович
заведующий, кмн, онколог высшей квалификационной категории,
хирург высшей квалификационной категории, пластический хирург
Запишитесь на консультацию по телефону: 8 (812) 939-18-00 или через форму на сайте
Тамоксифен или анастрозол что лучше при рмж
В большинстве случаев обследования больных с локализованными опухолями врач приходит к выводу, что болезнь носит преимущественно системный характер, и метастазы разовьются позже. Обнаружение многочисленных метастазов, часто спустя годы после проведения мастэктомии, а также в течение многолетнего наблюдения за больными подтверждает этот вывод.
По данным классических исследований Бринкли и Хейбитл, общая выживаемость больных раком молочной железы через 25 лет после лечения составляет только 20%. Даже среди пациенток, которым мастэктомия была сделана своевременно («ранние» операбельные случаи), выживаемость составляет лишь 30%.
Обычно появление метастазов приводит к смертельному исходу в пределах трех лет, хотя в случаях, когда лечение оказывается эффективным, пациентки могут жить дольше. Вероятность метастазирования опухоли сильно зависит от степени вовлечения подмышечных лимфатических узлов в патологический процесс, что определяется при гистологическом анализе образцов, взятых во время операции.
Существует взаимосвязь между количеством пораженных подмышечных лимфатических узлов и вероятностью распространения метастазов.
Со времени проведения первой операции терапевтической овариэктомии, проведенной Битсоном в 1896 г., стало очевидно, что при изменении гормонального статуса организма в случаях распространенного опухолевого процесса, по крайней мере для одной трети пациенток достигается симптоматический эффект.
Использовались различные методы: удаление яичников или их облучение (иногда называемое «создание искусственной менопаузы»), лечение эстрогенами, антиэстрогенами и антагонистами гонадотропин-рилизинг-гормона (например, гозерелином). Этот гормон регулирует секрецию лютеинизирующего гормона (LHRH).
Также применяли анаболические стероиды, глюкокортикоиды и прогестерон, проводили удаление надпочечников или гипофиза и назначали ингибиторы ароматазы (анастрозол или летрозол).
Стандартный подход основан на менструальном статусе пациентки. Для большинства больных с метастазирующими опухолями в пременопаузе и перименопаузе используется хирургическое удаление яичников или их облучение. Однако с появлением антагонистов гонадотропин-рилизинг-гормона эти процедуры стали применять реже.
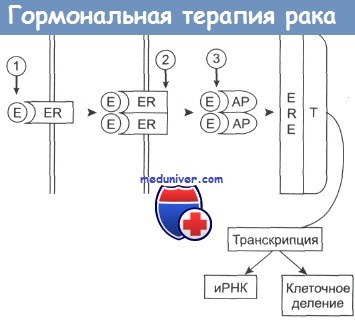
Комплекс приобретает активность (АР) и присоединяется к эстроген-зависимым структурам (ERE) клеточного ядра.
Происходит активация таких белков, участвующих в транскрипции (Т), как РНК-полимераза II, что приводит к синтезу белка и делению клетки.
Гозерелин вызывает снижение уровня эстрогенов в плазме крови (1); фульвестран (2) предотвращает процесс димеризации рецептора и его активацию; тамоксифен (3) связывается с активным комплексом, подавляя его способность инициировать транскрипцию.
Антагонисты обеспечивают стойкое снижение уровня эстрогенов и вызывают у пациентки состояние менопаузы, которое длится в продолжении примерно двух месяцев с начала применения гозерелина. Препарат назначается ежемесячно в виде внутримышечных инъекций. Вместе с тем в качестве альтернативы снова стал популярным такой хирургический метод, как лапароскопическое удаление яичников.
Это достаточно безопасная и несложная операция, после которой пациентка на одну ночь остается в стационаре. Следует отметить, что перед операцией больные проходят тщательный отбор по критерию гормональной чувствительности опухоли, и тем, для кого не предполагается проявление лечебного эффекта, операция не проводится.
Для пациенток с опухолью в постменопаузе широко применяется тамоксифен, поскольку он практически не проявляет побочных эффектов. Препарат действует как антиэстроген, но, вероятно, оказывает и прямой цитотоксический эффект. В течение почти 20 лет тамоксифен использовался в качестве стандартного препарата адъювантной терапии.
Тамоксифен назначается перорально в ежедневной стандартной дозе 20 мг. Он обладает медленным кумулятивным действием. Побочные эффекты редки, однако могут наблюдаться приливы, тошнота, гиперкальциемия, тромбоцитопения, удержание жидкости и расстройство менструального цикла. После приема препарата большинство пациенток прибавляют 1-2 фунта в весе и некоторые отмечают ухудшение состояния кожи, волос и ногтей.
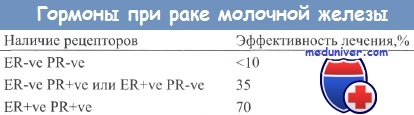
Гораздо более существенный эффект получен при назначении гормонотерапии пациенткам с гормонально зависимыми опухолями, в то время как при лечении гормонально независимых опухолей благоприятный эффект наблюдался лишь в редких случаях. Прогноз в случаях гормонально зависимых и независимых опухолей отличается. Для больных с гормонально-зависимыми опухолями характерен более длительный безрецидивный период и большая выживаемость.
Совместное определение показателей ER и PR обеспечивает более точный прогноз в отношении чувствительности опухоли к гормонотерапии, чем это оказывается возможным при оперировании только показателем ER. Больные с PR-положительными опухолями также характеризуются более длительным безболезненным периодом.
На эффективность гормонотерапии сильно влияет характер распространения метастазов. Костные метастазы проявляют некоторую чувствительность к гормонам, хотя после лечения пациентки живут в среднем около 12-15 месяцев. Тем не менее некоторые больные с гормоночувствительными опухолями и с костными метастазами живут дольше, иногда несколько лет.
В большинстве случаев, при рецидиве опухоли, развившейся в пременопаузе, применяется гозерин (или его аналоги) или лапароскопическая овариэктомия (или облучение яичников). Эти меры эффективны для гормонально чувствительных опухолей. При опухолях в периоде постменопаузы обычно назначают тамоксифен, если пациентки раньше не получали этот препарат в качестве средства адъювантной терапии.
В любом случае можно ожидать, что выживаемость больных составит по крайней мере 30%. Экзогенные гормоны назначают до тех пор, пока не наступит эффект. В дальнейшем гормональную терапию продолжают только тем пациенткам, у которых проявился эффект первичного лечения. Предложены новые противоопухолевые препараты, относящиеся к группе ингибиторов ароматазы.
К числу их относится анастрозол, который блокирует биосинтез предшественников эстрогенов и их последующие превращения в тканях. Анастрозол действует при пероральном применении. Он хорошо переносится больными, так же как и другие родственные соединения, благодаря чему эти препараты быстро заняли место тамоксифена, который оказался неэффективным в лечении пациенток с гормонозависимыми опухолями, развивающимися в период постменопаузы. Рекомендуемая ежедневная доза препарата составляет 1 мг.
Если после первичного лечения возникает рецидив, то назначают другие препараты, например анаболические стероиды, прогестогены и глюкокортикоиды. Анаболические стероиды более эффективны у пациенток с опухолями, развившимися в постменопаузе, и, по-видимому, их особенно необходимо применять в случаях обнаружения костных метастазов.
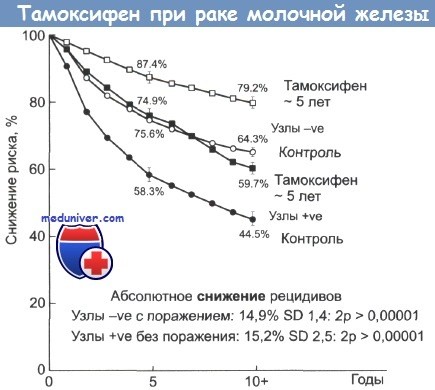
Светлые значки — пациентки без признаков поражения лимфатических узлов; затемненные значки — пациентки с признаками поражения лимфоузлов.
Благоприятный эффект достигается примерно у 20% пациенток, однако недостатком применения стероидов является вирилизация. Удобным для применения является нандролон деканоат (Deca-Durabolin), который назначается в виде внутримышечных инъекций в дозе 50-100 мг каждые 3-4 недели. Если гормонотерапия раньше давала положительные результаты, то можно применять прогестогены. Наиболее часто используется ацетат медроксипрогестерона (МРА, Provera), который обычно назначают перорально в дозе 100 мг три раза в день.
Однако его применение ограничено из-за развития побочного эффекта — прибавления в весе. Такой же эффективностью обладает другое производное прогестерона — мегестрол-ацетат (Megace).
Широко обсуждается вопрос выбора метода лечения первого рецидива опухоли. Следует в этом случае использовать гормональный метод или же химиотерапию с использованием цитотостатиков? Если принимать во внимание количественные показатели, то выбирать надо между гормонотерапией (эффективна в 30% случаев) и комбинационной химиотерапией (эффективность которой в два раза выше). Однако это упрощенное решение вопроса, ответить на который на самом деле сложно.
Реакция опухоли на гормоны обычно носит более продолжительный характер, и у пациентки наблюдаются минимальные токсические проявления. При химиотерапии развивается более кратковременный эффект, который сопровождается токсическими и психологическими осложнениями. Большинство клиницистов в Великобритании в качестве средства первичного лечения предпочитают использовать гормональную терапию. Выбор облегчается все более широким применением метода анализа состояния рецепторов эстрогенов: гормональная терапия должна проводиться только среди пациенток с ER-положительными опухолями. Недавно предложен препарат фульвестрант (Faslodex), подавляющий функции рецепторов эстрогенов. Он может применяться у пациенток с гормоноустойчивыми опухолями, которые развились в постменопаузе. Одним из основных преимуществ этого препарата, по сравнению с агонистом эстрогенов, тамоксифеном, является отсутствие побочных эффектов. Он также не опустошает пул эстрогенов в женском организме, что происходит при применении ингибиторов ароматазы.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Тамоксифен или анастрозол что лучше при рмж
Адъювантная гормональная терапия существенно изменила прогноз больных раком молочной железы с наличием рецепторов эстрогенов и прогестерона в опухоли. При назначении тамоксифена отмечается снижение на 50% частоты рецидива на фоне приема препарата и на 30% в следующие 5 лет после прекращения его приема. Это сопровождается снижением смертности на 30% в течение 15 лет с начала приема тамоксифена. Ингибиторы ароматазы в течение 5 лет обладают еще большим эффектом в сравнении с тамоксифеном, уменьшая риск прогрессирования на 30% за период приема и на 15% риск смерти в первые 10 лет. Однако накопленный опыт показывает, что после прекращения 5-летнего приема тамоксифена или ингибиторов ароматазы у больных сохраняется риск отсроченного прогрессирования. Это послужило основанием для проведения исследований по увеличению сроков адъювантной гормонотерапии.
Увеличение продолжительности приема тамоксифена было изучено в двух опубликованных на сегодняшний день исследованиях (таблица 1). В исследовании NSABP-14 увеличение продолжительности приема до 10 лет не привело к улучшению отдаленных результатов. В это исследование включались больные с N0, а значит с низким риском прогрессирования, что не позволило выявить потенциально возможную пользу длительного приема тамоксифена. В исследовании ATLAS увеличение продолжительности приема тамоксифена с 5 до 10 лет привело к достоверному снижению риска прогрессирования и смерти. При этом польза от длительного приема тамоксифена становится достоверной отсроченно, только после прекращения 10-летнего приема препарата. Причиной улучшения результатов лечения является уменьшение частоты локальных рецидивов заболевания, возникновения контрлатерального рака молочной железы (профилактический эффект) и незначительное снижение частоты отдаленных метастазов. В обоих исследованиях отмечено снижение частоты и выраженности ишемической болезни сердца, отсутствие увеличения частоты инсультов и тромбоэмболий и увеличение в 2 раза (с 2-3% до 4-5%) частоты возникновения рака эндометрия.
Таблица 1. Результаты рандомизированных исследований
по сравнению продленной и стандартной адъювантной гормонотерапии.
| Исследование | Число больных | Лечение | Срок наблюдения после рандомизации | БРВ | OВ |
|---|---|---|---|---|---|
| NSABP B-14 [1] | 1172 | Тамоксифен 5 лет Плацебо 5 лет | 7 лет | 78% 82% | 91% 94% |
| ATLAS [2] | 6846 | Тамоксифен 5 лет Плацебо 5 лет | 10 лет | 78,6%* 74,9% | 87,8%* 85% |
| MA.17 [3] | 1918 | Летрозол 5 лет Плацебо 5 лет | 5 лет | 95%* 91% | 93% 94% |
| NSABP B-42 [4] | 3966 | Летрозол 5 лет Плацебо 5 лет | 7 лет | 84,7% 81,3% | Н.Д. |
| IDEAL [5] | 1824 | Летрозол 5 лет Летрозол 2,5 года | 6,6 года | 82% 85,4% | Н.Д. |
| ABCSG-16 [6] | 3482 | Анастрозол 5 лет Анастрозол 2 года | 5 лет | 78% 78% | Н.Д. |
* – статистически достоверная разница; Н.Д. – нет данных.
Ингибиторы ароматазы продемонстрировали большую эффективность в сравнении с тамоксифеном при проведении адъювантной гормонотерапии больным раком молочной железы с наличием рецепторов стероидных гормонов в опухоли. В связи с этим стало актуальным изучить клиническую эффективность увеличения продолжительности приема ингибиторов ароматазы по сравнению со стандартным 5-летним приемом. В таблице 1 приведены результаты исследования по изучению продленной терапии ингибиторами ароматазы. Следует отметить, что только одно исследование MA.17 опубликовано в полном виде, для всех остальных исследований известна только безрецидивная выживаемость и токсичность терапии. В исследовании MA.17 прием летрозола в течение 5 лет после окончания 5-летней терапии тамоксифеном (79% больных) или ингибиторами ароматазы (21%) привел к достоверному снижению безрецидивной выживаемости, не оказав влияния на общую. Отмечено, что основной причиной снижения безрецидивной выживаемости стало уменьшение частоты контрлатерального рака. В исследования NSABP B-42 10-летний прием летрозола не повлиял на частоту прогрессирования заболевания по сравнению с 5-летним приемом тамоксифена или ингибиторов ароматазы. Анализ токсичности демонстрирует увеличение риска развития сердечно-сосудистых заболеваний и костных переломов на фоне длительного приема препаратов. Риск развития переломов повышается после 7 лет приема ингибиторов ароматазы.
Два исследования посвящены определению оптимальной продолжительности проведения адъювантной гормонотерапии. Дополнительные 5 лет приема были выбраны эмпирически, и остается актуальным сокращение сроков проведения адъювантной терапии для удобства пациентов и уменьшения риска развития побочных эффектов. В исследовании IDEAL сравнивается дополнительное назначение летрозола в течение 2,5 и 5 лет после ранее проведенной стандартной 5-летней адъювантной терапии. При медиане наблюдения 6,6 года после рандомизации не отмечено разницы в показателях безрецидивной и общей выживаемости. Длительный прием летрозола сочетался со снижением частоты контрлатерального рака.
В исследовании ABCSG-16 больным раком молочной железы с наличием рецепторов стероидных гормонов в опухоли и отсутствием амплификации HER2, получавшим адъювантную терапию тамоксифеном или ингибиторами ароматазы в течение 5 лет, назначали дополнительный прием анастрозола в течение 2 или 5 лет. В исследование были включены 3484 больные без признаков болезни на момент рандомизации после 5 лет адъювантной терапии. Стратификация проводилась в зависимости от проводимой гормонотерапии в первые 5 лет (тамоксифен или ингибиторы ароматазы). Предварительные результаты, доложенные на прошедшем симпозиуме по раку молочной железы в Сан-Антонио (США) в декабре 2017 года, свидетельствуют, что частота развития прогрессирования заболевания была одинаковой в обеих группах, безрецидивная выживаемость составила 78% и не зависела от вида гормонотерапии в первые 5 лет. Не отмечено разницы в развитии контрлатерального рака молочной железы. В группе длительного приема анастрозола отмечается повышение частоты костных переломов после 3-го года приема. Авторы делают вывод, что увеличение продолжительности адъювантной терапии на 2 года (всего 7 лет) эффективно предотвращает прогрессирование рака молочной железы и предохраняет от развития побочных эффектов, обусловленных длительным приемом ингибиторов ароматазы. Добавление ингибиторов ароматазы в течение 5 лет не дает выигрыша в улучшении отдаленных результатов и сопровождается увеличением побочных эффектов.
Приведенные исследования показывают, что назначение тамоксифена или ингибиторов ароматазы в течение 7-10 лет может приводить к выигрышу в безрецидивной и общей выживаемости по сравнению с 5-летним их назначением. Очевидно, что выигрыш этот отмечается лишь у меньшинства пациенток, в то время как большинство напрасно получают потенциально токсичную терапию со снижением качества жизни. Поэтому важно при обсуждении увеличения продолжительности гормонотерапии оценивать риск дальнейшего прогрессирования после 5 лет адъювантной гормонотерапии у каждой конкретной больной. Этому было посвящено исследование Оксфордской группы EBCTCG (Early Breast Cancer Trialists Collaborative Group) [7].
Были обобщены 88 исследований по 5-летнему назначению адъювантной гормонотерапии и оценен риск прогрессирования и смерти в течение 15 (5-20) лет после прекращения приема в зависимости от различных прогностических факторов.
Результаты наблюдения за больными в последующие 15 лет после 5-летнего прекращения гормонотерапии демонстрируют увеличение кумулятивного риска прогрессирования и смерти от рака молочной железы. Риск прогрессирования и последующей смерти от рака молочной железы напрямую связан с наличием метастазов и их числом в подмышечных лимфоузлах (см. таблицу 2). В первые 5 лет приема гормональных препаратов наблюдается существенное отставание риска смерти от частоты развития прогрессирования заболевания. Однако при наблюдении в течение 20 лет частота смерти от рака молочной железы догоняет частоту рецидивирования и составляет в зависимости от метастатического поражения подмышечных лимфоузлов 15%, 28% и 49%.
Таблица 2. Риск прогрессирования и смерти при проведении гормонотерапии в течение 5 лет.
| Частота рецидивов | Частота смерти | |||
|---|---|---|---|---|
| 5-летняя | 20-летняя | 5-летняя | 20-летняя | |
| N0 | 6% | 22% | 3% | 15% |
| N1-3 | 10% | 31% | 5% | 28% |
| N4-9 | 22% | 52% | 12% | 49% |
Авторы изучили, какие клинические факторы в наибольшей степени определяют риск прогрессирования после прекращения приема гормонов за период 5-20 лет. Оказалось, что, несмотря на то, что на период 5 лет все больные не имели признаков прогрессирования заболевания, размер первичной опухоли и состояние подмышечных лимфоузлов в момент постановки диагноза в наибольшей степени предсказывали риск прогрессирования в последующие после прекращения приема гормональных препаратов годы. Минимальный ежегодный риск прогрессирования менее 1% и кумулятивный в 13% на период 20 лет отмечается у больных с T1N0. С увеличением размера первичной опухоли и числа метастазов в подмышечные лимфоузлы растет как ежегодный, так и кумулятивный риск прогрессирования, достигая максимальных значений 2,8% и 41% при T2N4-9. У больных с T1N0 на частоту прогрессирования оказывала влияние степень дифференцировки, увеличивая его с 10% при высокой степени до 17% при низкой.
Таким образом, проведенное исследование подтвердило, что после прекращения приема гормональных препаратов в течение 5 лет в последующие годы происходит увеличение риска прогрессирования, степень которого зависит от размера первичной опухоли, наличия и числа метастазов в подмышечных лимфоузлах. Все это оправдывает и объясняет целесообразность увеличения продолжительности приема тамоксифена или ингибиторов ароматазы у больных с высоким риском прогрессирования. При обсуждении необходимости продолжения гормонотерапии после 5 лет приема исследование EBCTCG помогает оценить риск прогрессирования и принять правильное решение.
Можно ли с большей точностью определить популяцию больных, которым показано проведение продленной адъювантной гормонотерапии? Возможно, использование генетических тестов (например, Oncotype DX или MammaPrint) с лучшей точностью в сравнении со стадией болезни позволит выявить пациентов с высоким риском прогрессирования после 5 лет адъювантной терапии. Но пока отсутствуют результаты таких исследований, практический интерес представляет исследование по изучению циркулирующих опухолевых клеток у больных после 5 лет адъювантной гормонотерапии [8]. В исследование, которое было представлено на конференции по раку молочной железы в Сан-Антонио в 2017 году, включались больные раком молочной железы II-III стадий с отсутствием экспрессии HER2, которым проводилась адъювантная химиотерапия с добавлением и без бевацизумаба (исследование E5103). Затем больным с наличием рецепторов стероидных гормонов назначали адъювантную гормонотерапию. У 546 больных без признаков прогрессирования выполняли определение наличия циркулирующих опухолевых клеток в крови методом CELLSEARCH CTC assay в период 4,5-7 лет с момента постановки диагноза.
Оказалось, что циркулирующие опухолевые клетки определяются у 4,8% больных: у больных с наличием рецепторов стероидных гормонов – 5,1%, при отрицательных рецепторах – 4,3%. При медиане наблюдения 1,6 года после выполнения теста наличие циркулирующих опухолевых клеток увеличивает риск прогрессирования в 20 раз у больных с положительными рецепторами и не влияет на частоту прогрессирования при отрицательных рецепторах. Было показано, что риск прогрессирования в ближайшие 2 года у больных с положительными рецепторами и наличием циркулирующих опухолевых клеток и без них составляет 35% и 2% соответственно. Авторы посчитали полученные результаты неожиданными. Первой неожиданностью было обнаружение циркулирующих опухолевых клеток у больных без признаков болезни после 5 лет интенсивной адъювантной химиогормонотерапии. Второй неожиданностью была высокая предсказывающая способность прогрессирования заболевания в случае обнаружения циркулирующих опухолевых клеток только у больных с наличием рецепторов стероидных гормонов в опухоли. И третья неожиданность – это быстрое прогрессирование болезни в этой группе больных после окончания адъювантной гормонотерапии.
Авторы делают вывод, что обнаружение циркулирующих опухолевых клеток у больных с наличием рецепторов стероидных гормонов в момент окончания 5-летнего приема адъювантной гормонотерапии является четким биомаркером быстрого прогрессирования заболевания в ближайшие годы после ее окончания. Можно предположить, что определение опухолевой ДНК в плазме крови больных после 5-летнего приема гормональной адъювантной терапии также может служить индикатором присутствия микрометастазов и высокого риска прогрессирования. Возможно, именно эти больные выигрывают от увеличения продолжительности адъювантной гормонотерапии, а тест на определение циркулирующих опухолевых клеток или опухолевой ДНК будет обязательным для определения оптимальной продолжительности гормонотерапии. Можно думать, что в группе больных с высоким риском прогрессирования будут найдены более эффективные методы лечения в сравнении с увеличением только продолжительности приема гормональных препаратов. Добавление ингибиторов циклинзависимых киназ приведет не только к повышению эффективности адъювантной гормонотерапии, но и к возможному сокращению сроков ее проведения. Интересным представляется назначение ингибиторов контрольных точек иммунного ответа у больных с микрометастазами рака молочной железы после проведения начального этапа гормонотерапии.
Исходя из полученных данных, можно сделать следующие выводы:
Ключевые слова: рак молочной железы, адъювантная гормонотерапия.
Узнать больше о лечении рака молочной железы можно на
Большой конференции RUSSCO «Рак молочной железы»
(25-26 января 2018, Лотте Отель Москва)