Терапия энд что это
Коррекция эндотелиальной дисфункции в терапии мужских сексуальных расстройств (лекция)
Истекшие 1,5 десятилетия ознаменовались значительными успехами в изучении этиологии и патогенеза, совершенствовании диагностики и лечения мужских сексуальных расстройств и, прежде всего эректильной дисфункции (ЭД). Мы не только преодолели устаревшее понятие «импотенция», заменив этот термин на ЭД, но и поднялись от медикаментозного модулирования эрекции с помощью ингибиторов ФДЭ 5 к улучшению качества эрекции, повышению ее твердости, лечению ЭД, восстановлению сексуальной функции в целом и профилактике мужских сексуальных расстройств.
Эректильная дисфункция в понимании большинства урологов одно из наиболее частых мужских сексуальных расстройств болезненные проявления, требующие своевременной диагностики и эффективного лечения. Многообразие ее причин подсказывает, что ЭД следует рассматривать шире как симптомокомплекс, входящий в клиническую картину значительного ряда соматических заболеваний, который по своей выраженности и тяжести непосредственно зависит от них. Известны многочисленные факторы риска, создающие благоприятные условия для развития ЭД: соматические заболевания (ишемическая болезнь сердца, артериальная гипертензия, почечная и печеночная недостаточность), нервные болезни (неврозы, рассеянный склероз, болезни Паркинсона и Альцгеймера, нейропатии различного генеза), психические заболевания (депрессии, астенодепрессивные и ипохондрические состояния), эндокринные заболевания (сахарный диабет, гипои гипертиреоз, андрогенный дефицит, гиперпролактинемия, ожирение, метаболический синдром). Наиболее частыми соматическими заболеваниями, при которых ЭД становится одним из характерных проявлений, являются возрастной андрогенный дефицит (18,3%), сахарный диабет (СД 35%), артериальная гипертензия (АГ 31%), дислипидемия, как предшественник атеросклероза (21%). Кроме того, причиной ЭД может являться и проводимая лекарственная терапия. Лекарственные препараты принимают 74% больных сахарным диабетом, 54% больных ишемической болезнью сердца, 37% больных депрессией. Негативное действие на эректильную функцию оказывает применение гипотензивных средств (тиазидные диуретики, бетта-адреноблокаторы), сердечных гликозидов, «гипогликемических» средств, гормонов (эстрогены, прогестины, глюкокортикоиды, антиандрогены, агонисты гонадотропин-РФ), транквилизаторы, нестероидные противовоспалительные средства, блокаторы Н2-рецепторов и пр.
Все эти обстоятельства заставляют рассматривать проблему диагностики и терапии ЭД не только как узкую задачу специалиста-уролога, андролога и сексопатолога, решение которой направлено на восстановление нарушенной сексуальной функции. Она лежит за пределами только урологии и, с одной стороны, требует знаний и участия других специалистов (врач общей практики, терапевт, кардиолог, невролог, нефролог и пр.), с другой делает необходимым для уролога, андролога, сексопатолога пристальное изучение внутренней медицины тех самых соматических заболеваний, которые тесно связаны с ЭД. Иными словами, эффективная терапия ЭД является, как и большинство проблем мужского здоровья, мультидисциплинарной. Это подтверждает врачебная практика, когда почти 49% больных впервые обращаются по поводу ЭД не к урологу, а к специалистам терапевтического профиля.
У 80% больных причиной развития ЭД является нарушение функции эндотелия. Наряду с генетической предрасположенностью и возрастом эндотелиальная дисфункция (ЭнД) развивается как результат окислительного стресса, предшественниками которого являются артериальная гипертензия (АГ), сахарный диабет (СД), дислипидемия и курение. Окислительный стресс, в свою очередь, ведет к поражению клеток эндотелия, которое усугубляет вазоконстрикцию, обусловливая атеросклероз, тромбозы и ЭД. В основе окислительного стресса лежит дибалланс прои антиоксидантных систем эндотелия с последующим развитием стойкой вазоконстрикции, которая ведет к прогрессированию АГ, атеросклероза, развитию ишемической болезни сердца (ИБС), их тромботическими осложнениями в виде мозговых инсультов и инфарктов миокарда. ЭД является ранним предиктором этих тяжелых заболеваний. Известно, что 57% мужчин, подвергнутых аортокоронарному шунтированию, задолго до операции уже страдали ЭД, а 64% мужчин, госпитализированных по поводу первого острого инфаркта миокарда, отмечали существенные расстройства эрекции. Косвенно это подтверждается и общими факторами риска ЭД и ИБС: АГ, СД, дислипидемия, депрессия, курение, гиподинамия, ожирение. Таким образом, ЭД, возникшую на фоне и вследствие ЭнД, следует считать одним из ранних симптомов сердечно-сосудистых заболеваний. Порой пациенты с сердечно-сосудистыми заболеваниями бывают больше обеспокоены ЭД, нежели риском ИМ на фоне ИБС или мозгового инсульта на фоне прогрессирующей АГ. ЭД, вызывая личностный стресс у мужчины, может, в свою очередь, не только усугубить течение АГ и ИБС, но и существенно нарушать межличностные отношения между половыми партнерами, вызывая депрессии и замыкая патологический круг патогенеза заболевания.
Эндотелиальная дисфункция сложный процесс, основными проявлениями которого являются нарушение биодоступности оксида азота ^О), уменьшение количества мускариновых рецепторов на поверхности эндотелиальных клеток, повышение активности ангиотензинпревращающего фермента (АПФ) на поверхности эндотелиальных клеток. NO один из важнейших биологических медиаторов организма. Окись азота (NO) обладает бронхорасширяющим действием, является возможным медиатором функции памяти и болевой рецепции, регулятором воспаления и иммунной защиты, медиатором деятельности гладкой мускулатуры пищеварительной и мочеполовой систем, гладкой мускулатуры сердечно-сосудистой системы. NO регулирует расширение и сужение просвета сосудов в соответствии с потребностью тканей в кровоснабжении и является средством антитромботической защиты.
NO образуется путем окисления L-аргинина атомом кислорода при участии NO-синтаз, которые обнаружены в эндотелии, миоцитах сосудов, скелетных мышц, миокарда, нейронах, тромбоцитах, фибробластах, нейтрофилах и др. Выработка NO в центральной нервной системе происходит вследствие эротической стимуляции через допаминэргические структуры гипоталамуса, и центральное возбуждение нитрергических нейронов, по-видимому, инициирует эрекцию. Нейрональная NO является важнейшим фактором, вызывающим непосредственное быстрое расслабление сосудов полового члена для возникновения эрекции, NO эндотелиального происхождения необходима для поддержания эрекции под влиянием периферического действия NO-синтазы эндотелиальных клеток. Она способствует поддержанию эрекции, поскольку в гладкомышечной ткани путем активизации гуанилатциклазы обеспечивает образование циклического гуанозинмонофосфата, выходу кальция из клеток, их расслаблению, что при достаточном притоке артериальной крови и действующем веноокклюзивном механизме вызывает устойчивую эрекцию. В гладкомышечных клетках сосудов сердца и кавернозной ткани полового члена NO повышает концентрацию цГМФ, который активирует специфическую протеинкиназу, под действием которой происходит уменьшение концентрации кальция внутри клетки и расслабление гладкомышечных волокон. Разрушение циклического гуанозинмонофосфата под влиянием фосфодиэстеразы 5 типа (ФДЭ 5) обусловливает детумесценцию. Органические нитраты являются донаторами NO, следовательно, существенно повышают продукцию циклического гуанозинмонофосфата (цГМФ). Их применение в сочетании с ингибиторами ФДЭ 5 с целью терапии ЭД опасно тяжелыми коллапсами и, поэтому, противопоказано.
Сочетание ЭД с ИБС патогенетически взаимосвязано, поэтому рациональная терапия подобного сочетания, исключающего применение ингибиторов ФДЭ 5 с органическими нитратами, которые являются одним из основных компонентов ангиангинальной терапии ИБС, не теряет своей актуальности. Не менее серьезной проблемой, возникающей перед урологом и кардиологом, является преодоление страха восстановления утраченной сексуальной функции. Известно, что сексуальная активность увеличивает потребность миокарда в кислороде, что вызывает обоснованные опасения кардиологов. Однако риск развития ИМ при наличии ИБС у мужчины 50 лет составляет всего 1% в год. При повышении сексуальной активности он возрастает до 1,01% в год. Половой акт по энергозатратам составляет от 2-3 до 5-6 метаболических эквивалентов, которые, в сущности, равны игре в гольф (4-5 метаболических эквивалентов) или тяжелой физической работе (3-6 метаболических эквивалентов).
Помимо торможения распада цГМФ под влиянием ингибиторов ФДЭ 5 механизмом накопления цГМФ является увеличение синтеза NО. При связывании NO с гемопротеинами плазмы при участии гуанилатциклазы возникают клеточные эффекты NO расслабление гладкомышечных клеток сосудов сердца и кавернозных тел. ЭнД включает при реакции NO с супероксиданионом образование оксидантов пероксинитрита и гидроксил-радикалов, повреждающее действующих на липиды, белки и нуклеиновые кислоты эндотелия сосудов.
Первым и пока единственным препаратом, усиливающим синтез NO, является импаза (сверхмалые дозы антител к эндотелиальной NО-синтазе). Оказывая непосредственное влияние на активность NO-синтазы, импаза способствует ликвидации эндотелиальной дисфункции одного из ведущих факторов ЭД, курсовая терапия импазой в течение 3 месяцев необходима как лечебный аспект восстановления эндотелия. Эффект от ее применения развивается в зависимости от тяжести эндотелиальной дисфункции с первой недели до 1 месяца. При этом стимулирующий прием таблетки за час до сексуальной близости не нужен. ЭФ восстанавливается в процессе курсовой терапии в ответ на сексуальную стимуляцию. К концу курса терапии эффект закрепляется и сохраняется в течение полугода, что позволяет пациентам сохранить свои сексуальные способности и без приема лекарств. У пожилых с сопутствующими сосудистыми заболеваниями этот позитивный эффект может быть короче, как правило, бывает необходима поддерживающая терапия по 1 т. через день. Положительный лечебный эффект может сохраняться более длительное время после окончания курса в зависимости от возраста и образа жизни пациента. Курсовая терапия импазой позитивно влияет на все составляющие сексуальных отношений. Больные отмечают улучшение и восстановление спонтанных эрекций, нахождении полового члена в состоянии постоянной частичной тумесценции, а после 3-4 месяцев терапии нормализацию спонтанных и адекватных эрекций. При терапии импазой имеет место кумулятивный эффект, поэтому для наступления стойкого лечебного эффекта необходим ее прием не менее 3-4 месяцев, прогрессирующее нарастание эффективности имеет место с 33,2% после 1-го месяца до 56,2% к 3-4 месяцам лечения.
Циклический ГМФ играет ключевую роль не только в расслаблении мышц кавернозных тел при эрекции, но и опосредует нейрогенный и зависимый от эндотелия путь расслабления гладких мышц артерий миокарда и кровеносных сосудов. Поскольку роль дисфункции эндотелия в развитии гипертонической болезни и ишемической болезни сердца подтверждена, воздействие на недостаточность эндотелия можно рассматривать как универсальный метод патогенетического лечения этих заболеваний, сочетающихся с ЭД. На фоне кардиотропной терапии в сочетании с импазой у больных ИБС со стенокардией напряжения повышается переносимость физической нагрузки, уменьшается количество болевых приступов при легкой и умеренной физической нагрузке. Введение импазы в комплекс лечения способствует увеличению перфузии как показателя усиления коронарного микроциркуляторного кровотока. У больных гипертонической болезнью дополнение гипотензивной терапии приемом импазы способствует не только улучшению микроциркуляции, но и уменьшает выраженность ЭД, что оказывает благоприятное воздействие на течение болезни в целом. Применение импазы в составе комбинированной гипотензивной терапии (с Р-адреноблокаторами и диуретиками) ведет не только к достоверному улучшению ЭФ и основным компонентам сексуальной функции в целом, но и к нормализации суточного профиля АД, коррекции эндотелиальной дисфункции, улучшению психологического состояния больных со снижением депрессии и проявлений ипохондрии. Максимальный положительный эффект имеет место при курсовом применении импазы в течение 3 месяцев. Препарат не вызывает побочных эффектов и нежелательных взаимодействий с гипотензивными препаратами, что доказывает его эффективность и безопасность у больных АГ.
В силу стабилизации уровня тестостерона импаза способна нивелировать проявления мужского возрастного андрогенодефицита. Позитивный лечебный эффект импазы доказан при сочетании ЭД с метаболическим синдромом, сахарным диабетом, аденомой простаты. Нормализация функции эндотелия под влиянием импазы повышает чувствительность его к ингибиторам ФДЭ 5, позволяет избежать их применения в больших дозах с нежелательными побочными эффектами. В сочетании с заместительной тестостеронотерапией она позволит разработать наиболее действенный подход к терапии ЭД и ее соматических «спутников» второй половины жизни мужчин.
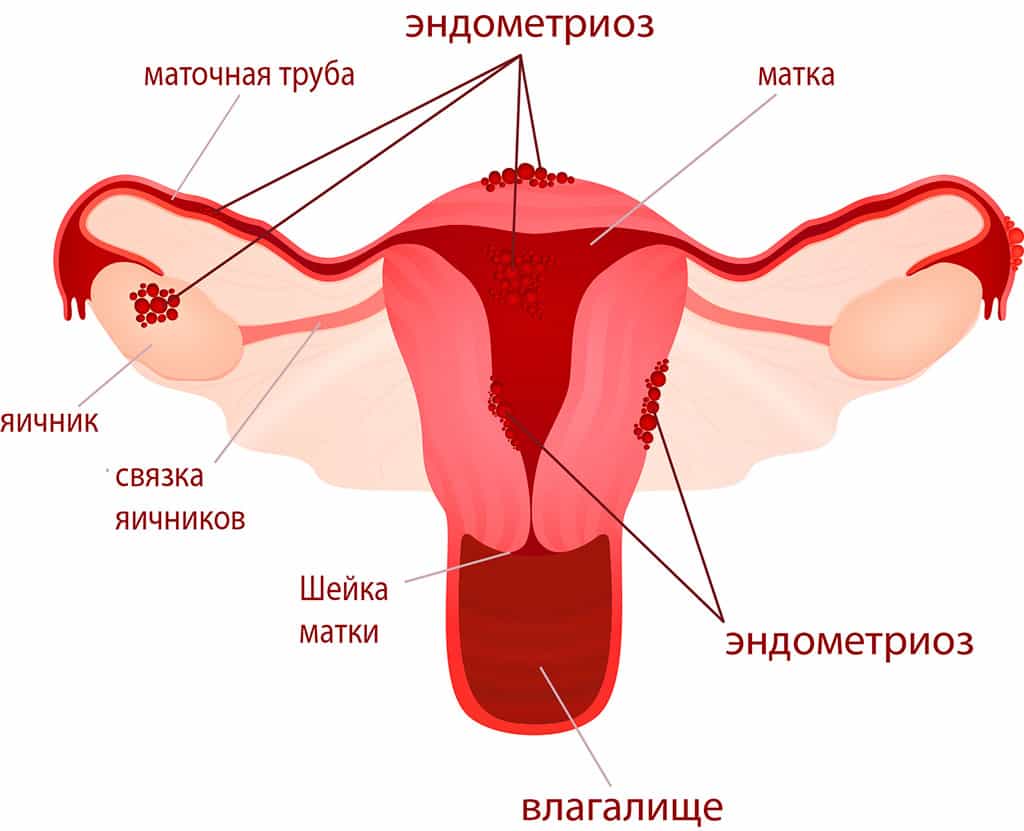
Эндометриоз
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
Эндометриоз обнаруживается не только отделах репродуктивной системы, но и вне ее (брюшная стенка, мочевыделительная система, пищеварительный тракт, брюшина, легкие и пр.). Клинические проявления разнообразны и зависеть от расположения патологического процесса. Могут выражаться: болью, нарушениями менструального цикла (кровянистых выделений перед началом менструации, контактных кровянистых выделений).
Причины эндометриоза
Единой версии причин возникновения эндометриоза на сегодняшний день нет.
1 теория: «Ретроградная менструация или имплантационная теория»
У некоторых женщин имеется склонность к такой особенности как ретроградная менструация (когда мышечный слой матки сокращается в обратном направлении от шейки матки). В период месячных (регул) кровь с элементами эндометрия за счет перистальтических движений гладкомышечной мускулатуры матки заносится в брюшную полость и фаллопиевы трубы, где эндометрий имплантируется в ткани различных органов. В течение обычного менструального цикла внутренний слой матки (эндометрий) отделяется и выводится из полости матки, в то время как в других органах, пораженных эндометриозными очагами, происходят микрокровоизлияния и возникает асептическое воспаление. Вероятность появления эндометриоза может увеличиться от таких причин как: особенности строения маточных придатков, иммунные патологические процессы, аборты, операции на матке, кесарево сечение, оперативное лечение заболеваний шейки матки, наследственная предрасположенность.
Особенно высока роль наследственности при рассматриваемой патологии и предполагает весьма высокую возможность возникновения болезни у дочери, если её мать ранее перенесла такое заболевание. Зная о предрасположенности к данной патологии, женщина, соблюдая меры профилактики, может предотвратить возникновение болезни. Так, например, после оперативных вмешательств на органах репродуктивной системы женщине необходим систематический контроль состояния здоровья для предотвращения возможных осложнений.
2 теория: «Генные мутации»
3 теория: «Отклонения в функции клеточных ферментов и реакции рецепторов к гормонам»
Однако, последние две теории не получили повсеместной популяризации в связи с малой базой доказательности. Классификация эндометриоза разделяется по локализации.
Классификация эндометриоза
Генитальный. Из самого названия следует, что при течении болезни в этой форме эндометриозные очаги располагаются в тканях детородных органов пациентки.
Экстраперитонеальный (внебрюшинный) эндометриоз возникает в органах не покрытых брюшиной: в нижних частях половых органов, вульве, в шейке матки (ее влагалищном сегменте), позадивагинальной перегородке и пр. В мускульном слое матки может сформироваться внутренний эндометриоз (аденомиоз), при этом матка обретает шаровидную форму и достигает величины до 5-6 недели беременности.
Экстрагенитальный эндометриоз. При этой форме эндометриозные очаги находятся за пределами репродуктивной системы (пищеварительный тракт, дыхательная система, мочевыделительная система, послеоперационные рубцы).
При серьезных, осложненных случаях болезни эндометриоз бывает смешанный.
В зависимости от глубины и распространения очагов эндометриоза различают 4 степени:
В зависимости от цикличности регул эндометриозные очаги большей частью проявляются в преддверии месячных. Очаги имеют самую различную локализацию и обнаруживаются не только на поверхности органов, но и проявляют тенденцию к глубокой инвазии в ткани. При вовлечении яичников в процесс эндометриоза кисты сгруппированы и наполнены кровянистым содержимым. Исходя из размеров и глубины эндометриозных поражений, а также локализации образований, степень эндометриоза определяют по бальной системе.
Симптомы эндометриоза
Тазовая боль. Возникает у 16-24% пациенток. Может иметь как точечную, так и разлитую локализацию, возникает и усиливается в корреляции от менструального цикла, может быть и постоянной. Зачастую она вызвана с воспалением и спаечным процессом, развивающимися при поражении эндометриозом.
Постгеморрагическая анемия. У 25-40% пациенток из-за значительной хронической кровопотери во время менструаций может возникнуть состояние малокровия. Постепенно нарастает слабость, бледность или желтушность кожных и слизистых покровов, головокружение, утомляемость, сонливостью раздражительность и психической возбудимостью.
Бесплодие. Точно дать оценку тому, как и почему возникает бесплодие при поражении эндометриозом, ученые и врачи сегодня не в силах. Связывают это с процессами в придатках матки при эндометриозе, с перебоями в функционировании общего и местного иммунного статуса организма в целом, и как итог- сбои в овуляторных процессах. Не абсолютна, но достаточно высока при эндометриозе возможность не наступления беременности. Эндометриоз и сопутствующие ему процессы могут провоцировать самопроизвольные аборты, которые в свою очередь, кардинально и значительно сокращают шансы не только на наступление беременности, но и на нормальное её течение. Поэтому беременные с эндометриозом в анамнезе должны постоянно наблюдаться у врача.15- 56% пролеченных от эндометриоза пациенток беременеют в течение 6-12 месяцев.
Диагностика эндометриоза
С внедрением малоинвазивных методов диагностики и лечения (гистероскопии и лапароскопии) выявляемость эндометриоза значительно увеличилась.
В силу своей схожести протекания данного заболевания с другими, похожими по симптоматике, заболеваниями половых органов, на всех этапах постановки диагноза очень важное значение имеет дифференциальная диагностика. Врач тщательно собирает жалобы и анамнез, информацию о перенесенных заболеваниях, в том числе репродуктивной системы, хирургических операциях, наличии гинекологического и акушерского отягощённого анамнеза у родственников по женской линии.
Дальнейшее обследование включает в себя:
Комплекс всех методов позволяет выявить эндометриозные очаги до 96% случаев.
Заключительный диагноз можно поставить только в том случае, если произведено гистологическое исследование биоптата из очагов эндометриоза, взятых при проведении гистероскопии (лапароскопии).
Лечение эндометриоза
Очень важно в определении тактики терапии эндометриоза учитывать следующие факторы:
к какой возрастной категории относится пациентка,
количество беременностей, в том числе окончившихся родоразрешениями,
важно знать, как протекали роды и не было-ли в послеродовом периоде каких-либо осложнений,
учитывается тяжесть патологического процесса, его местонахождение, глубина, сопутствующие патологии, желание родить ребенка.
При терапии эндометриоза действия врача направлены не просто на устранение проявлений рассматриваемой болезни, но и её последствий (спаечные и кистозные образования, психоневрологические проявления, пр.).
Оперативное лечение эндометриоза
При средней и тяжелой стадиях эндометриоза рекомендуется прибегать к органосохраняющему хирургическому лечению с удалением очагов. Лечение всесторонне нацелено на резекцию гетеротопий в пораженных органокомплексах, резекцию эндометриоидных кист в яичниках, а также рассекание спаек. Как правило, оно применяется, если эффект от медикаментозного лечения отсутствует, имеются различные противопоказания, например непереносимость препаратов или их компонентов, при обнаружении эндометриоидных новообразований размером более 3-4 сантиметров, дисфункции мочевыделения, проблемах с желудочно-кишечным трактом. Зачастую оперативное лечение совмещают с лекарственным. Вмешательство осуществляют лапароскопическим или лапаротомным доступами.
Если у пациентки в возрасте после 40 лет активно прогрессирует заболевание и консервативно-хирургические мероприятия не дают должного эффекта, то прибегают к радикальному хирургическому удалению эндометриоза (экстирпация матки с придатками). Такие мероприятия применяются не часто и встречаются у 12% пациенток.
Основные принципы хирургического лечения эндометриоза с позиций доказательной медицины
Независимо от того, насколько далеко и глубоко распространился патологический процесс, лапароскопия является предпочтительным хирургическим доступом («золотой стандарт») при лечении эндометриоза. Она способствует лучшей визуализации очагов, благодаря их оптическому увеличению, минимальной травматизации тканей и более быстрой реабилитации пациенток, чем после лапаротомии. Лечебно-диагностическая лапароскопия с удалением эндометриозных новообразований обеспечивает значительное уменьшение интенсивности ассоциированных с эндометриозом болей.
Эндометриомы яичников у женщин с тазовой болью должны быть удалены хирургическим путем при лапароскопии.
Женщинам в детородном возрасте принципиально важно излечиться от эндометриоза яичников без риска рецидивирования с максимальным сохранением не поражённой ткани овоцитов. Для этого выполняют пункцию, дренирование кисты, алкоголизацию и уничтожение капсулы путем воздействия энергии различных видов. Однако, все эти методы не позволяют полностью удалить капсулу кисты, что может привести к рецидиву болезни.
У женщин, незаинтересованных в беременности эндометриозные очаги могут быть удалены лапароскопическим или комбинированным лапароскопически-влагалищным доступом, при необходимости в сочетании с одновременной резекцией пораженного участка стенки прямой кишки или в едином блоке с маткой.
Радикальным методом лечения аденомиоза можно считать лишь удаление матки (экстирпация матки). Данная операция, как правило, производится лапароскопическим путем. При выполнении операции по удалению матки очень важно удалить все видимые эндометриоидные очаги, при этом двухстороннее удаление яичников может способствовать более эффективному исчезновению боли и уменьшению вероятности рецидива заболевания.
С каждой пациенткой индивидуально должен обсуждаться вопрос об удалении яичников.
Консервативное лечение применяется, если эндометриоз имеет скрытое латентное течение, возраст пациентки до 45 лет, во время пременопаузы, и имеется потребность сохранения репродуктивной функции.
Гормонотерапия при лечении эндометриоза
Полная реконвалесценция при эндометриозе наступает только при его раннем выявлении и качественной последующей терапии.
Оценочными показателями выздоровления от эндометриоза являются: хорошее самочувствие, отсутствие жалоб на тазовые боли, непоявление рецидивов в течение 5 лет после терапии, восстановление или сохранение функции деторождения.
При современном уровне развитости хирургической гинекологии с обширным использованием органосохраняющих методов лечения, всего вышеперечисленного можно добиться у 60% женщин возрасте от 20 до 36 лет. Если пациентка была оказана помощь в виде радикальной операции, то заболевание не рецидивирует.
1. Эндометриоидные кисты яичников («шоколадные» кисты), заполненные старой менструальной кровью.
2. Кровоизлияния и рубцовые изменения.
Эти два осложнения с большой долей вероятности могут привести к состоянию бесплодия. Обширные и распространенные эндометриозные очаги оказывают давление на нервные стволы и окончания, что приводит к разнообразным неврологическим нарушениям. Редко встречается озлокачествление перерожденных очагов эндометриоза. По данным ученых, у женщин с эндометриозом риск развития онкологических перерождений на 50% выше среднестатистических.
Профилактика эндометриоза
Чем раньше при появлении первых симптомов эндометриоза женщина приходит на консультацию к гинекологу, тем выше шанс на полное избавление необходимости оперативного лечения. Попытки самостоятельной терапии или отсрочка обращения за помощью совершенно не оправданы: с очередным менструальным циклом появляются новые эндометриозные очаги, возникают кисты, усиливаются рубцовые и спаечные процессы, усугубляется состояние фаллопиевых труб.
Для профилактики эндометриоза, необходимо:
обследование девочек-подростков и женщин с жалобами на боли во время месячных;
курирование пациенток после абортов и других иных манипуляций на матке для ликвидации возможных последствий;
своевременная и полная элиминация острых и хронических патологий гениталий;
прием оральных гормональных контрацептивов.
Риск возникновения эндометриоза выше у курящих женщин в возрасте после 30-35 лет с коротким менструальным циклом, страдающих нарушениями метаболизма, ожирением, излишним весом; имеющих внутриматочные контрацептивы; с повышенным уровнем эстрогенов; страдающих иммунодепрессией; имеющих наследственную предрасположенность и перенесших операции на матке.