Тромбоз пба что это
Тромбоз пба что это
Эффективные технологии удаления тромбов!
Центр спасения конечностей от гангрены
Московская область, город Клин, улица Победы влад. 2
Записаться на прием
Вопросы-ответы
Здравствуйте, уважаемый доктор. Обращаюсь к Вам по вопросу спасения конечностей стопы моего отца, сейчас он находится в больнице ему уже ампутиповали больше пол стопы. Обратился своевременно и даже подозреваю, что.
Ответ: Пришлите на почту [email protected] фотографию стопы и данные исследований сосудов.
Ответ: Боюсь, что это очень надолго. Когда была операция?
Сухая гангрена, что делать?
Ответ: Приезжайте на консультацию. Мы этим занимаемся и спасаем ноги в большинстве случаев.
Нога ампутирована, рана не заживает
Добрый день! Отец мужа 6 раз оперировался в городской больнице. Ногу спасти не удалось и недавно ампутировали выше колена. Рана не заживает, гноится. А в больнице просто выписывают и толком ничего.
Ответ: Вам надо прислать фотографию культи и выписку из больницы (последнюю)
атеросклероз артерий нижних конечностей ХАН 2 стадии
Ответ: Все рекомендации корректны и при их исполнении должны вам помочь.
Шунтирование артерии нижней конечности
Здравствуйте. Скажите пожалуйста делают ли повторные операции шунтирование артерии на ноге.
Ответ: Конечно, если есть необходимость и условия для этого.
Здравствуйте. У деда некроз 4 пальца и отёк уже стопы. На снимках видны сосуды до колена. Палец не удалили объяснив что дальше ещё быстрее пойдёт. Если удалять, то сказали надо.
Ответ: Я советую обратиться к компетентным сосудистым хирургам, занимающимся проблемой критической ишемии.
где и когда можно прооперировать ногу?? мы из Армении согласны приехать.. врач посоветовал обратиться к вам.. далее присылаю эпикриз врача
Ответ: Пришлите данные обследований и фотографии ноги на почту [email protected]
Стеноз чревного ствола
Добрый день! Мне после КТ с контрастом поставили диагноз \»Стеноз Чревного ствола 70%\» и сказали, что нужна операция. На сколько это серьёзно и если необходимо делать операцию, то как срочно.
Ответ: Любая операция имеет риски. Но стентирование чревного ствола не очень опасно. Нужна очная консультация, чтобы точно определить показания к операции.
Я повредил руку сорвал кожу при подении на гравии и ржавчина рука за два часа опухла что делать
Ответ: К хирургу на прием.
© 2007-2021. Инновационный сосудистый центр — сосудистая хирургия нового уровня
Контактная информация:
Место ангиопластики при лечении окклюзированных (длиной более 10 см) бедренных артерий.
Структура статьи
Поражение бедренных артерий является наиболее часто встречающейся локализацией атеросклеротического поражения артерий нижних конечностей. При обследовании популяции населения старше 50 лет, ее частота составляет 1%, а у больных с периферическим атеросклерозом 55%. [1].
Клинически поражение этой зоны протекает доброкачественно, около 78% пациентов с перемежающейся хромотой при проведении только консервативной терапии составляют стабильную группу в течение 6-ти лет [2]. Инвалидизирующая перемежающаяся хромота и критическая ишемия являются показанием к оперативному лечению – хирургической (реконструктивная сосудистая операция или ангиопластика ) реваскуляризации, при этом операцией выбора до настоящего времени считается шунтирование.
Чрескожная транслюминальная ангиопластика (ЧТА) уже почти 40 лет интенсивно внедряется в лечение окклюзирующих поражений бедренных артерий. Возможность реканализации длинных окклюзий, хорошие непосредственные результаты, простота процедуры, очень низкий процент осложнений постепенно расширяют показания к ЧТА и в настоящее время она проводится даже у пациентов с выраженными и распространенными поражениями периферических артерий.
Несмотря на совершенствование методики и инструментария, широкое внедрение стентирования и энтузиазм исследователей, отдаленные результаты ангиопластики в 90-е годы не соответствовали результатам реконструктивных операций.
Эти данные значительно отличаются от результатов операций в аорто-подвздошной зоне, в которой роль ангиопластики достоверно выше и отдаленные результаты не отличаются от результатов реконструктивной хирургии 10.
Тем не менее, продолжаются исследования с многофакторным анализом, в каких случаях ЧТА предпочтительнее реконструктивной хирургии и какие причины влияют на отдаленные результаты. В данной работе мы анализируем наш опыт ангиопластики окклюзированных (длиной более 10 см) бедренных артерий.
Материалы и методы.
С 1993 года по 2002 год, мы произвели 73 эндоваскулярных реканализации окклюзированных поверхностных бедренных артерий (ПБА) у 58 пациентов (56 мужчин и 2 женщины). Длина поражения более 10 см (от 11 до 26 см, средняя длина 15.5 см). В 8 случаях у 7 больных были полностью окклюзированные ПБА от устья до входа в Гунтеров канал.
Техника оперативного вмешательства.
После проводниковой реканализации выполнялась баллонная ангиопластика, использовались баллонные катетеры «Opta» (Cordis), диаметр баллона 5, 6 и 7 mm, длинной 100 мм.
Результаты.
Непосредственные результаты:После удачной проводниковой реканализации с последующей баллонной дилятацией и стентированием хорошие ангиографические и клинические результаты были достигнуты во всех случаях. Осложнения отмечены у 4 больных (6.0%). В 2 случаях произошла дистальная артериальная эмболия, в 2 других образовалась ложная аневризма бедренной артерии. Периферическая макроэмболия с перекрытием кровотока подколенной артерии или магистральных артерий голени – одно из основных осложнений реканализации хронических окклюзий. В одном случае эмбол удалось аспирировать через катетер, в другом случае – эмбол был низведен в переднюю тибиальную артерию и произведена открытая эмболэктомия типичным доступом на уровне лодыжки. Ложные аневризмы были пролечены с помощью давящей повязки, контролируемой ультразвуком.
Ближайшие и отдаленные результаты: Результаты оценивались по первичной и вторичной проходимости оперированных артерий
Контроль осуществляли с помощью клинического осмотра с использованием неинвазивных методов исследования (измерение ПЛИ и ультразвуковое дуплексное сканирование) в сроки 3, 6, 12 месяц и затем ежегодно.
Высокая вторичная проходимость при стентировании непосредственно связана с обязательным периодичным неинвазивным дуплексным обследованием зоны ангиопластики для как можно более раннего выявления неоинтимальной гиперплазии и борьбы с ней.
Анализируя результаты исследования и данные литературы, мы считаем, что ЧТА является методом выбора при лечении окклюзий в бедренной зоне.
Выбор способа реваскуляризации при поражениях ПБА основывается на анализе общего состояния пациента (с учетом возраста, сопутствующей патологии); данных инструментальных методов исследования (протяженности и степени поражения и состоянии дистального артериального русла), а также степени ишемии, наличии трофических нарушений, инфекции.
Применение ангиопластики и стентирования длинных окклюзии ПБА позволяет достичь удовлетворительных результатов в большинстве случаев, как непосредственно после операции, так и в отдаленном периоде, сопоставимых, а в ряде случаев превосходящих стандартные операции шунтирования.
Облитерирующие заболевания аорты и артерий нижних конечностей
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
РГМУ имени Н.И. Пирогова
Х ронические облитерирующие заболевания аорты и артерий нижних конечностей (обусловленные в большинстве случаев атеросклерозом) составляют более 20% от всех видов сердечно-сосудистой патологии, что соответствует 2–3% от общей численности населения [1]. Так, в эдинбургском исследовании (1990) [2] пациенты с перемежающейся хромотой составили 4,5% в возрастной группе от 55 до 74 лет, а асимптомные поражения отмечены в 8% случаев. Показательно, что лечащие врачи только 30–50% пациентов знали о наличии у последних перемежающейся хромоты [3].
Главной особенностью данной патологии является неуклонно прогрессирующее течение, характеризующееся нарастанием выраженности перемежающейся хромоты и переходом ее в постоянный болевой синдром или гангрену, которая возникает у 15–20% больных [4]. Периоперационная летальность при ампутациях ниже колена составляет 5–10%, выше колена – 15–20%. Летальность в течение первых двух лет после ампутации колеблется в пределах 25–30%, а через 5 лет – 50–75%. При этом после ампутации голени на протезе через 2 года ходят лишь 69,4% больных, а бедра – всего 30,3%.
Летальность после реконструктивных операций, ранее составлявшая 2–13% [5], в настоящее время в ведущих клиниках России не превышает 1,2% [6]. Оценивая необходимое количество операций больным с облитерирующими заболеваниями аорты и артерий нижних конечностей, можно как пример привести США, где в 1995 г. выполнено 400 000 госпитализаций по поводу заболеваний периферических артерий. Было выполнено 50 000 баллонных ангиопластик, 110 000 шунтирований, 69000 ампутаций. При этом расходы при первичной ампутации в развитых странах, таких как Великобритания, превышали вдвое расходы при успешной реваскуляризации [7].
По данным Л.А. Бокерия и соавт. [8], на 1998 г. потребность в реконструктивных операциях на артериальной системе в России составляет 930 на 1 млн населения, ежегодно выполняется не более 22% от необходимого количества.
Патоморфология и патогенез
Термин “атеросклероз” происходит от греческих слов “athtre” – пшеничная кашица и “sclerosis” – твердый. Несмотря на то что патоморфология атеросклероза изучается более 140 лет, начиная с первых работ Р. Вирхова (1856), характер и особенности процессов, происходящих в стенке сосудов при этом заболевании, остаются до конца не ясными. Даже наблюдаемые при микроскопическом исследовании клеточные и внеклеточные изменения в стенке сосуда в области формирования атеросклеротической бляшки трактуются по-разному. При формировании атеросклероза основные изменения происходят в эндотелии и гладких мышечных клетках субэндотелиального слоя интимы.
Различают 4 вида атеросклеротических изменений сосудов:
1. Жировые пятна или полоски, представляющие собой участки бледно-желтого цвета, содержащие липиды, не возвышающиеся над поверхностью интимы. Это наиболее ранние проявления атеросклероза.
2. Фиброзные бляшки – овальные или округлые образования, содержащие липиды, возвышающиеся над поверхностью интимы, нередко сливающиеся в сплошные бугристые поля.
3. Фиброзные бляшки с различного рода осложнениями: изъязвлением, кровоизлиянием, наложением тромботических масс.
4. Кальциноз – отложение в фиброзных бляшках солей кальция.
Наиболее значительные атеросклеротические изменения чаще всего локализуются в местах наибольшего гемодинамического или механического воздействия на стенку сосуда: зонах бифуркации, местах отхождения магистральных артерий от аорты и в извитых участках артерии.
По данным J.S.A. Fuchs [9], к ведущим факторам риска развития атеросклероза относятся артериальная гипертензия, гиперхолестеринемия и курение. В меньшей степени влияют ожирение, сахарный диабет, гипертриглицеридемия, сидячий образ жизни, стресс и наследственность.
Современные методы диагностики
Современные методы диагностики расстройств периферического артериального кровообращения отличаются широтой диапазона – одни используются для уточнения клинического диагноза, характера и степени поражения сосудов, другие – для оценки эффективности проводимого лечения либо динамического наблюдения за больным. С целью изучения гемодинамики в нижних конечностях и топической диагностики поражений артериального русла используют следующие инструментальные методы исследования: ультразвуковая допплер-сфигмоманометрия, тредмил-тест, ультразвуковое ангиосканирование, в том числе дуплексное, и рентгеноконтрастная аортоартериография. Кроме этого, необходимо определять показатели липидного обмена, свертывающей системы и реологических свойств крови.
Как первый этап, всем пациентам с подозрением на окклюзионно-стенотическое поражение аорты или артерий нижних конечностей выполняется ультразвуковая допплерография с измерением лодыжечно-плечевого индекса.
Этот индекс составляет отношение максимального давления на одной из берцовых артерий к давлению на плечевой артерии. Снижение этого показателя менее 0,9 требует более пристального внимания к пациенту. В этой связи одним из наиболее перспективных в настоящее время представляется комбинированное использование ультразвуковой допплерометрии и стандартного тредмил-теста [10]. К неинвазивным методам исследования также относится ультразвуковое ангиосканирование, благодаря которому можно с большой долей достоверности определить степень стенотического поражения. В последнее время дуплексное ультразвуковое ангиосканирование в алгоритме диагностической программы занимает одно из ведущих мест вследствие неинвазивности и безопасности, а также высокой чувствительности и специфичности. По данным дуплексного сканирования определяется не только структура атеросклеротической бляшки, но и оценивается гемодинамическая степень стеноза, что имеет принципиальное значение. Рентгеноконтрастное ангиографическое исследование в настоящее время остается основным методом диагностики облитерирующих заболеваний сосудистого русла. С помощью этого метода возможно точно определить локализацию, протяженность, степень и характер стеноза, множественность окклюзионных поражений магистральных артерий нижних конечностей, оценить состояние коллатерального русла, прогнозировать характер и объем реконструктивной операции, а также осуществлять контроль за эффективностью лечения и хирургического вмешательства. В арсенале ангиологов и сосудистых хирургов имеются также такие методы диагностики, как лазерная допплер-флоуметрия, транскутанное мониторирование О2, фотоплетизмография, радиоизотопное исследование, компьютерная томография и ядерно-магнитный резонанс.
Терминология и клиническая классификация
В клинической практике для обозначения заболеваний брюшной аорты, приводящих к ее сужению или окклюзии, часто употребляют термин “синдром Лериша”, который обобщает картину поражения бифуркации брюшной аорты и подвздошных артерий.
Основными особенностями клинического течения этого поражения являются высокая перемежающаяся хромота (боль в конечности при ходьбе), двустороннее отсутствие пульса на артериях и импотенция.
Примерно у 30% пациентов с хронической артериальной недостаточностью нижних конечностей атеросклеротический окклюзирующий процесс локализуется в брюшном отделе аорты, у 70% больных – в артериях бедренно-подколенного сегмента.
Тактические вопросы в выборе того или иного метода лечения при атеросклеротическом поражении аорты и артерий конечности основываются на выраженности хронического ишемического синдрома, который классифицируется по 4 стадиям заболевания. Преобладающей системой оценки являются классификация R. Fontaine и А.В. Покровского.
При 1-й стадии заболевания боль в нижних конечностях появляется только при большой физической нагрузке, она не связана с проходимой пациентом дистанцией.
Для 2-й стадии характерно появление лимитирующей боли при ходьбе (лимитирующая перемежающаяся хромота). С тактических позиций эту стадию подразделяют на 2А (проходимая дистанция без боли более 200 м) и 2Б (появление болей при ходьбе на расстояние менее 200 м).
Боль в конечности в состоянии покоя характеризует 3-ю стадию, появление язвенно-некротических изменений – 4-ю стадию заболевания.
Хирургическая тактика и определение степени операционного риска
Принципиальной общепризнанной позицией в выборе метода лечения в соответствии с данной классификацией считается необходимость восстановления магистрального кровотока с применением реконструктивных операций, начиная со стадии 2Б.
Исходя из всего вышеизложенного, лечение больных атеросклерозом должно быть комплексным, направленным как на восстановление кровообращения в аорте и магистральных артериях конечности, так и на коррекцию сопутствующей патологии. Основная цель – восстановление крообращения – должна достигаться с минимальной травмой для больного.
Принципы консервативного лечения
Одним из главных направлений консервативного лечения является улучшение реологических свойств крови. И это не случайно, так как у больных имеются выраженные отклонения реологических характеристик: повышение уровня фибриногена в плазме, увеличение времени агрегации тромбоцитов, вязкости крови и плазмы, уменьшение фибринолитической активности крови и изменение показателей тромбоэластограммы в сторону гиперкоагуляции.
Среди лекарственных средств, используемых для консервативной терапии, выделяется несколько групп.
1. Спазмолитики: периферические миолитики (папаверин, дротаверин, бенциклан), препараты блокирующие a-адренорецепторы или преганглионарную передачу импульса (кофеин, празозин), центральные холиномиолитики (толперизон, баклофен), вещества с разносторонним действием (абана).
2. Дезагреганты: пентоксифиллин, ацетилсалициловая кислота, ксантинола никотинат, тиклопидин, реополиглюкин.
3. Антиатеросклеротические средства: препараты, блокирующие всасывание холестерина из кишечника (холестирамин), тормозящие биосинтез и перенос холестерина и триглицеридов (производные фиброевой кислоты – клофибрат, ципрофибрат) и статины (ловастатин, симвастатин), другие средства (никотиновая кислота).
4. Препараты метаболического действия: солкосерил, актовегин и др.
5. Ангиопротекторы: пирикарбат и др.
Особо хочется подчеркнуть, что важное место в общем арсенале лечебных мероприятий у больных с облитерирующими заболеваниями аорты и артерий нижних конечностей занимает дозированная ходьба – терренкур, которая способствует развитию коллатерального кровообращения.
Сугубо консервативное лечение показано больным с хронической артериальной недостаточностью 1-й стадии и 2А, у пациентов со стадией 2Б и критической ишемией с развитием язвенно-некротических поражений встает вопрос о необходимости восстановления магистрального кровообращения. Благодаря возможностям современных технологий в последние годы появилось много работ по применению баллонной ангиопластики у пациентов с различной локализацией окклюзионно-стенотических поражений артерий таза и нижних конечностей.
Однако не во всех случаях удается применить баллонную пластику вследствие окклюзии аорты или распространенных окклюзий артерий. Попытки реканализации в этих случаях опасны развитием тромбоза магистральных артерий (нередко с тромбозом периферического русла), что неминуемо ведет к ампутации конечности в 60% случаев, а нередко и к летальным исходам.
Виды реконструктивных хирургических вмешательств
При высокой окклюзии аорты, двустороннем поражении артерий конечностей в зависимости от тяжести состояния больного выполняют операции от аортобедренного бифуркационного или линейного шунтирования до подмышечно- или подключично-бедренного бифуркационного шунтирования. Если критическая ишемия имеется только с одной стороны, то при поражении подвздошной и бедренной артерии на контралатеральной конечности выполняется одностороннее перекрестное подвздошно-бедренное, подмышечно- или подключично-бедренное шунтирование.
На современном этапе реконструктивные операции занимают ведущее место в лечении этих больных. Количество таких операций постоянно увеличивается, значительно расширяется их объем, что дает возможность сохранить конечность даже при тяжелых формах хронической артериальной недостаточности. Для рассасывания келлоидных рубцов, возникающих после операции, эффективен препарат Контрактубекс, обладающий фибринолитическим, антитромботическим и кератолитическим действием.
Между тем выполнение полноценной реконструкции нередко вступает в противоречие с возможностями больного перенести оперативное вмешательство. Операции в этих случаях должны быть минимальными по травматичности и продолжительности, так как у подавляющего большинства этого контингента больных имеются тяжелые сопутствующие заболевания, резко ограничивающие функциональные резервные возможности организма [11]. Использование метода комбинированных операций, включающих баллонную ангиопластику в сочетании с открытой операцией под перидуральным или местным обезболиванием, позволяет значительно сократить объем вмешательства и отказаться от сложной хирургической реконструкции на нескольких сегментах.
Больной З., 68 лет, поступил с жалобами на ноющие боли в правой голени и стопе в покое, перемежающуюся хромоту через 30 м.
Ультразвуковая допплерография: значительное снижение магистрального кровотока по правой общей бедренной артерии, коллатеральный кровоток на подколенных и тибиальных артериях.
Лодыжечно-плечевой индекс слева 0,59, справа 0,35.
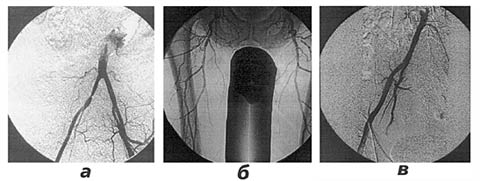
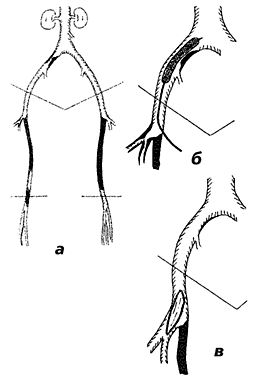
Аортоартериография: критический стеноз общей подвздошной артерии (ОПА) справа; стеноз глубокой бедренной артерии (ГБА) справа; окклюзия обеих поверхностных бедренных артерий (ПБА), сегментарная окклюзия правой подколенной артерии на протяжении 5 см (рис. 1).
Атеросклеротическое поражение артерий (история болезни).
Сопутствующие заболевания: ишемическая болезнь сердца, атеросклеротический кардиосклероз, стенокардия напряжения, хронический бронхит, пневмосклероз, эмфизема легких.
ишемическая болезнь сердца, атеросклеротический кардиосклероз, стенокардия напряжения, хронический бронхит, пневмосклероз, эмфизема легких.
Первым этапом выполнена баллонная ангиопластика ОПА справа, вторым – под перидуральной анестезией – боковая пластика ГБА справа (рис. 2).
В результате отмечена положительная динамика: лодыжечно-плечевой индекс справа увеличился до 0,71 (исходно 0,35). В удовлетворительном состоянии больной выписан на амбулаторное лечение.
Список литературы Вы можете найти на сайте http://www.rmj.ru
1. Покровский А.В., Кошкин В.М., Кириченко А.А. и др. Вазапростан (простагландин Е1) в лечении тяжелых стадий артериальной недостаточности нижних конечностей. Пособие для врачей. М., 1999; 16.
2. Fowkes F.G., Housley E., Cawood E.H. et al. Edinburgh artery study: prevalence оf asymptomatic and symptomatic peripheral arterial disease in the general population. Int J Epidimiol 1991; 20: 384–92.
3. Бураковский А.И., Бокерия Л.А. Сердечно-сосудистая хирургия. М., 1989; 750.
4. Dormandy J., Mahir M., Ascady G. et al. Fate of the patient with chronic leg ischaemia. J. Cardiovasc Surg 1989; 30: 50–7.
5. Stoffers HEJH. Kaiser V. and Knottnerus J.A. Prevalence in the general practice. In: Fowkes FGR, ed. Epidemiology of peripheral vascular disease. London: Springer Verlag. 1992; 109–13.
6. Спиридонов А.А., Фитилева Е.Б., Аракелян В.С. Пути снижения летальности при хирургическом лечении хронической ишемии нижних конечностей. Ж. Анналы хирургии. 1996; 1: 62–6.
7. Биэд Дж.Д. Ампутация или реконструкция при критической ишемии. Ж. Ангитология и сосудистая хирургия 1998; 1 (4): 72–82.
8. Бокерия Л.А., Гудкова Р.Г. Хирургия сердца и сосудов в Российской федерации. М., 1998; 43.
9. Fuchs JSA. Atherogenesis and the medical management of Atherosclerosis. In: Rutherford RB, ed. Vascular surgery. Philadelphia: W.B. Saunders Company. 1996; 1: 222–35.
10. Затевахин И.И., Цициашвили М.Ш., Юдин Р.Ю. Тредмил в диагностике и лечении хронической артериальной недостаточности. М., 1999; 87.
Венозные тромбозы и тромбофлебиты, посттромбофлебитический синдром
Общая информация
Краткое описание
Одобрен
Объединенной комиссией по качеству медицинских услуг
Министерства здравоохранения Республики Казахстан
от «29» марта 2019 года
Протокол №60
Тромбоз глубоких вен конечностей – формирование одного или нескольких тромбов в пределах глубоких вен, сопровождаемое воспалением сосудистой стенки, что приводит к нарушению венозного оттока и является предиктором трофических расстройств.
Тромбофлебит – воспаление стенок вен с образованием в них тромба.
Синдром Мей-Тернера или синдром компрессии левой общей подвздошной вены – результат сдавления указанного сосуда правой общей подвздошной артерией, в связи с чем происходит нарушение оттока крови из левой нижней конечности и малого таза.
Название протокола: Венозные тромбозы и тромбофлебиты, посттромбофлебитический синдром
Код (ы) МКБ-10:
| Код | Название |
| I80.0 | Флебит и тромбофлебит поверхностных сосудов нижних конечностей |
| I80.1 | Флебит и тромбофлебит бедренной вены |
| I80.2 | Флебит и тромбофлебит других глубоких сосудов нижних конечностей Тромбоз глубоких вен БДУ |
| I80.3 | Флебит и тромбофлебит нижних конечностей неуточненный Эмболия или тромбоз нижних конечностей БДУ |
| I80.8 | Флебит и тромбофлебит других локализаций |
| I80.9 | Флебит и тромбофлебит неуточненной локализации |
| I83.1 | Варикозное расширение вен нижних конечностей с воспалением |
| I87.0 | Постфлебитический синдром |
Дата разработки/пересмотра протокола: 2015 год (пересмотр 2018 г.).
Сокращения, используемые в протоколе:
| АЧТВ | – | активированное частичное тромбопластиновое время |
| ВБ | – | варикозная болезнь |
| ТГВ | – | тромбоз глубоких вен |
| ТЭЛА | – | тромбоэмболия легочной артерии |
| ВТЭ | – | венозная тромбоэмболия (ТГВ И ТЭЛА) |
| НОАК | – | новый оральный антикоагулянт |
| АВК | – | антагонист витамина К |
| НМГ | – | низкомоллекулярные гепарины |
| КТ | – | компьютерная томография |
| МКБ | – | международная классификация болезней |
| МНО | – | международное нормализованное отношение |
| ОАК | – | общий анализ крови |
| ПТБ | – | посттромботическая болезнь/синдром |
| УД | – | уровень доказательности |
| УЗАС | – | ультразвуковое ангиосканирование |
| ХВН | – | хроническая венозная недостаточность |
| ЭКГ | – | электрокардиография |
Пользователи протокола: ангиохирурги, хирурги, врачи общей практики.
Категория пациентов: взрослые.
Шкала уровня докозательности:
Критерии, разработанные Европейским обществом кардиологов. Kirchhof P, Benussi S, Kotecha D et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J. Published online ahead of print. doi:10.1093/eurheartj/ehw210.
Классы рекомендаций
| Класс рекомендаций | Определение | Предлагаемая формулировка |
| I | Доказательство и / или общее соглашение, что данный вид лечения или вмешательства благоприятно, полезно, эффективно | Рекомендовано / показано |
| II | Противоречивые доказательства и / или расхождение во мнениях о пользе / эффективности данного вида лечения или вмешательства | |
| IIa | Больше доказательств / мнений в пользу пользы / эффективности | Должно быть рассмотрено |
| IIb | Меньше доказательств / мнений о пользе / эффективности | Может быть рассмотрено |
| III | Доказательство и / или общее соглашение, что данный вид лечения или вмешательства не полезен / не эффективен и в некоторых случаях может быть вредным | Не рекомендуется |
| А | Данные получены во множестве рандомизированных клинических исследований или мета-анализов |
| В | Данные получены в одном рандомизированном клиническом исследовании или крупных не рандомизированных исследованиях |
| С | Консенсусное мнение экспертов и / или небольших исследования, ретроспективных исследований, регистров |
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Классификация
По локализации патологического процесса различают:
Диагностика
МЕТОДЫ, ПОДХОДЫ И ПРОЦЕДУРЫ ДИАГНОСТИКИ
Жалобы:
Анамнез:
Физикальное обследование:
общий осмотр:
пальпация:
Лабораторные исследования:
Коагулограмма:
Инструментальные исследования:
УЗАС:
Флебография, каваграфия:
Показания для консультации узких специалистов:
Дифференциальный диагноз
Дифференциальный диагноз:
клинические
признаки
(корешковый синдром)
тканей
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Апиксабан (Apixaban) |
| Варфарин (Warfarin) |
| Гепарин (Heparin) |
| Гесперидин (Hesperidin) |
| Дабигатрана этексилат (Dabigatran etexilate) |
| Диосмин (Diosmin) |
| Каштана конского семян экстракт (Aesculo hippocastano semen extract) |
| Надропарин (Nadroparin) |
| Ривароксабан (Rivaroxaban) |
| Рутозид (Rutoside) |
| Стрептокиназа (Streptokinase) |
| Сулодексид (Sulodexide) |
| Урокиназа (Urokinase) |
| Эноксапарин натрия (Enoxaparin sodium) |
Группы препаратов согласно АТХ, применяющиеся при лечении
| (B01) Антикоагулянты |
| (M01A) Нестероидные противовоспалительные препараты |
Лечение (амбулатория)
ТАКТИКА ЛЕЧЕНИЯ НА АМБУЛАТОРНОМ УРОВНЕ
Компрессионная терапия: может осуществляться как эластическими, так и неэластическими изделиями: эластические бинты, компрессионный трикотаж.
Таблица №1. Выбор класса компрессионного изделия
Медикаментозное лечение
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЯ НА СТАЦИОНАРНОМ УРОВНЕ
Карта наблюдения пациента, маршрутизация пациента: нет.
Немедикаментозное лечение:
Режим – I или II или III или IV (в зависимости от тяжести состояния);
В случае признаков острого тромбоза, до исключения флотации тромба, подтвержденной инструментально, пациенту требуется постельный режим.
После исключения флотации назначается общий режим.
Диета – №10.
Компрессионная терапия: может осуществляться как эластическими, так и неэластическими изделиями: эластические бинты, компрессионный трикотаж.
Таблица №1. Выбор класса компрессионного изделия
Медикаментозное лечение
Общие рекомендации [8]:
·У пациентов с проксимальным тромбозом глубоких вен или ТЭЛА рекомендуется длительная антикоагулянтная терапия (3 месяца) [УД-B, 1];
·У пациентов с ТГВ до подколенного сегмента или ТЭЛА, не ассоциированный онкологическими заболеваниями, как антикоагулянтная терапия предпочтитение отдается НОАК (дабигатран, ривороксабан, апиксабан, эдоксабан), чем АВК (варфарин) [УД-В, 2,];
·У пациентов с ТГВ на голени или ТЭЛА, ассоциированный онкологическими заболеваниями («рак-ассоциированный тромбоз») как длительная терапия (первые 3 месяца), предлагается НМГ больше чем АВК [УД-В, 2] и НОАК [УД-С, 2];
·Пациентам с ТГВ рекомендуется ограничить рутинное использование компрессионного трикотажа только для профилактики ПТФБ [УД-В, 2];
·Рекомендуется применять системную тромболитическую терапию у пациентов с острой (до 7 дней) ТЭЛА с гипотензией больше чем катетерный тромболизис [УД-В, 2];
·Пациентам с рецидивом ВТЭО, которые не применяли НМГ, рекомендуется использовать НМГ [УД-С, 2];
·Пациентам с рецидивом ВТЭО, которые применяли НМГ, рекомендуется увеличить дозировки НМГ [УД-С, 2];
·Веноактивные препараты (диосмин, гесперидин, рутозиды, сулодексид, микронизированную очищенную фракцию флавоноидов или экстракт семян конского каштана [эсцин]) рекомендовано применять в дополнение к компрессионной терапии пациентам с болью и отеком, обусловленное хроническим заболеванием вен в странах, где эти препараты доступны. [УД-В, 2,3].
Тромболизисная терапия:
Цели лечения:
Хирургическое вмешательство:
Эндоваскулярная хирургия:
Гибридная хирургия:
Сочетание вышеуказанных методов.
Показания к операции:
Противопоказания к операции:
Дальнейшее ведение:
Индикаторы эффективности лечения:
Госпитализация
ПОКАЗАНИЯ ДЛЯ ГОСПИТАЛИЗАЦИИ С УКАЗАНИЕМ ТИПА ГОСПИТАЛИЗАЦИИ
Показания для экстренной госпитализации:
Показания для плановой госпитализации:
Информация
Источники и литература
Информация
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ВНЕДРЕНИЯ ПРОТОКОЛА
Список разработчиков протокола:
Конфликт интересов: нет.
Рецензенты:
Конысов Марат Нурышевич – доктор медицинских наук, главный врач КГП на ПХВ «Атырауская городская больница».
Условия пересмотра протокола: пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.