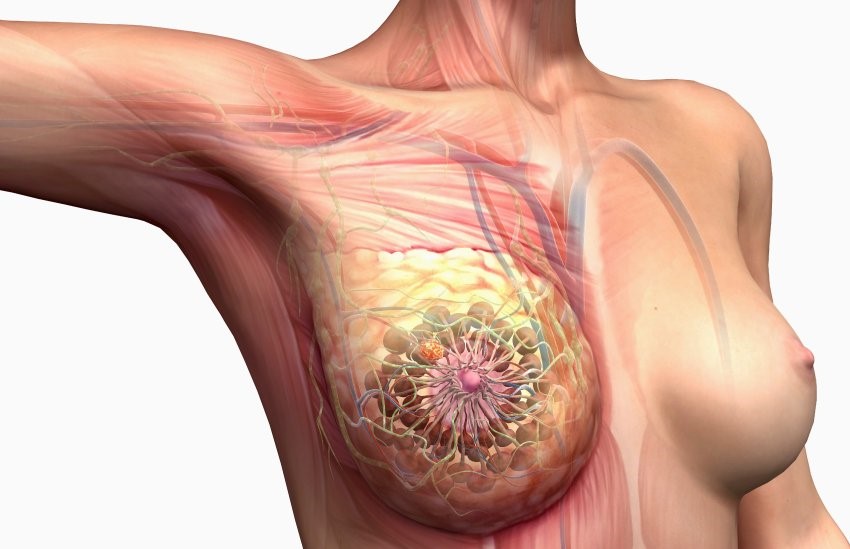
вторично отечно инфильтративная форма
Материалы конгрессов и конференций
VIII РОССИЙСКИЙ ОНКОЛОГИЧЕСКИЙ КОНГРЕСС
ВОЗМОЖНОСТИ ЛЕЧЕНИЯ ОТЁЧНО-ИНФИЛЬТРАТИВНОЙ ФОРМЫ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ
С.М. Портной
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, Москва
Под отёчно-инфильтративной формой рака молочной железы (РМЖ) понимают варианты болезни, сопровождающиеся отёком и/или гиперемией кожи молочной железы. Для истинной или первичной отечно-инфильтративной формы (ОИФ) РМЖ характерно диффузное распространение опухоли по тканям молочной железы, отсутствие выявляемого первичного опухолевого узла и плохой прогноз. Сходный прогноз наблюдается и при вторичной ОИФ, то есть узловой форме РМЖ, сопровождающейся вторичным отёком кожи.
ОИФ РМЖ отличается от локализованного рака не только степенью распространённости опухоли; при этом варианте возрастает частота опухолей с неблагоприятным прогнозом и снижается частота относительно благоприятных прогностических факторов. Так, частота редких морфологических форм рака с относительно доброкачественным течением (слизистый, папиллярный, тубулярный и медуллярный) при раннем РМЖ (T1-2N0M0) составляет 11,4%, а при местно-распространенном, включая и ОИФ, – 2,6% (2p=0,0001). Доля анеуплоидных многоклоновых (по индексу плоидности ДНК) опухолей при узловой форме РМЖ составляет 6%, а при ОИФ – 20% (2p=0,0013); частота поражения лимфатических узлов – 39% и 87% (2p=0,0000); частота рецепторонегативных опухолей по рецепторам эстрогенов – 43% и 55% (2p=0,0058), по рецепторам прогестерона – 49% и 65% (2p=0,0006) соответственно (1).
Лечение ОИФ РМЖ складывается из предоперационного (индукционного) лечения, местного лечения (операция или ЛТ, или сочетание ЛТ с операцией) и адъювантной терапии.
Рис. 1. Безрецидивная (а) и общая (б) выживаемости больных РМЖ T1-4N1-2M0 и T3-4N0M0 стадий без адъювантной терапии.
Предоперационная (индукционная) химиотерапия
Трудно переоценить значение эффективности предоперационной химиотерапии (ХТ): прогрессирование на фоне ХТ означает начало конца, эффективная ХТ даёт шансы на радикальное излечение.
Схемы CMF, VCMFP. Истинная ОИФ РМЖ не является исходно резистентной к лечению. Так, например, проведение ХТ по схеме VCMFP в сочетании с эндокринной терапией (ЭТ) позволило в 84% случаев добиться эффекта различной степени выраженности и выполнить больным радикальную операцию (2). Дальнейшее течение болезни, в большинстве случаев, оказывается обескураживающим. Несмотря на проведение профилактической ХТ по схеме CMF и профилактической ЭТ, уже на первом году наблюдений рецидивы и метастазы развиваются в 50% случаев, 3-летняя БРВ составляет 24%, 5-летняя – 19% (3). Таким образом, второй особенностью ОИФ РМЖ является быстро манифестирующаяся лекарственная устойчивость; ответом на это должно быть последовательное проведение нескольких линий системной терапии.
Схемы, включающие антрациклины (FAC, FEC, AC, EC), применяются наиболее часто, значительно реже антрациклины назначаются в виде монохимиотерапии. Поддержка кроветворения гранулоцитарным (Г-КСФ) или гранулоцитарно-макрофагальным (ГМ-КСФ) колониестимулирующими факторами позволяет увеличить интенсивность дозы препаратов, что может привести к повышению эффективности ХТ.
U. Coskun и соавт. (4) описывают свой опыт проведения предоперационной ХТ у 91 больной местно-распространенным РМЖ (30 больная – IIIa стадия, 61 больная – IIIb стадия). ХТ по схеме FAC или AC была эффективна в 91%, по схеме FEC или EC – в 82%, по схеме CMF – в 60 % случаев (p 0.05). Полученные данные могут свидетельствовать о перспективности дальнейшего изучения эффективности высокодозной ХТ в качестве адъювантного лечения местно-распространенного РМЖ (14).
Лучевая терапия. Относительно сроков проведения лучевой терапии в лечении местно-распространенного РМЖ существуют различные мнения. Согласно новой концепции, лучевую терапию проводят после операции и завершения адъювантной ХТ (39,40,36;). Schwartzberg L. и соавт., (9), L.E. Morrell и соавт. (20), M. Colozza и соавт. (19) проводят лучевую терапию после операции перед адъювантной ХТ; а V.F. Semiglazov и O.M. Golubeva (32), J. Yau и соавт. (41) – перед операцией. Наконец, некоторые авторы предпочитают проводить лучевую терапию одновременно с предоперационной ХТ (30,12,42).
40. Pinedo H.M., Honkoop A.H., Boven E. et al. Improved disease-free survival (DFS) of patients with locally advanced breast cancer (LABC) using prolonged dose intensive neoadjuvant doxorubicin (A), cyclophosphamide (C) and GM-CSF //Proc. Am. Soc. Clin. Oncol. 1996. Vol. 15. P. 88.
41. Yau J., Lee K., Verma S. et al. A phase III study of high dose cyclophosphamide, etoposide, and cisplatin (HDCVP) without marrow or stem cells support in patients with high risk primary breast carcinoma //Proc. Am. Soc. Clin. Oncol. 1996. Vol. 15. P. 19).
Вторично отечно инфильтративная форма
Российский научный центр рентгенорадиологии МЗ РФ, Москва
ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России, Москва
ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России, Москва
ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России, Москва
Отечно-инфильтративный рак молочной железы: целесообразность разделения на первичную и вторичную формы
Журнал: Онкология. Журнал им. П.А. Герцена. 2015;4(1): 21-24
Чхиквадзе В. Д., Колесник А. Ю., Меских Е. В., Лагожина И. А. Отечно-инфильтративный рак молочной железы: целесообразность разделения на первичную и вторичную формы. Онкология. Журнал им. П.А. Герцена. 2015;4(1):21-24.
Chkhikvadze V D, Kolesnik A Yu, Meskikh E V, Lagozhina I A. Edematous-infiltrative breast cancer: Expediency of its division into primary and secondary forms. P.A. Herzen Journal of Oncology. 2015;4(1):21-24.
https://doi.org/10.17116/onkolog20154121-24
Российский научный центр рентгенорадиологии МЗ РФ, Москва
Цель исследования — уточнение целесообразности разделения отечных форм рака молочной железы на первичную и вторичную формы. Материал и методы. В настоящем исследовании изучены и сопоставлены ретроспективные данные о результатах инструментальных и патоморфологических исследований у 70 больных отечно-инфильтративным раком молочной железы (ОИРМЖ). Результаты. Установлено, что с внедрением в клинику цифровой маммографии качество диагностики значительно улучшилось, что позволило выявить опухолевое поражение при наличии отека молочной железы у 77,7% больных, в то время как при использовании аналоговой маммографии этот показатель не превышал 35,3%. При выполнении УЗИ опухолевый узел в молочной железе на фоне отека был выявлен у 76—85,1% больных. Эти результаты подтверждают наибольшую чувствительность метода для выявления объемных образований при наличии отека тканей по сравнению с маммографией. При исследовании послеоперационного материала опухолевая ткань была выявлена у 100% больных. Заключение. Разделение ОИРМЖ на первичные и вторичные формы не имеет достаточного клинического и морфологического обоснования, и, по всей вероятности, было связано с недостатками аналоговой маммографии.
Российский научный центр рентгенорадиологии МЗ РФ, Москва
ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России, Москва
ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России, Москва
ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России, Москва
Отечно-инфильтративный рак молочной железы (ОИРМЖ) — редкое злокачественное новообразование, которое составляет 1—5% от всех случаев РМЖ [1, 2]. Хотя масштабы заболеваемости ОИРМЖ невелики, существует тенденция к росту, которая в среднем составляет 1,23% в год, в то время как для неотечных форм — 0,42% [3].
Одной из характеристик ОИРМЖ является агрессивность течения заболевания. Смертность пациентов с данной формой заболевания в 2 раза превышает смертность пациентов с неотечными формами РМЖ [4]. При этом сроки установления диагноза влияют на долгосрочные результаты лечения [1].
В связи с редкостью встречаемости ОИРМЖ существуют нечеткости в определениях, что следует относить к этой форме РМЖ и какие существуют его варианты. Следует отметить, что имеются и терминологические противоречия у разных авторов и в различных регионах. Так, в англоязычной литературе чаще применяется термин «воспалительный рак молочной железы». До недавнего времени рекомендации и руководства по диагностике и лечению РМЖ были посвящены в основном неотечным формам. В последние годы все больше публикаций посвящается углубленному исследованию ОИРМЖ.
Клинически ОИРМЖ был описан в 1814 г. шотландским хирургом Чарльзом Беллом. Впервые термин «воспалительный рак молочной железы» был предложен в 1924 г. Lee и Tannebaum. Ранее ОИРМЖ упоминался, как синдром Фолькмана у беременных женщин, лактационная карцинома, раковый мастит, острая карцинома молочной железы и т. д. [3, 5].
В клинической международной классификации TNM (VII издание 2010 г.) ОИРМЖ рассматривается как в категории T4d, так и в категории Т4b, при этом принципиальные различия отечного рака в данных категориях не указываются [6]. В отечественной литературе и клинической практике в настоящее время имеется разделение ОИРМЖ на первичную и вторичную формы, где первое подразумевает наличие клиники отека молочной железы без формирования опухолевого узла, а второе — отек молочной железы при существовании опухолевого узла или диффузном росте опухоли [5, 7—9]. Это разделение отсутствует в принятых международных критериях установления диагноза и вносит существенную нечеткость при формулировке диагноза.
Разделение ОИРМЖ на первичную и вторичную формы возникло тогда, когда методы лучевой и ультразвуковой диагностики не были столь совершенны, как в настоящее время. Практикующие врачи не имели возможность получить полную картину болезни, в большинстве случаев отсутствовала визуализация опухоли, в связи с чем материал для морфологического исследования получали не всегда. Клиницисты вынуждены были опираться на данные физикального осмотра, при котором на фоне отечности ткани железы не всегда пальпировался опухолевый узел. С развитием лучевых и ультразвуковых методов диагностики ситуация изменилась, и теперь имеются более широкие возможности для визуализации опухоли и морфологического подтверждения диагноза. Однако понятие первичного и вторичного отечного рака укоренилось, в связи с чем в настоящее время имеется существенная путаница в формировании диагноза при отечных формах рака молочной железы.
По классификации опухолей молочных желез ВОЗ (2012), воспалительный рак молочной железы (ОИРМЖ) характеризуется клинической картиной воспаления (гиперемия, отек тканей и кожи, симптом лимонной корочки), наличием опухолевой массы в ткани железы и множественными опухолевыми эмболами в лимфатических сосудах кожи. Чаще всего опухоль имеет протоковый фенотип, не всегда образовывает опухолевый узел и нередко поражает строму диффузно, что затрудняет оценку размера опухоли [10—12].
Диагноз ОИРМЖ устанавливается на основании наличия клинических симптомов и морфологического подтверждения диагноза [7].
К характерным симптомам ОИРМЖ относятся отек, гиперемия кожи молочной железы без подлежащей опухоли и увеличение ее размера. С отеком связано увеличение ямок волосяных фолликулов, в результате чего внешний вид кожи напоминает лимонную корочку. У большинства пациентов опухолевая масса не распределяется при клиническом обследовании в связи с выраженным отеком кожи и ткани железы и нередко из-за диффузного опухолевого поражения без четкого формирования узла [10—12].
Для инструментальной диагностики ОИРМЖ используются стандартные методы визуализации — маммография и ультразвуковое исследование (УЗИ). В настоящее время применяются новые методы исследования, такие как магнитно-резонансная томография (МРТ) и позитронно-эмиссионная томография/компьютерная томография (ПЭТ/КТ), претендующие на место стандартных [13].
УЗИ является наиболее информативным из стандартных методов исследования при ОИРМЖ, в возможности которого входит определение паренхиматозных изменений, что облегчает дальнейшую морфологическую диагностику. Опухолевая масса в молочной железе при выполнении УЗИ выявляется в 80% случаев [14]. Маммография — менее чувствительный метод для визуализации паренхиматозных изменений при отечном раке молочной железы [14].
Наиболее точным методом исследования для обнаружения изменений в паренхиме молочной железы при отечно-инфильтративном раке является МРТ, однако возможности применения этого метода как рутинного, к сожалению, весьма ограничены [15].
ПЭТ представляет собой молекулярный метод визуализации, который чувствителен к функциональным или метаболическим изменениям в тканях, а совмещение ПЭТ с компьютерной томографией позволяет топировать выявленные изменения. При ОИРМЖ отсутствие клинически определяемой опухолевой массы делает ПЭТ привлекательным методом как для установления диагноза, так и для оценки ответа на проведенную терапию [16—18].
Цель исследования — уточнение целесообразности разделения отечных форм рака молочной железы на первичную и вторичную формы.
Материал и методы
Настоящая работа основана на анализе результатов лечения и обследования 70 больных ОИРМЖ. Все больные находились на лечении в Российском научном центре рентгенорадиологии (РНЦРР) с 1994 по 2013 г. Больные были разделены на 2 группы в зависимости от времени диагностики и лечения. Временной границей послужил 2009 г. — время начала применения в клинике цифровой маммографии. В 1-ю группу включили 34 больных, проходивших лечение с 1994 по 2009 г., во 2-ю — 36 больных, проходивших лечение с 2009 по 2013 г.
В нашем исследовании изучены и сопоставлены ретроспективные данные о клинической картине, результатах инструментальных и патоморфологических исследований в обеих группах.
Методом лучевой диагностики являлась маммография: в 1-й группе — аналоговая, во 2-й — цифровая.
Цифровая маммография обладает преимуществами, свойственными цифровым методам вообще, включая возможность обрабатывать изображения при помощи специального программного обеспечения, чтобы облегчить их восприятие [19]. Стало возможным получать больше диагностической информации при обследовании молочных желез за счет применения инструментов обработки снимков. Используя данную систему, можно воспроизвести мельчайшие патологические изменения при помощи разных дополнительных функций обработки снимков, таких как панорамирование, изменение масштаба снимка, измерение длин прямолинейных и криволинейных отрезков, измерение углов, измерение произвольных площадей, изменения яркости/контрастности, возможности инверсии изображения, поворот изображения. Кроме того, существует возможность просмотра одновременно нескольких снимков, что позволяет проводить сравнительную оценку структуры левой и правой молочных желез, а также проводить мониторинг состояния молочных желез в динамике [20]. Расширение возможностей в диагностике заболеваний молочных желез при помощи использования цифровой техники постепенно приводит к замене аналоговых рентгеновских аппаратов цифровыми или использованию цифровых рентгеновских комплексов для обработки рентгеновского изображения. В РНЦРР, как указывалось выше, аналоговая маммография замещена цифровой в 2009 г.
В обеих группах с целью дообследования выполняли УЗИ молочных желез. Этот метод еще с конца 90-х годов стал обязательным дополнением к маммографии. Считается, что УЗИ молочных желез позволяет выявить узлы, которые не всегда удается визуализировать при выполнении рентгенологического исследования, и уточнить природу изменений. Со временем возможности метода расширились благодаря появлению дополнительных опций.
Проведено морфологическое исследование послеоперационного материла у больных ОИРМЖ.
Результаты и обсуждение
При анализе данных осмотра больных в группах установлено, что увеличение размера пораженной молочной железы наблюдалось у 87% больных, гиперемия кожи железы — у 93,6%, а отек кожи — у 100%, опухолевый узел пальпировался у 38,2% больных. По всей вероятности, этим и обусловлено разделение ОИРМЖ на первичные и вторичные.
По результатам маммографии в нашем исследовании в 1-й группе больных (больные до 2009 г.) объемное образование выявлено у 35,3% (n=12). Диффузное увеличение плотности тканей молочной железы было выявлено у 64,7% (n=22) больных. Во 2-й группе объемное образование выявлено у 77,7% (n=28), а диффузное увеличение плотности паренхимы у 22,3% (n=8). Таким образом, очевидно, что с внедрением в клинику цифровой маммографии качество диагностики значительно улучшилось, что позволило выявить опухолевое поражение при наличии отека молочной железы у 77,7% больных, в то время как при использовании аналоговой маммографии этот показатель не превышал 35,3% (р 
При выполнении УЗИ в 1-й группе больных ОИРМЖ (27 пациенток) опухолевый узел в молочной железе был выявлен у 76%, а во 2-й — у 85,1%. Улучшение показателей у пациенток 2-й группы связано с усовершенствованием аппаратуры и появлением дополнительных опций. Эти результаты подтверждают наибольшую чувствительность метода для выявления объемных образований при наличии отека тканей по сравнению с маммографией.
При исследовании послеоперационного материала опухолевая ткань была выявлена у 100% больных обеих групп: в виде опухолевого узла — у 79,3 и 87,5%, в виде диффузного роста опухоли без четкого формирования узла — у 20,7 и 12,5% соответственно. Размер узла варьировал от 0,2 до 10 см. Маленьким размером узла на фоне отечной ткани молочной железы и объясняется затруднение его визуализации при выполнении рентгенологического исследования.
Заключение
Таким образом, по результатам исследования нами установлено, что разделение ОИРМЖ на первичные и вторичные формы не имеет достаточного клинического и морфологического обоснования. Маммография и УЗИ молочных желез являются достаточно эффективными методами диагностики ОИРМЖ, однако имеются наблюдения, когда отсутствует визуализация опухоли на фоне отека. Возможности визуализировать опухоль при рентгенологическом исследовании молочных желез на фоне отека тканей увеличились с появлением в клинической практике цифровой маммографии. Это позволяет судить о том, что разделение ОИРМЖ на первичную и вторичную формы, по всей вероятности, было связано с недостатками аналоговой маммографии.
Концепция и дизайн исследования: В.Д.Ч., Е.В.М., А.Ю.К.
Инфильтративный рак молочной железы
Молочная железа состоит из 20 железистых долек, разделенных между собой жировой клетчаткой. Каждая из них вырабатывает молоко, поступающее к соску по млечным протокам. Рак молочной железы развивается из эпителиальных клеток протоков, либо из клеток железистых долек. Существует множество разновидностей онкологических опухолей груди. Одна из них – инфильтративный рак молочной железы.
Особенности инфильтративного рака
Инфильтративный рак молочной железы имеет отличия от других форм. Образование проникает (инфильтрирует) в окружающие ткани, жировые и мышечные. Доброкачественные опухоли, даже при больших размерах, не склонны к прорастанию в соседние структуры.
Еще одна особенность инфильтративной опухоли – быстрое образование и распространение метастазов в подмышечные, надключичные и подключичные лимфоузлы. Если не начать срочное лечение, метастазы появятся и во внутренних органах: печени, головном мозге, позвоночнике. На этом этапе прогноз для пациентки неблагоприятный.
Инфильтративный рак имеет высокую степень агрессивности. Злокачественные клетки могут сохраняться в организме длительное время после лечения. Это приводит к образованию скрытых метастазов. Даже после пройденной операции и химиотерапии, возможен рецидив.
Виды инфильтративного рака
Инфильтрирующий рак молочной железы разделяется на несколько видов. Особенности есть у каждого.
Отечно-инфильтративный
Диагностируется довольно редко, в 1%-5% случаев. Выделяют диффузную и узловую форму. Узловая более агрессивна, метастазы возникают на первом году заболевания. Обе формы плохо поддаются лучевой терапии и химиотерапии. Смертность пациенток с этой формой патологии в 2 раза превышает смертность пациенток с неотечными формами рака молочной железы.
Симптомы болезни напоминают симптомы мастита. Это отек и увеличение молочных желез, выраженное покраснение кожи.
Инфильтрирующий протоковый
Инфильтративный протоковый рак молочной железы поражает клетки эпителия млечных протоков. Это самая распространенная форма онкологии среди женщин старше 40 лет.
Инфильтрирующий протоковый рак молочной железы имеет несколько форм:
Протоковая опухоль диагностируется в 80% случаев. Она напоминает твердый неподвижный узел овальной формы с неровными краями, проросший в окружающие ткани. Ее объем составляет от 5 – 50 мм. Внутри пораженной области могут присутствовать некротические участки.
Инфильтративный дольковый
Возникает из железистой ткани груди. Чаще всего опухоль локализуется во внутренне-верхнем и наружно-верхнем квадранте груди. Выявляется в 10 – 15% всех случаев. Заболевают нерожавшие женщины в возрасте до 45 лет.
При пальпации образование не причиняет дискомфорта, имеет округлую форму и плотную структуру, характерную для раковых опухолей. На маммографических снимках будут видны нечеткие границы, обозначающие слияние с окружающими тканями. В 30% случаев дольковый рак выявляется в правой и левой железах одновременно.
Неспецифический инфильтративный
Выявляется редко, в 1%-5% случаев. Имеет несколько форм:
Прогноз зависит от поражения лимфоузлов. При 1 степени есть метастазы в единичном лимфоузле, при 2 степени поражаются 4 – 9 лимфоузлов, при 3 степени злокачественные клетки есть более чем в 10 регионарных лимфоузлах.
Причины и симптомы
Невозможно назвать точную причину, почему у женщины развивается инфильтрирующая карцинома молочной железы. Значение имеет наследственный фактор. Существуют гены, отвечающие за регенерацию клеток с поврежденной ДНК и регулирующие механизмы клеточного роста. При различных мутациях этих генов риск развития атипичного процесса значительно повышается.
Если женщина страдает от сбоев в гормональной системе, повышается вероятность развития гормонозависимой опухоли.
К предрасполагающим факторам относят:
Патологические симптомы поначалу отсутствуют. По мере роста опухоли она начинает проявлять себя. Женщина может жаловаться на болезненность груди, чувство жжения и зуда, патологические выделения из сосков. Часто деформируется форма молочной железы, изменяется кожа. Она краснеет, становится сморщенной. При дольковом раке сосок втягивается внутрь.
Диагностика
С помощью каких исследований диагностируют инфильтративный рак:
Чтобы понять, начался ли процесс метастазирования, женщине проводят ПЭТ-КТ. Этот метод позволяет найти регионарные и отдаленные метастазы.
Как лечат инфильтративный рак груди
Схема лечения будет определена после гистологического исследования. Какие методы помогают бороться с заболеванием:
Обойтись без мастэктомии удается редко. Современные хирургические методики позволяют женщине сохранить эстетичный вид груди даже после оперативного вмешательства. Иногда мастэктомию совмещают с маммопластикой. Сложно заранее ответить на вопрос, сколько лимфатических узлов придется удалить. Все зависит от того, есть ли в них атипичные клетки.
Прогноз выживаемости
Вероятность вылечиться сильно зависит от степени злокачественности опухоли. Выделяют несколько степеней:
При степени дифференцировки g1 прогноз благоприятный, при g4 он гораздо менее оптимистичен.
Кроме степени злокачественности, нужно учитывать стадию заболевания. Если рак обнаружили на первой стадии, прогноз выживаемости будет высоким. Пятилетний рубеж перешагивают 95% пациенток. На второй стадии пятилетняя выживаемость снижается до 70 – 85%. Многое зависит от наличия метастаз в близрасположенных лимфоузлах. Инфильтративный рак 3 стадии удается победить 35 – 50% пациенток. 4 стадия считается терминальной, но около 10% женщин живут в течение 10 лет при правильно подобранной терапии.
Проблема заключается в высокой агрессивности инфильтративного рака. Первая стадия может перейти в третью за несколько месяцев. Из-за отсутствия выраженных симптомов на начальных стадиях женщины обращаются к врачу, когда их начинает беспокоить не сама опухоль, а отдаленные метастазы.
Поэтому нельзя пренебрегать профилактическими обследованиями. Регулярное посещение маммолога и прохождение маммографии 1 раз в 2 года позволяют вовремя обнаружить заболевание.
Компания «Пациент менеджмент» на протяжении многих лет занимается организацией индивидуального медицинского обслуживания высокого качества.
За годы работы мы накопили статистику по ведущим зарубежным клиникам и готовы рекомендовать пациентам для лечения инфильтративного рака молочной железы только те медицинские центры, где действительно окажут наиболее эффективную помощь.